Les Traitements Biologiques
Généralités
Nous ne reviendrons pas sur les traitements étiologiques antiinfectieux, hormonaux, vitaminiques, détoxicants, les traitements des perturbations fonctionnelles viscérales ou métaboliques, etc., que nous avons décrits à propos des syndromes psychiatriques correspondants.
Nous allons dans ce chapitre étudier seulement les techniques thérapeutiques non spécifiques (mais non pas irrationnelles, comme nous le verrons), que l’on emploie en psychiatrie pour modifier favorablement le substratum organique des maladies. Ces méthodes peuvent être groupées sous deux chefs principaux :
1° Les traitements pharmacologiques qui prennent actuellement une extension considérable en raison de l’apparition constante de nouvelles substances psychotropes de grande efficacité et dont le mécanisme d’action se précise chaque jour davantage grâce aux progrès de la neuro-physiologie, de la psycho pharmacologie et des techniques biochimiques.
2° Les traitements dits de choc qui ont fait leur preuve mais dont l’emploi tend à se limiter de plus en plus en raison même du développement et de l’efficacité des traitements précédents. Ces traitements de choc (nous ne retiendrons que les chocs insuliniques et électriques) peuvent être groupés car, si leur mécanisme d’action reste mal connu, on peut cependant le ramener à un grossier dénominateur commun, une sorte de « commotion psychosomatique », de « stress » efficace par son influence sur les mécanismes régulateurs de la vie végétative et de la dynamique cérébrale.
Nous ne ferons que citer les techniques chirurgicales ou la psychochirurgie (lobotomie, lobectomie, etc.) qui ne sont actuellement, après des discussions passionnées, que très rarement pratiquées quoique leurs effets thérapeutiques aient été dans certains cas incontestables.
Enfin les très nombreux traitements par les agents physiques (hydrothérapie, chimatothérapie, électrothérapie, massage, etc.) constituent dans le traitement total un appoint non négligeable.
LES TRAITEMENTS PHARMACOLOGIQUES
L’abondance et l’efficacité des chimiothérapies ne doivent faire oublier ni les autres traitements biologiques, ni la nécessité conjointe de l’action psychothérapique. C’est à bien comprendre les activités réciproques des procédés biologiques sur le système nerveux et des situations psycho-sociales sur le Moi que doit s’efforcer le psychiatre pour coordonner ses efforts et ceux de l’entourage du patient, hospitalisé ou non.
En ce qui concerne les médications actuelles, si précieuses, il faut leur reconnaître une capacité toute nouvelle de s’associer aux actions psychothérapiques. Les modifications qu’elles apportent à l’état de la conscience ou de l’humeur sont généralement graduelles, et l’exploitation de ces modifications sera donc possible à chaque instant. Il en résulte un profond changement dans l’ambiance des lieux d’hospitalisation — ou du milieu familial, quand cela est possible — dans le maniement des relations entre le malade et l’entourage, et un changement non moins grand dans les expressions morbides, puisque très rapidement le malade est sous l’influence des médicaments. Des effets nouveaux apparaissent, les uns dus à des « actions secondaires » du médicament (c’est-à-dire non recherchées), parfois gênantes, les autres dus à des modifications symptomatiques ou structurales de la maladie qui prend désormais des visages inconnus naguere, une nouvelle semiologie des psychoses apparaît. Cependant les chimiothérapies, comme les cures de sommeil à l’époque de leur apparition et comme également la cure de Sakel à une époque plus ancienne encore, posent, mais avec plus d’éclat encore en raison de leur action modificatrice et régressive sur les structures neurologiques, une tendance à penser en termes trop physiologiques. Aussi, comme nous l’avons déjà signalé dans différents chapitres, attitudes physiologique et psychologique sont dans et . l’état actuel de la psychiatrie, indissolublement complémentaires dans la conduite de toute chimiothérapie.
La place de la psychothérapie dans tous les cas consiste, en dehors de ses effets de sens, sur lesquels nous ne reviendrons pas à aménager une relation malade-médecin satisfaisante, ce qui suppose de prendre le temps d’écouter et de donner des explications au prorata de la personnalité du patient : prévenir à du délai de l’effet des médicaments, de leurs effets latéraux ; essayer de les atténuer par l’adjonction d’un correcteur ; porter une grande attention à Îa posologie : quantité et heures des prises, rythme de la progression et de la décroissance des doses, les incompatibilités, etc.
On trouvera une documentation importante dans les deux ouvrages suivants : Cuche (H.), Gérard (A.), Loo (H.), Zarifian (E.). — Séminaire de Pyschiatrie biologique à l’hôpital Sainte-Anne, publié par les Éditions Fournier Frères, Gennevilliers, 1982 et L’Encéphale, n° 1, 1982, Doin éditeurs. Neuromédiateurs (Ouvrage collectif). Confrontation Psychiatrique, n° 22, Paris. Éditions Spécia, 1983, 446 pages.
Mode d’action et appréciation de l’effet des médicaments. — Quel est le mode d’action des psychotropes dans le fonctionnement cérébral ?
Il est évident que les substances psychotropes ont une action sur le comportement en agissant, directement ou indirectement, mais nécessairement, sur le métabolisme des cellules cérébrales. Cette action se fait par l’intermédiaire des neuro-médiateurs ou mono-amines cérébrales, synthétisées à partir du tryptophane et de la tyrosine et constituées par les catécholamines (noradrénaline, adrénaline, dopamine et aussi sérotonine, acétylcholine, histamine, GABA (acide gamma-aminobutyrique) qui sont actuellement les mieux étudiés. De très nombreuses autres molécules ayant fonction de neurotransmetteurs ont été identifiées particulièrement les neuropeptides qui comprennent notamment les endorphines et la substance P. La neurotransmission et la modulation se font au niveau de la synapse. Toutes les phases, biosynthèse, stockage, libération, dégradation, recapture, etc., du métabolisme complexe des neurotransmetteurs peuvent être l’objectif d’une intervention pharmacologique qui va avoir pour effet d’augmenter ou de diminuer et même d’inhiber la réponse biologique de ce transmetteur. « En fait, c’est au niveau de l’interaction des neurotransmetteurs avec les récepteurs que portent les efforts de la psychopharmacologie moderne qui tend à promouvoir des produits agissant directement et spécifiquement sur un type de récepteur déterminé » (A. Nieoullon, 1982). Les neurotransmetteurs se répartissent dans le S. N. C. selon des voies et des systèmes sérotoninergiques, dopaminergiques, noradrénergiques, adrénergiques, cholinergiques et GABA ergiques. Il existe une certaine compétition entre les diverses substances et c’est la substance dont le pouvoir de fixation est le plus fort qui empêche le transport des autres. Ce phénomène permet de comprendre l’effet parfois décevant de la prescription de certaines associations de trop nombreux psychotropes.
L’élimination urinaire des médicaments varie également selon la structure (liposoluble ou hydrosoluble) des substances. Donc il faut retenir que la concentration sanguine, l’élimination du psychotrope sont individuelles car elles dépendent tout à la fois de l’âge, du sexe, de l’état émotionnel, d’altérations enzymatiques et aussi de facteurs génétiques.
C’est pour toutes ces raisons que les études actuelles se portent sur l’action des psychotropes au niveau des récepteurs. Ces études nécessitent que l’on recherche les conséquences de l’imprégnation du médicament au niveau cellulaire et synaptique. On cherche ainsi à suivre les variations de concentration des aminés cérébrales dans les divers sites cérébraux, où elles sont catabolisées d’une manière différente sous l’action des substances psychotropes.
Pour plus de détails sur la transmission chimique de l’influx nerveux, les localisations des divers neurotransmetteurs dans le S. N. C. et les principales voies qu’ils utilisent pour former des systèmes : monoaminergiques, dopaminergiques, noradrénalinergiques, adrénergiques, sérotoninergiques, cholinergiques, acides aminés (GABA ergi ques), principales voies peptidergiques (endorphines, substance P) ainsi que les diffé rentes étapes du métabolisme des neurotransmetteurs (biosynthèse, stockage, libération), les mécanismes intervenant dans le contrôle du fonctionnement biochimique du neurone, l’aspect neuropharmacologique et les implications des neurotransmetteurs dans le comportement sensorimoteur et les principaux comportements neuro-psychiatriques se reporter à l’article de A. Nieoullon (Encycl. méd.-chir. (Neurologie), Paris, 17003, A-10, 10, 1982).
L’action des substances psychotropes vis-à-vis des mono-amines peut se résumer ainsi :
— La réserpine provoque une déplétion cellulaire des mono-amines et par suite de la libération des stocks de mono-amines provoque leur catabolisme. On observe ainsi la libération et l’élévation de l’excrétion des métabolites de la sérotonine. Il est possible d’autre part que les troubles extra-pyramidaux qui suivent l’absorption de réserpine soient dus à une déficience d’une catécholamine (la dopamine).
— Le groupe des anti-dépresseurs I. M. A. O. inhibe la mono-amine-oxydase. Or celle-ci catabolyse la sérotonine il en résulte une augmentation de la teneur en sérotonine provoquant une action anti-dépressive.
— D’autres psychotropes le largactil, les butyrophénones, etc. bloquent les récepteurs catécholaminergiques (les catécholamines sont des stimulants de la formation réticulée) et empêchent la pénétration intra-cellulaire des mono-amines.
— Certains psychotropes anti-dépresseurs comme l’imipramine (Tofranil*) ou l’amitriptyline (Elavil* ou Laroxyl*) augmentent la sensibilité de certains récepteurs aux mono-amines.
— Enfin les psychotropes peuvent aussi avoir une action inhibitrice sur la synthèse des mono-amines.
A titre d’exemples, prenons celui de la sérotonine. Le rôle physiologique de cette aminé semble être celui d’un médiateur qui stimulerait les centres parasympathiques sous-corticaux ou inhiberait les centres sympathiques, elle est inactivée par dégradation enzymatique (la mono-amine-oxydase). Il en résulte que des drogues inhibitrices de la mono-amine-oxydase (iproniazide et ses dérivés) provoquent une augmentation notable de la teneur en sérotonine et par suite un effet anti-dépresseur. De même d’autres médiateurs comme l’acétylcholine ou l’histamine jouent certainement un rôle important au niveau des centres nerveux, mais ce rôle demeure encore obscur. C’est ainsi que l’atropine, la scopolamine, la bénactyzine, ont un rôle anti-cholinergique ; des neuroleptiques, la lévomépromazine (Nozinan*) et l’alimémazine (Théralêne*) sont de puissants anti-histaminiques. L’halopéridol et l’imipramine (Tofranil*) ont également Classification. un effet anti-histaminique.
On s’est efforcé également de déterminer la puissance d’action des substances psychotropes et de les classer dans un ordre quantifiable. Ces mesures ont été faites, et sont reprises, à l’apparition de chaque nouvelle drogue par de nombreuses méthodes dont nous citerons les principales. Les méthodes pharmacologiques sont essentiellement basées sur l’observation d’animaux soumis à la drogue (étude du comportement général, des réflexes, du comportement instinctif, leurs examens par les diverses méthodes d’électro-physiologie : électrocorticographie, potentiels d’action, etc.), et les méthodes biochimiques (l’action des drogues à l’égard des médiateurs chimiques du cerveau : sérotonine, catécholamines, etc.). Les méthodes d’appréciation psychologique utilisent la méthode des placebos (technique à double insu où malades et médecins ignorent quel est le médicament et quel est le placebo) et la méthode des échelles d’appréciation (rating scales) qui fournit des profils psychologiques que l’on peut comparer, grouper en profils moyens d’une catégorie de malades, et étudier avant et après la drogue à tester. Les principales échelles utilisées sont celles de Lorr, de Wittenborn, de Fergus-Falls, d’Hamilton, etc.
Cependant l’observation clinique demeure une méthode irremplaçable pour l’appréciation des effets d’un médicament mais elle comporte de nombreuses causes d’erreurs dues notamment au coefficient personnel et aux différences de nosographies utilisées par les auteurs. Cliniquement, à l’heure actuelle, le moyen de définir la puissance d’un neuroleptique et son seuil d’action sur l’homme est essentiellement un critère neurologique, l’appréciation des modifications extra-pyramidales. Mais le pouvoir neuroleptique en neurologie est-il superposable à l’effet en psychiatrie?
On voit combien il est difficile d’analyser l’effet d’un médicament — et cela explique l’impossibilité pratique d’une concordance des résultats — puisqu’il s’agit finalement de l’analyse des stades de la relation du malade avec le milieu avant, pendant et après une interposition médicamenteuse. Cette analyse dépendra donc du milieu (avant et après la sortie de l’hôpital, par exemple), de l’observateur, de la nosographie de cet observateur, des critères de guérison qu’il utilise (disparition des symptômes principaux, des symptômes-cibles, remaniement de la structure de la psychose, adaptation sociale, etc.), de même également, de la nosographie et des critères de guérison de celui à qui est destinée l’observation.
Il ne nous semble pas inutile de commencer ce chapitre de pharmacologie en rappelant quelques notions préliminaires.
1° Pour tout médicament il faut connaître et apprécier les effets indésirables, la posologie excessive pour le sujet traité, les contre-indications, l’absence d’indications ou que le médicament n’est plus indiqué.
Ces recommandations constituent l’objet de la pharmacovigilance.
2° Connaître le devenir du médicament : de son absorption à son élimination, c’est l’objet de la pharmacocinétique dont les paramètres pratiques sont l’appré ciation de la posologie unique ou multiple, la durée du traitement, le temps de résorption du médicament, tant plasmatique, apprécié par la demi-vie du médi cament ou temps nécessaire pour que sa concentration plasmatique maximal diminue de moitié dont on peut déduire L’accumulation dans l’organisme et son élimination, ainsi que ses métabolites actifs, état du foie et des reins, âge du malade.
3° La surveillance constante du malade et des effets du médicament,l’adapta tion à l’organisme du sujet généralement en commençant par une posologie croissante et terminant par des doses décroissantes (pharmacodynamique du médicament).
Nous n’envisagerons que les médicaments neurotropes ou psychotropes ayant une action modificatrice sur le fonctionnement du système nerveux de la vie de relation ou de la vie végétative (1). On sait par ailleurs combien il est malaisé — sinon impossible — de faire une classification de ces médica ments; aussi nous les classerons en vue de la pratique psychiatrique par groupes d’indications thérapeutiques les plus homogènes possible, ce qui nous impose une première grande division, qui, on le sait, n’est pas absolue, en médicaments neuro-dépresseurs et en médicaments neuro-excitants ou anti dépresseurs.
A — LES NEURO- ET PSYCHO-DÉPRESSEURS
N’ayant donc en vue qu’une classification pratique des médicaments dépresseurs du système nerveux central, nous les répartirons en : a) sédatifs classiques morphiniques et végétaux, b) alcaloïdes antispasmodiques, c) antiparkisoniens,
(1) Nous donnons en minuscules et en italiques la dénomination commune des médi caments et nous donnons également en italiques, suivi d’un astérisque le nom déposé des spécialités. Bien entendu, nous avons tenté d’être en ce domaine très objectifs et nous ne nous portons pas garants de l’efficacité de certains produits cités. On ne saurait non plus interpréter comme un conseil d’abstention les omissions qui pourraient nous être reprochées.
d) hypnotiques, e) anticonvulsivants, f) curarisants et trois groupes qui ont entièrement renouvelé la chimiothérapie des maladies mentales, g) les neuro leptiques, h) les tranquillisants, i) les antidépresseurs.
I LES SÉDATIFS TRADITIONNELS DE L’ANGOISSE ET LES ANALGÉSIQUES DE LA DOULEUR MORALE
Tous les dépresseurs peuvent être donnés à « dose sédative ». Aussi ne ferons-nous que citer ici les sédatifs classiques de l’angoisse et de la douleur morale. C’est ainsi que le plus ancien et le plus puissant, Xopium, n’est plus utilisé qu’exceptionnellement en psychiatrie, ainsi que ses dérivés ou substituts. La péthidine (Dolosal* ) trouve son emploi dans certains « cocktails », mélanges utilisés en perfusion veineuse dans certains états de panique anxieuse (cf. p. 153).
Des médicaments sédatifs mineurs, moins utilisés maintenant, phytothérapiques pour la plupart (simples ou alcaloïdes), peuvent éviter les surcharges de médicaments chimiques, ou favoriser une action psychothérapique. Ce sont l’extrait fluide d’aubépine ou Cratœgus oxyacantha (4 fois XX gouttes), l’extrait de jusquiame (5 à 10 cg), etc. Ces médicaments se prescrivent en association, soit entre eux, soit avec des barbituriques. Ces mélanges font l’objet de nom breuses formules spécialisées.
Enfin il peut être utile parfois de ne pas oublier les vertus sédatives et analgésiques banales de l’aspirine.
II — LES ALCALOÏDES ANTISPASMODIQUES
Ces médicaments anticholinergiques, fort divers par ailleurs, ont seulement la commune propriété de faire cesser ou d’empêcher l’état de contracture qui peut se manifester au niveau des fibres lisses des divers organes.
Les alcaloïdes des solanées occupent une place spéciale parmi les médicaments de ce groupe.
L’atropine, alcaloïde de la belladone, est le plus classique des anti-spasmo diques et le modèle naturel dont la structure chimique a inspiré les chimistes dans leur découverte de nombreux produits synthétiques ultérieurs. L’atro pine est le paralysant type du parasympathique en s’opposant aux effets de tiques. l’acétylcholine sur les effecteurs parasympathiques. On utilise le sulfate d’atro pine à la dose de 1/4 à 1/2 mg en injections hypodermiques ou intraveineuses et aussi à la dose de 1 mg par la voie digestive.
L’hyoscyamine (sulfate, chlorhydrate ou bromhydrate), alcaloïde de la jus quiame, s’emploie de la même façon mais à dose moitié moindre que l’atropine.
La scopolamine (ou hyoscine), alcaloïde de diverses solanées, a les pro priétés parasympatholytiques de l’atropine, mais en plus une action sédative centrale, utilisée depuis longtemps en psychiatrie (Magnan, 1889). Le brom hydrate de scopolamine se prescrit le plus souvent à la dose de 1/4 à 1/2 mg par voie sous-cutanée, fréquemment en association avec d’autres dépresseurs comme nous l’avons vu.
A côté des alcaloïdes des solanées, il faut citer un spasmolytique qui agit directement sur la fibre musculaire, la papavérine, alcaloïde de l’opium, qui se prescrit sous forme de chlorhydrate de papavérine à la dose de 0,03 à 0,05 g en injections intramusculaires.
III — LES ANTIPARKINSONIENS
Les alcaloïdes des solanées que nous venons de voir, trouvaient leur indicaclassique dans la maladie de Parkinson. Mais leur action vagolytique, en aux neurolep. étalant sur de nombreux visceres (pupille, cœur, muqueuses, etc.), présentait de graves inconvénients. Pour réduire cet étalement, on s’est efforcé de rechercher des antispasmodiques atropiniques de synthèse ayant des actions plus électives. C’est ainsi que furent mis au point la diéthazine (Diparcol), l’isothiazine (Parsidol), la prométhazine (Phénergan), médicaments qui nous font déboucher sur toute une classe de produits synthétiques : les phénothiazines (D. Bovet, J. Fournel et P. Charpentier, 1945). L’idée d’utiliser ces produits dans la maladie de Parkinson revient à Sigwald (1946).
Bien d’autres antiparkinsoniens, anticholinergiques de synthèse que nous allons énumérer ci-dessous ont été utilisés pour soigner la maladie de Parkinson idiopathique et les syndromes extra-pyramidaux provoqués par les neuro leptiques. Mais aujourd’hui la L.-Dopa s’est imposée pour traiter la maladie de Parkinson, par contre les anticholinergiques de synthèse classiques, agonistes dopaminergiques, gardent tout leur intérêt en psychiatrie dans le syndrome extra-pyramidal provoqué par les neuroleptiques. On peut les diviser en deux groupes. Au préalable rappelons que dans la maladie de Parkinson il s’agit d’un déficit de la dopamine au niveau du locus niger. Par contre, dans les syndromes extra-pyramidaux par neuroleptiques, la sécrétion est normale, mais les récepteurs dopaminergiques striataux sont bloqués.
Les antiparkinsoniens stimulants : le trihexyphénidyle (Ariane*) 1 à 3 com primés de 2 à 5 mg ou l’injection d’une demi ou d’une ampoule de 10 mg en une fois, renouvelable une fois, dans les crises paroxystiques. La préparation galénique du trihéxyphénidyle à effet retard (Parkinane retard* ) est présentée sous forme de gélules de 2 mg et de 5 mg en une prise 10 mg en moyenne chez l’adulte, le matin, l’orphénadrine (Disipal*) 1 comprimé de 50 mg, corri gent l’inhibition psychomotrice et la passivité, ils doivent être prescrits dans la première partie de la journée au cours des repas, le chlorhydrate de bipiridène (Akinéton-retard*) 1 ou 2 comprimés en prise unique le matin, la profénamine (Parsidol*). Certains conseillent d’associer ces antiparkinso niens aux antiparkinsoniens sédatifs.
Les antiparkinsoniens sédatifs : la benzatropine (Cogentine*) 1 à 3 compri més de 2 mg, le bipéridène (Akinophyl*) 1 à 3 comprimés de 2 mg, l’éty benzatropine (Ponalide* ) 1 à 4 comprimés de 5 mg ou 1 ampoule de 5 mg en cas d’accidents d’hyperkinésie paroxystique. Le chlorhydrate de tropatépine (Lepticure* ) 1 à 2 comprimés de 10 mg par jour. Les antiparkinsoniens sédatifs peuvent être prescrits en deux prises matin et soir.
IV. — LES HYPNOTIQUES
Si un hypnotique est un médicament qui est capable de provoquer un sommeil comparable au sommeil physiologique, on ne connaît pas un produit qui réponde à cette définition (J.-R. Boissier, 1976). Donc plus modestement les hypnotiques sont des médicaments destinés à réduire les différentes formes d’insomnie et devraient être utilisés d’une manière beaucoup plus modérée qu’ils le sont bien souvent.
Il est bien malaisé de classer actuellement les produits utilisés pour leur action hypnogène. Il nous paraît seulement commode, sans plus, de les répartir, en clinique psychiatrique, en deux groupes principaux : les barbituriques et les non-barbituriques.
En fait nous verrons qu’il faut citer, en plus de ces deux groupes, bien des médicaments non hypnotiques à proprement parler : des tranquillisants, des neuroleptiques, etc. que l’on prescrit souvent en association avec les précé dents pour leurs effets inducteurs du sommeil, « potentialisateurs » des hypnotiques ou de relaxation musculaire.
1° Nous rappellerons d’abord, pour mémoire, les hypnotiques anciens pour la plupart aussi sédatifs qu’hypnotiques et de moins en moins prescrits :
a) Les sels de calcium. — L’ion calcium diminue l’excitabilité du système nerveux central, et aussi l’excitabilité neuro-musculaire. Les sels de calcium (chlorure, lactate, gluconate) sont encore associés au brome. — b) Le classi que bromure de potassium. On utilise encore, surtout en neuro-psychiatrie infantile, le bromure de calcium. — c) L’hydrate de chloral. — d) Le chloralose. — e) La par aldéhyde.
2° Les barbituriques forment un groupe très vaste de produits, dérivés de la malonylurée, qui se différencient les uns des autres, comme tous les psycho tropes, par la vitesse de résorption (temps au bout duquel est atteinte la concen tration plasmatique maximale) et leur demi-vie d’élimination (temps nécessaire pour que la concentration plasmatique du médicament diminue de moitié). Ils ne représentent plus le traitement de première intention de l’insomnie maintenant dévolu aux benzodiazépines. On reproche aux barbituriques le ris que de toxicomanie lors d’une administration au long cours et à dose trop élevée. On a pratiquement abandonné, sauf pour l’épilepsie, les barbituriques à action longue (phénobarbital) mais on emploie encore contre l’insomnie des barbituriques à action intermédiaire ou brève qui ont une action rapide (15 à 20 minutes) et brève (3 à 4 heures en moyenne) : sécobarbital (Imménoctal*) indiqué dans les endormissements longs à venir ou les réveils prolongés de la nuit, et qui, associe à l’amobarbital donne le Binoctal*, dont l’action se prolonge 8 heures en moyenne. En cas de tentative de suicide ces derniers barbituriques sont très dangereux par le risque d’une apnée brusque ou dépres sion respiratoire avant les signes propres d’intoxication. En conclusion les barbituriques ont une faible marge de sécurité par rapport aux benzodiazépines.
3° Les hypnotiques non barbituriques. — Il faut distinguer dans ces hypnogènes les hypnotiques de synthèse non barbituriques, s’adressant à l’insomnie simple, et surtout le vaste groupe de benzodiazépines.
Les hypnotiques non barbituriques simples. — Nous citerons seulement l’hexapropymate (Mérinax*), la méthaqualone (Mandrax*), inscrite à la section II du tableau B des substances vénéneuses par l’arrêté du 19 avril 1974, ne peut être prescrite pour une durée de traitement dépassant soixante jours.
Les benzodiazépines. — D’une manière générale les benzodiazépines ont une action anxiolytique, action qui peut être indiquée dans les insomnies anxieuses. Mais d’autres molécules de cette famille sont plus particulièrement retenues par leur action hypnotique. Il est bien difficile de les classer d’après leur effet sur l’insomnie. En thérapeutique des essais sont souvent à faire pour trouver le benzodiazépine efficace. Nous allons citer parmi elles les plus utilisées comme hypnotiques : le nitrozépam (Mogadon*), comprimés de 5 et 2 mg, 2,5 mg à 10 mg/jour, l’oxazépam (Séresta*), comp. 50 et 10 mg, 25 à 50 mg/ jour, le flunitrazépam (Rohypnol* ), comp. 1 et 2 mg, 1 à 3 mg/jour, le lorazépam (Témesta*), comp. 1 et 2,5 mg, 1 à 5 mg/jour, le triazolam (Halcion*), comp. 0,5 et 0,25 mg, 0,25 à 0,50 mg/jour, le clorazépate dipotassique (Tranxène*, Noctran*), 1 comp. 10 mg avant le coucher, le loprazolam (Havlane*), 1 comp. de 1 mg au coucher. Bien d’autres benzodiazépines peuvent être utili sées pour leurs vertus anxiolytiques et hypnotiques.
Par contre, des précautions d’emploi sont indispensables à respecter. La myasthénie est une contre-indication, l’hypersensibilité aux benzodiazépines connue est évidemment une contre-indication. Dans l’éventualité d’une insuffi sance hépatique, rénale ou respiratoire, bien surveiller les doses. On doit retenir que toute benzodiazépine entraîne une réduction de la vigilance et de la mémoire dans les heures qui suivent l’absorption. Enfin, après traitement, l’arrêt des doses doit être progressif.
4° Propriétés hypnogènes et des neuroleptiques. — Les neuroleptiques que nous étudierons longuement, dans un autre chapitre, sans être théoriquement hypnotiques, doivent être cités ici car ils sont souvent associés aux hypnotiques barbituriques ou non barbituriques, qu’ils « potentialisent ».
Les neuroleptiques dits « sédatifs » ont une action hypnotique certaine, notamment l’alimémazine (Théralène*), l’acépromazine (Plégicil*, Mépronizine* (association)), la lévomépromazine (Nozinan*), la prométhazine (Phénergan*).
Enfin paradoxalement les antidépresseurs, bien que psycho-analeptiques, peuvent avoir une action hypnogène en traitant la dépression génératrice d’insomnie. Cette remarque nous amène, si cela était nécessaire, à ne pas oublier que l’insomnie n’est qu’un symptôme dont il importe toujours de chercher la cause (cf. P. Pichot et M. Serdan : Psychopathologie du sommeil, Encéphale, 1972, 350-457).
V — LES ANTICOMITIAUX
Nous nous limiterons ici à l’énumération des principaux anticonvulsivants.
Des indications plus précises ont été fournies au chapitre de l’épilepsie.
Les quatre groupes principaux d anti-epileptiques ont tous en commun une grande partie de leur formule de constitution ainsi qu’il apparaît au premier coup d’œil jeté sur leur formule développée; ce sont les barbituriques, les hydantoïnes, les oxazolidines-diones et la phénacétylurée.
Depuis quelques années, d’autres anti-épileptiques ont été introduits : la Mysoline*, la Posédrine*, le Lifène*, le Glior*, LÉliptène*, le Tégrétol*, Dépakine*, LÉlisal*, le Zarontin*, le Rivotril*, etc. Nouvel antiépileptique : le progabide (Gabrène*), comp. sécables 600 et 300 mg, sachets 150 mg.
VI — CURARISANTS ET INFRACURARISANTS
L’idée d’employer les propriétés paralysantes du curare en psychiatrie revient à Bennet (1940) qui l’utilisa le premier aux U. S. A. dans la préven tion des accidents de la convulsivothérapie. Mais la découverte de nombreux curarisants de synthèse a permis non seulement de perfectionner la curarisation pour électrochocs mais encore d’utiliser ces drogues aux doses infraliminaires afin d’obtenir des effets « relaxants » comme complément de certains traitements : cures de sommeil, cures de relaxation, traitement sédatif des névroses, etc.
On sait que les curarisants agissent à la jonction neuro-musculaire en arrêtant la transmission de l’influx nerveux (Cl. Bernard, 1857). Il existe cependant des pseudo-curarisants, notamment le crésoxydiol (ou Décontractyl *) qui exercent leurs effets sur les centres médullaires et cérébraux.
Les curares vrais agissant sur la jonction myo-neurale se divisent en deux groupes pharmacologiques, correspondant grossièrement à deux groupes d’indications psychiatriques, les pachycurares et les leptocurares.
Les pachycurares agissent par inhibition de l’acétylcholine au niveau de la jonction myo-neurale. Ils comprennent soit des curares naturels (d-tubo- Pachycurares. curarine ou Intocostrine T*, bébéerine ou Auxopéran*, etc.), soit des cura risants synthétiques (gallamine ou Flaxédil *, Isocurine *, etc.).
Les leptocurares bloquent la jonction myo-neurale par une accumulation Leptocurares. très fugace de l’acétylcholine. Ils sont donc particulièrement indiqués dans les brèves curarisations pour électrochocs mais par contre ils sont sans intérêt pour les cures de relaxation. Les principaux sont le décaméthonium, les dérivés de la succinylcholine (Célocurine *, etc., le Brévatonal*, etc.).
L’action physiologique recherchée, curarisation ou infracurarisation, dépend non seulement de la constitution chimique du curarisant mais tout Préparation à autant de son mode d’administration. Ainsi pour la curarisation de la convulla convulsivoithérapie dont nous reparlerons à propos de cette technique, on utilise exclusivement la voie intraveineuse et les leptocurares. Par contre, pour les infracurarisations on utilise la voie digestive (dragées ou suppositoires) : le crésoxydiol (Décontractyl*, 4 à 8 dragées de 0,25 g par jour). Les infracura risations endorectales (Delay, Thuillier et de Montrémy, 1952) se pratiquent avec un à quatre suppositoires d’Isocurine de 1 g ou 4 à 6 suppositoires d’Auxopéran* à 30 mg.
VII — LES NEUROLEPTIQUES
L’introduction de ces médicaments, vers 1952, a complètement renouvelé la thérapeutique biologique en psychiatrie. Avant l’ère des neuroleptiques, on peut dire (Kalinowski et Hoch, 1961) que la chimiothérapie en psychiatrie n’allait guère au-delà d’une « contrainte chimique » provoquée par les diffé rents sédatifs et calmants que nous avons rappelés plus haut, tandis que les médicaments actuels, neuroleptiques et antidépresseurs, bien que n’ayant pas encore une action directe sur les facteurs étiologiques et patho-physiologiques, ont une action suspensive, et parfois élective, sur les symptômes. Dans les psychoses aiguës il n’est probablement pas excessif de penser qu’elles ont une action curative. Quoi qu’il en soit l’évolution des psychoses semble dorénavant modifiée dans leur organisation structurale et l’on cons tate dès à présent une transformation de l’évolution et de la sémiologie des psychoses chroniques.
Cette ère psycho-pharmacothérapique a été ouverte par la synthèse de la chlorpromazine en France par P. Charpentier, en 1950. Cette drogue fut considérée d’abord, selon les travaux de Laborit sur l’hibernation, comme un neuroleptique potentialisateur des hypnotiques et utilisée dans des techniques inspirées de l’hibernothérapie (Hamon, Paraire et Veluze, 1952; Mlle Des champs, 1952; Brisset, 1952; Henri Ey et Bérard, 1952). Cependant Delay, Deniker, Harl, Grasset, 1952, puis de nombreux auteurs ensuite ont montré le parti qu’on pouvait tirer de ce seul médicament (cf. J. Delay et Deniker, 1961 ; Anne A. Caldwell : Origins of Psychopharmacology from CPZ to LSD. Ch. C. Thomas, Springfield, 1970).
La même année (1952) un autre neuroleptique, la réserpine, chimiquement totalement différent, était isolé de la racine de Rauwolfia par Muller, Schlittler et Bein à Bâle.
Depuis lors, d’innombrables neuroleptiques ont été proposés soit, les plus nombreux, appartenant à la série de la chlorpromazine (les phénothiazines) soit à la série réserpinique, soit à la série des butyrophénones dont le type est l’halopéridol, soit enfin à de nouveaux groupes, tels que celui des dibenzothiazèpines (Etumine*), les thioxanthènes (Taractan *), les anisamides substi tués (Dogmatil*). On convient d’appeler les plus efficaces d’entre eux neuro leptiques majeurs sans que pour autant tous les auteurs soient entièrement d’accord sur la liste de ces neuroleptiques majeurs. D’ailleurs toute liste de ces médicaments ne peut-elle être que provisoire et constamment revisible. Nous ne ferons état que de celles d’entre elles qui, commercialisées en France, ont donné satisfaction à une majorité d’expérimentateurs.
L’individualisation du groupe des neuroleptiques parmi les autres neurodépresseurs, notamment celui des hypnotiques et celui des tranquillisants, a été proposée par Delay et Deniker (1957) par la réunion des cinq critères suivants :
1. Action psycholeptique (c’est-à-dire à effets cliniques sédatifs) sans action hypnotique.
2. Action inhibitrice à l’égard de l’excitation, de l’agitation, de l’agressivité, réduc tion des états maniaques.
3. Action réductrice vis-à-vis de certaines psychoses aiguës et chroniques et vis-à- vis des psychoses expérimentales.
4. Importance des manifestations psychomotrices neurologiques et neurovégé tatives.
Delay et Deniker insistent sur les effets neurologiques particuliers qui non seulement distinguent les neuroleptiques de l’ensemble des psycholeptiques mais dont l’importance pour ces auteurs ainsi que pour Flugel et Goldmann est proportionnelle à leur activité thérapeutique. Ce syndrome neurologique est fait de plusieurs éléments : a) des modifications neuro-végétatives portant sur les régulations cardio-vasculaires, thermiques, pondérales, etc.; b) une inhibition psycho-motrice avec diminution de l’initiative, l’allongement du temps de réaction, un ralentissement du cours de la pensée, une indifférence affective, un ralentissement moteur et une réduction de la mimique; c) plus rarement des modifications du tonus : hypertonie parkinsonienne, état catalep tique et hypotonie musculaire; d) plus rarement encore des mouvements anormaux principalement tremblement, myoclonies, crises d’allure hystéroïde, akathisie (impossibilité de rester assis), tasikinésie (tendance aux mouve ments), etc. Tous ces effets secondaires des neuroleptiques font admettre que leur action s’exerce en grande partie par l’intermédiaire des centres souscorticaux.
Les neuroleptiques peuvent être employés selon des méthodes diverses que l’on peut grouper selon deux types : I° ils peuvent être utilisés pour leurs propriétés seules, sans recherche notamment d’effets hypnotiques, c’est la cure neuroleptique simple, la plus employée; 2° le repos obtenu par les neuro leptiques peut être complété en recherchant un effet de sommeil, ce sont les cures de sommeil.
Mais les effets thérapeutiques recherchés des neuroleptiques peuvent se résumer en trois actions principales, pas forcément homogènes :
uneaction sédative, la première recherchée et qui nous a fait situer ce groupe dans les psycho-dépresseurs. Les neuroleptiques constituent la meil leure arme contre l’agitation ;
une action désinhibitrice ou psychostimulante, plus spécialement manifeste avec certains neuroleptiques tels que la prochlorpérazine (Témentil *), la thiopropérazine (Majeptil *), etc., qui provoque une stimulation psychique et parfois des crises excito-motrices mais aux doses thérapeutiques « désinhibe » les schizophrènes passifs, apathiques, athymhormiques et autistiques ; rappelons que le terme « désinhibiteur » est classiquement réservé dans la littérature psy chiatrique francophone à certains neuroleptiques qui s’opposent à l’inertie, à l’indifférence apparente et à la perte de l’initiative psychomotrice de l’hébéphrénie.
une action anti-psychotique, c’est l’action suspensive, dont nous avons déjà parlé, et qui porte surtout sur les expériences délirantes et hallucinatoires et moins efficacement sur l’activité délirante et hallucinatoire noético-affective (d’où les réserves de M. Bleuler, 1972).
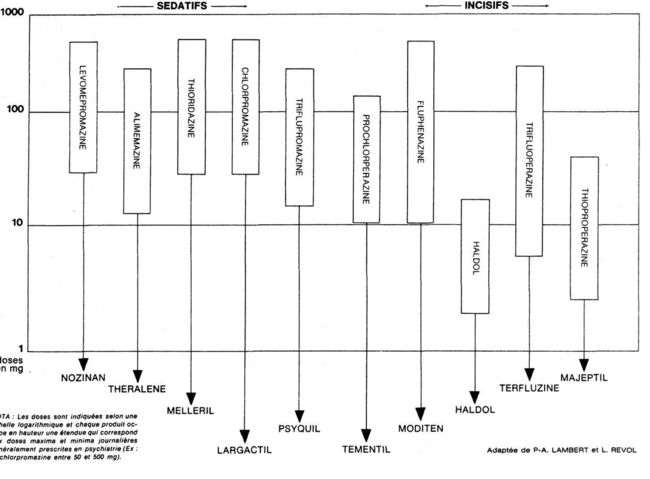
Chacune de ces actions thérapeutiques prévaut chez chacun des neuro leptiques et permet ainsi leur classification. C’est ainsi que P.-A. Lambert et L. Revol (v. tableau XXVI) ont classé les principaux neuroleptiques de gauche à droite en fonction de leurs propriétés sédatives et suspensives sur les troubles mentaux, du plus sédatif situé à l’extrême gauche (Nozinan*) au plus « incisif », c’est-à-dire au plus puissant anti-psychotique, situé à l’extrême droite (Majeptil*), le largactil occupant une position médiane.
Enfin l’emploi des neuroleptiques constitue un sujet-clef de la psychiatrie d’aujourd’hui. En effet si le médecin vise à atteindre, le plus électivement possible certains symptômes ou syndrome gênants tels que l’agitation, l’agressivité, l’anxiété, l’autisme, l’apragmatisme, le délire, les hallucinations, etc. (1), qu on appelle aussi symptômesou syndromes-cibles, il faut bien savoir que le médicament neuroleptique modifie, en fait et à la fois, le comportement dans son ensemble, le champ de la conscience et la communi cation du malade avec son environnement social. Autrement dit nous modi fions, aussi et ainsi, toute la façon « d’être au monde » du malade. En atteignant ses symptômes morbides et indésirables nous atteignons également sa personnalité tout entière, de sorte que nous modifions son humeur, nous réduisons son efficience intellectuelle, son activité psycho-motrice, sa puis sance sexuelle, etc. Mais de plus — et cela est essentiel — nous le privons du seul compromis qu’il avait imaginé — et qui rendait son existence vivable — entre ses pulsions libérées et la réalité sociale qui l’entoure. C’est-à-dire que nous le privons des symptômes auxquels il tient de toutes ses forces et qui, du même coup, sont devenus nos cibles sur lesquelles nous tirons avec non moins de force, à coup de neuroleptiques. Dans ces conditions, nous devons nous demander ce qu’il advient du malade dépossédé de son délire et inévi tablement saisi par un « manque » qui se traduit bien souvent par une dépression plus ou moins accusée. C’est ainsi, que les traitements neuroleptiques généralisés et au long cours ont créé une nouvelle sémiologie des affections mentales chroniques. Le schizophrène d’aujourd’hui ne se présente pas sous les mêmes traits cliniques que ceux du schizophrène d’hier. Donc il faut penser à ce que devient le malade privé de ses symptômes ou d’une partie de ceux-ci après neuroleptisation. Sans doute le malade peut y trouver un confort et, bien entendu l’entourage aussi. On a même reproché à celui-ci (Laing, etc.) c’està-dire aux soignants et à la famille, d’être les premiers et les uniques bénéficiaires du traitement tandis que le malade devenait un objet passif et soumis, châtré en quelque sorte, et régressé au stade de nourrisson entre les mains de son entourage (infirmiers, parents, la mère en particulier). Aussi dépend-il des soignants qu’il n’en soit, bien entendu, pas ainsi et que ne s’instaure pas, à l’abri des neuroleptiques, un mode de relation détérioré, « tranquillisé et tran quillisant ».
(1) Cf. H. Ey : Traité des Hallucinations, 1973, p. 1362, 1364, p. 1392-1405 et p. 1408.
L’emploi des neuroleptiques ne permet donc jamais de négliger la relation psychothérapique qui doit accompagner toute thérapeutique biologique en psychiatrie. Nous venons de voir que les neuroleptiques réduisent les symp tômes les plus gênants des psychoses et contribuent par-là même à rendre le malade plus coopérant et apte à profiter des techniques de psychothérapie individuelle ou collective. Même dans les cas les moins favorables de psy choses chroniques où l’on ne saurait prétendre à une guérison, mais seule ment à une action suspensive du médicament sur les symptômes, il devient indispensable de placer le malade, maintenu sous les doses d’entretien conve nables, dans des conditions aussi normales et normalisantes que possible, c’est-à-dire dans des conditions qui lui permettent de rétablir des relations et des communications avec autrui au sein d’un groupe thérapeutique d’abord et de son groupe social et familial ensuite. On peut ainsi assister à des sorties de malades qui autrefois seraient demeurés internés de nombreuses années et les voir se maintenir dans leur milieu à la condition d’être soumis à un traitement régulier et à une surveillance médicale et psychothérapique attentive.
Bien plus, le recours aux cures ambulatoires sans hospitalisation ou avec une hospitalisation de courte durée ou une hospitalisation à temps partiel, tend, avec les thérapeutiques neuroleptiques, à devenir presque courante.
Ces traitements ambulatoires ont contribué à réduire dans une grande proportion la population des malades hospitalisés, parfois d’ailleurs, il faut le reconnaître, par simple fragmentation de l’évolution des psychoses chroniques, le malade ne faisant que de courts séjours à l’hôpital psychiatrique à l’occa sion de brèves rechutes mais demeurant la plus grande partie de son existence dans le milieu social. Ces malades doivent donc être suivis avec beaucoup de soins par les consultations externes ou par les visites à domicile. La coopéra tion du milieu familial — qui s’obtient par une information précise sur les possibilités du traitement et parfois par une psychothérapie de la famille ellemême — est indispensable.
Comme nous l’avons annoncé plus haut nous allons maintenant envisager successivement : les phénothiazines, les thioxanthènes, les dibenzothiazépines, la réserpine et les réserpiniques, les butyrophénones.
Les phénothiazines. — La chlorpromazine (Largactil *) est le premier neuroleptique synthétisé et l’un des plus employés encore actuellement. Nous avons déjà rencontré ses indications et sa posologie dans les psychoses aiguës, les états maniaques, la confusion mentale, les bouffées délirantes, dans les psychoses alcooliques aiguës, notamment dans la crise de delirium tremens, dans les états schizophréniques et les psychoses chroniques délirantes inter prétatives et hallucinatoires. Son action est véritablement curative dans les psychoses aiguës, mais dans les psychoses chroniques (plus de deux ans d’évolution) il est prudent de n’espérer qu’une action suspensive sur les symptômes et de considérer le malade en rémission seulement, même si la réadaptation sociale paraît normale. Parfois des résultats spectaculaires et inespérés ont pu être enregistrés.
Voici à titre indicatif quelques résultats statistiques publiés par Delay et Deniker (1961) concernant les rémissions complètes ou les « améliorations de premier ordre » : manies 78,5 %, confusions mentales 67 %, bouffées délirantes 50 %, schizophrénies (résultats d’ensemble) 30 %, psychoses chroniques hallucinatoires 53 %, interprétatives 39 % (cf. à ce sujet les réserves de M. Bleuler, 1972 et H. Ey, 1973).
La posologie est strictement individuelle. Le traitement se fait habituellement par voie buccale (comprimés de 0,025 g ou 0,100 g et gouttes dosées à 0,001 par goutte). Les injections intramusculaires (ampoules de 0,025 g) ou les perfusions (ampoules de 0,050 g) ne s’emploient qu’en cas d’urgence ou chez des malades non coopérants. Les doses quotidiennes moyennes par la bouche (à noter que le produit est quatre fois plus actif en injection intra-musculaire) s’étalent habituellement entre 150 et 500 mg (au-delà de cette accidents dose, il semble que le cerveau donne des signes de souffrance à l’E. E. G.).
La lévomépromazine (Nozinan *) a une action puissante vis-à-vis de l’anxiété et de l’agitation psychotiques (J. Sigwald et M. Henne, 1954 ; Des champs, 1957, etc.). Dans les états dépressifs elle est généralement associée aux thymoanaleptiques dont elle corrige les effets secondaires (anxiété et insomnie). Elle est prescrite aux doses de 100 à 500 mg. Dans les états névrotiques, les dysthymies, la turbulence sénile, etc., elle est prescrite à des doses plus réduites et progressives de 3 comp. à 2 mg à 3 comp. à 25 mg. Son action asthéniante et aussi hypotensive associée à la tachycardie doit inciter à la prudence dans sa prescription chez les vieillards et les athéromateux.
La cyamémazine (Tercian*) de formule proche de la lévomépromazine en a les indications. Elle est le type des neuroleptiques sédatifs (Lam bert, 1970) et se caractérise de plus par ses actions anxiolytique et anti-dépressive. Elle se prescrit en gélules de 25 mg ou en comprimés sécables de 100 mg ou en gouttes de 1 mg aux doses progressives de 50 à 500 mg chez l’adulte et de 25 à 100 mg chez le vieillard en deux prises ; les ampoules injectables de 50 mg sont réservées aux états anxieux aigus.
La prochlorpémazine (Témentil*). — Cette phénothiazine a d’abord été utilisée pour ses propriétés anti-émétiques mais ses indications psychiatriques signalées d’abord par Broussolle et Dubor (1956) sont les schizophrénies plus particulièrement à forme catatonique et les états d’excitation psychomotrice. Elle est utilisée aux doses moyennes de 50 à 200 mg. Elle peut provoquer un syndrome hyperkinétique ou excito-moteur, tremblements, myoclonie, crises de torticolis, trismus, manifestations choréo-athétosiques ou hystériformes.
La thiopropérazine (Majeptil *) est caractérisée par l’intensité des troubles neurologiques secondaires qui surviennent rapidement et dans l’ordre suivant (Delay et Deniker) : 1) syndrome d’akinésie sans hypertonie souvent dès les premières heures, 2) à partir de la quarante-huitième heure possibilité de crises excito-motrices à localisation cervico-linguo-masticatrice (protractions linguales, trismus, torticolis spasmodiques) mais aussi généralisées (crises d’opisthotonos), 3) au cours de la deuxième semaine une imprégnation médi camenteuse plus importante (50 à 70 mg) engendre un syndrome akinétohypertonique rappelant les formes sévères de parkinsonisme post-encéphalitique. Sur le fond d’hypertonie peut survenir un besoin impulsif de mouvement avec impossibilité de rester immobile. Les phénomènes végétatifs (sudation, sialorrhée, séborrhée) sont importants. L’état psychique passe de l’indif férence à l’hébétude et à la stupeur. Ces crises dyskinétiques aiguës cèdent sous l’influence d’un antiparkinsonien administré soit en injection intra musculaire (1 ou 2 ampoules de 5 mg de Ponalide *) soit per os (2 ou 3 com primés d’Ariane à 5 mg).
Ce médicament paraît particulièrement indiqué dans les divers états d’exci tation notamment maniaques et dans les psychoses aiguës agitées (bouffées délirantes et confusionnelles). Dans les psychoses schizophréniques la supé riorité de la thiopropérazine sur les autres neuroleptiques se manifesterait dans les formes hébéphréniques et catatoniques.
Les doses moyennes peuvent progressivement atteindre 50 à 70 mg en com mençant par 5 à 10 mg. Delay, Deniker, Coirault, P. Broussole et P.A. Lambert, proposent une technique d’administration discontinue avec interruption brusque au bout de 5 à 8 jours et reprise de la cure après disparition du syndrome neuro logique. Les doses d’entretien ne doivent pas dépasser quelques milligrammes par jour. L’activité du médicament commande toujours un examen médical préalable attentif et une surveillance constante tout au long du traitement notamment en prévision d’accidents graves (syndrome pâleur-hyperthermie, dyspnée asphyxique, etc.) annoncés par l’hyperthermie en plateau. Il est prudent d’éviter au cours des traitements par la thiopropérazine l’emploi de médica ments doués d’un effet dépresseur sur les centres respiratoires et notamment des barbituriques.
Il faut enfin savoir qu’on peut observer, chez les sujets âgés en particulier, des troubles dyskinétiques chroniques : mâchonnements, mouvements divers des lèvres, de la langue, dandinement sur place, impossibilité de rester assis (akathisie), besoin impérieux de marcher (tasikinésie), mouvements divers qui sont insensibles à l’action des parkinsoniens et qui ne régressent que lente ment après l’arrêt du traitement.
Le dichlorhydrate de fluphénazine (Moditen *) a été expérimenté d’abord aux U. S. A. (Darling, 1959), c’est une phénothiazine, classée dans les neuroleptiques majeurs et incisifs, qui est présentée sous plusieurs sels. Le dichlorhydrate de fluphénazine constitue la présentation orale habituelle. Elle a ses indications dans toutes les formes de psychoses chroniques, les schizo phrénies, les délires chroniques et secondairement dans les troubles du com portement ou du caractère des oligophrènes. La dose quotidienne efficace varie de 25 à 400 mg par jour, parfois plus.
La trifluopérazine (Terfluzine *) a été expérimentée depuis 1958 en Amé rique du Nord où elle a provoqué des observations enthousiastes. Les pre miers résultats obtenus par Delay et Deniker (1961) sont plus modestes. L’activité du produit serait particulièrement évidente dans les psychoses chro niques réfractaires aux autres neuroleptiques, notamment les schizophrènes où dominent autisme et apragmatisme (Barsa et coll., 1959). Il aurait égale ment une activité anti-hallucinatoire certaine (Kruse, 1959). Broussolle et coll. (Presse méd., 1962) confirment partiellement les résultats obtenus par les Américains. Elle s’administre aux doses progressivement croissantes de 5 à 60 mg par jour. La dose moyenne est de 30 mg. Sa tolérance est généralement bonne.
La perphénazine (Trilifan*) synthétisée en 1956 aux U. S. A. et expérimentée pour la première fois par Ayd (1957) dans l’anxiété et l’agitation sénile, par Cahn et Lehmann (1957). Aux doses moyennes de 3 comprimés de 4 mg par jour ou de 16 mg (jusqu’à 4 dragées par jour dans les psychoses chroniques) dans les psychoses aiguës agitées et aussi dans les psychoses chroniques, elle a donné des résultats assez semblables à la prochlorpémazine (Delay et Deniker) dont elle est d’ailleurs chimiquement assez proche.
La thioridazine (Melleril*) est une phénothiazine qui a d’abord été pro posée comme tranquillisant aux doses de 1 à 2 dragées de 10 mg, 3 fois par jour. A ce faible dosage elle a en effet une action anxiolytique évidente et constante dans les états névrotiques, d’hyperémotivité et psychosomatiques. Mais aux doses de 200 à 500 mg, ou plus elle a parfois les effets des neuro leptiques majeurs par une action anti-psychotique dans les délires chroniques, les schizophrènes, les psychoses séniles. Dans ces psychoses la posologie de la thioridazine est de 1 à 4 dragées de 100 mg par jour. Ce médicament est généralement bien toléré.
La propériciazine (Neuleptil*) dont l’action anti-sérotonine est 4 fois supé rieure à celle de la chlorpromazine est très maniable en raison de l’absence habituelle de syndrome neuroleptique. Ses indications sont les troubles du caractère et du comportement (chez les déséquilibrés, les débiles, les épileptiques, les alcooliques, etc., où elle réduit l’agressivité et l’impulsivité) à la dose de 30 à 60 mg (ou 30 à 60 gouttes) du soluté à 4 % par jour.
Les neuroleptiques à action prolongée. — L’œnanthate de fluphénazine (Moditen-retard *) tout en ayant les mêmes propriétés pharmacologiques et les mêmes indications thérapeutiques que le Moditen * oral (dichlorhydrate) présente l’originalité d’être actif par voie intramusculaire profonde pendant une durée prolongée de 15 à 20 jours en moyenne.
On débute généralement le traitement par la voie orale afin d’établir la dose avec laquelle on obtient une stabilisation de bonne qualité. On passe ensuite aux injections d’œnanthate de fluphénazine (Moditen-retard *) en injec tant toutes les deux semaines la dose quotidienne de fluphénazine orale en évitant de dépasser la dose moyenne de 200 mg.
Il existe toutefois quelques complications à retenir : une asthénie qui survient dans les jours qui suivent l’injection et ultérieurement les tendances dépressives qui peuvent aller jusqu’aux tentatives de suicide. On corrige ces Lesneuroleptiques tendances dépressives par un antidépresseur, par exemple de la clorimipramine (Anafranil *). Enfin les manifestations parkinsoniennes sont réductibles longée.qUOtidienne d’antiparkinsonien.
L’avantage de ce neuroleptique à durée d’action prolongée est évident. Le malade est libéré de la contrainte imposée par la prise pluri-quotidienne de médicaments. Le médecin est assuré que sa prescription a été scrupuleuse ment appliquée. Un autre progrès résulte de la diminution des doses actives pour une même efficacité thérapeutique. Les modalités mêmes de ce traite ment permettent au malade de retourner à son domicile et de reprendre sa vie familiale et même professionnelle supprimant ainsi tous les inconvénients de l’hospitalisation. Néanmoins il serait imprudent que le malade ne soit pas revu par son médecin, ou par le psychiatre, en consultation privée ou au dispensaire, à chaque injection.
Le Moditen-retard *, premier neuroleptique à action prolongée commercia lisé en France, a été suivi par le décanoate de fluphénazine (Modécate*) à effets analogues au Moditen * mais mieux toléré semble-t-il et permettant un espacement un peu plus long des injections.
La pipotiazine (Piportil*) est un neuroleptique phénothiazinique à noyau latéral pipéridiné dont l’effet thérapeutique prévalent est marqué par son action désinhibitrice : levée de l’inhibition psychomotrice, amélioration du contact et de la relation avec le milieu. L’action stimulante du médicament peut « réactualiser », pendant la première phase du traitement, un état d’angoisse ou un état délirant jusque-là moins apparent.
Les principales indications sont donc les psychoses chroniques, schizo phrénies a formes déficitaires ou paranoïdes, les délires chroniques halluci natoires, interprétatifs et passionnels, les psychoses autistiques de l’enfant.
L’action prolongée du Piportil* permet de réduire l’administration du médicament à une prise par jour et même à le suspendre deux jours par semaine (durant le week-end par exemple) à la dose quotidienne de 5 à 20 mg ou même de 20 à 80 mg hebdomadaire en une ou deux prises (comprimés dosés à 10 mg et soluté à 4 % dosé à 1 mg pour 1 goutte). Pour le traitement d’attaque de certains états aigus : 1 ou 2 ampoules I. M. de 10 mg.
L’ester undécylénique de pipotiazine (Piportil M2*) et l’ester palmitique de pipotiazine (Piportil L4*) ont les mêmes indications que la pipotiazine mais sont présentées en solution huileuse injectable en intramusculaire. La dose moyenne par injection est identique pour les deux produits, soit environ 100 mg. Par contre les intervalles entre les injections sont de l’ordre de deux semaines pour le Piportil M2* et de quatre semaines pour le Piportil L4*.
Le penfluridol (Semap*) est un désinhibiteur à effet analeptique sur la thymie qui peut à ce titre provoquer une recrudescence de l’anxiété ou des phénomènes délirants. Il est donc indiqué dans l’apathie, l’athymhormie, l’autisme. Il est prescrit par une prise hebdomadaire de 1 à 3 comprimés.
La perphénazine (Trilifan retard*), soluté injectable de 1 ml, taux plasmatique atteint au maximum de 12 à 3-5 jours, une ampoule I. M. toutes les 2 semaines. Des délais plus élevés peuvent être obtenus avec des doses plus élevées mais celles-ci, comme pour tous psychotropes, doit être adaptée à chaque cas (sensibilité, âge, etc.).
Neuroleptiques qui font la transition avec les tranquillisants. — Nous citerons sous cette rubrique des neuroleptiques dont les effets secon daires sont moindres que ceux des neuroleptiques majeurs. Ils se situent par leur action entre les neuroleptiques et les tranquillisants; à faibles doses ils sont prescrits au même titre que ces derniers.
La prométhazine (Phénergan *) n’a que de faibles propriétés neurosédatives comparées à son action anti-histaminique. Elle est surtout utilisée en psychia trie pour son action centrale hypnogène, analgésique et anti-spasmodique (2 à 6 comprimés de 25 mg par jour) mais souvent aussi en association pour son effet potentialisateur avec d’autres psycholeptiques et en perfusion (une ampoule de 50 mg).
L’alimémazine (Théralène *) a une action hypnogène à faible dose (50 à 100 gouttes de 1 mg par jour) et sédative centrale à doses élevées (300 à 500 gouttes). Il est indiqué dans les états névrotiques avec anxiété et insom nie, dans les affections psycho-somatiques, dans les états dépressifs mais aussi dans les divers états psychotiques. Il est contre-indiqué chez les épileptiques.
La clotiapine (Étumine*) neuroleptique d’action sédative et anxiolytique mar quée dans les états dépressifs anxieux, les états maniaques, les expériences de dépersonnalisation, etc. Les précautions et les contre-indications sont celles des neuroleptiques puissants. La posologie moyenne est de 2 à 3 comprimés de 40 mg par jour.
Les Thioxanthènes. — Lechlorprothixène (Taractan *) a des propriétés sédatives et anxiolytiques utilisées dans les névroses avec excitation en raison du peu de risque d’effets secondaires et aussi dans les psychoses. Les doses utiles varient 30 et 200 mg par jour (15 à 100 gouttes de la solution à 4 %).
Le flupentixol (Emergil * Fluanxol *) ne présente pas non plus les effets secondaires des neuroleptiques aux doses moyennes habituelles (3 comprimés de 0,5 mg). Il est indiqué dans les états anxieux et dépressifs, les affections psychosomatiques où domine l’adynamie. Le décanoate de flupentixol (Fluanxol retard *) est administré en injection I. M. 1 à 6 ampoules de 20 mg toutes les 2 semaines.
La réserpine et les dérivés du Rauwolfia serpentina. — Le Rauwolfia serpentina est un arbuste des Indes. On a pu extraire (G. Sen) de ses racines une vingtaine d’alcaloïdes aux propriétés très diverses. Seuls nous intéressent ici : a) l’alcaloïde le plus complet en vue de l’effet neuroleptique recherché en psychiatrie : la réserpine, b) les extraits totaux du Rauwolfia serpentina.
Les propriétés de la réserpine (Serpasil *) sont analogues à celles des phénothiazines : sédation sans effet narcotique, hypotenseur et bradycardisant ; elle aurait une action centrale et non périphérique ; elle ne produit pas en effet de blocage de la transmission des excitations au niveau des ganglions ou, expérimentalement, des organes isolés. Elle se distingue encore des phénothiazines par son action retardée, d’où la nécessité de traitements prolongés. Enfin la réserpine, comme les autres alcaloïdes de Rauwolfia, n’a aucune parenté chimique avec les phénothiazines (N. Kline, 1954 ; Delay et Deniker, 1954).
Les réserpiniques sont actuellement presque abandonnés en raison de l’in tensité des effets défavorables. En dehors de leurs contre-indications for melles : association avec les électrochocs, les ulcères digestifs, l’épilepsie, leurs effets secondaires sont analogues à ceux des phénothiazines mais plus mas sifs : hypotention artérielle, asthénie, syndromes extra-pyramidaux, augmen tation de poids, retentissement endocrinien. Leur action dépressive et asthéniante les contre-indique dans les états dépressifs. On a signalé (The Lancet, 21 septembre 1974) un accroissement du risque cancérigène au niveau du sein chez les femmes après la ménopause et après un traitement de longue durée.
Les butyrophénones. — L’haloperidol (Haldol*) synthétisé par P. Jans (1956) est le prototype d’un groupe chimique, les butyrophénones, complè tement différent des phénothiazines et des réserpiniques. Les premiers essais cliniques ont été rapportés par Divry, Bobon et Collard (1958). Ce médica ment a rapidement pris une place parmi les neuroleptiques majeurs et donne parfois des résultats spectaculaires. On le considère actuellement comme la médication la plus puissante de l’agitation psychomotrice notamment, des syndromes maniaques. Il a également une action très favorable dans les psychoses aiguës, délirantes, hallucinatoires ou confusionnelles et, d’une manière évidemment moins constante, dans les psychoses chroniques, schizophréniques et hallucinatoires. Comme nous l’avons vu précédemment, l’haloperidol aurait une meilleure action dans les schizophrénies paranoïdes que dans les formes à symptomatologie hébéphrénique.
Sa posologie moyenne est de 1 à 20 mg, soit 10 à 200 gouttes de la solution au deux millième par 24 heures, ou une à deux ampoules intramusculaires de 5 mg. Il faut surveiller les accidents d’intolérance : notamment les troubles akinéto-hypertoniques, les hyperkinésies, les dystonies paroxystiques, les paresthésies, les impatiences diffuses, les crampes. L’hyperthermie avec hypersudation et déshydratation doit faire craindre un syndrome malin secondaire et suspendre le traitement. Il faut noter que l’haloperidol est une médication dépressogène et qu’il est contre-indiqué dans tout syndrome présentant des éléments dépressifs. Pour prévenir cette action dépressive et anxiogène, il est habituel de l’associer à un thymoleptique tel que la lévomépromazine (Nozinan*).
Le triperidol (Triperidol *), de formule voisine de celle de l’haloperidol a une action sédative plus faible que ce dernier. Il a même un effet stimulant sur l’activité de l’humeur aux faibles doses, par suite il n’en a pas non plus les effets dépresseurs, aussi trouve-t-il son indication (P. Pichot, 1963), contrai rement à l’haloperidol, dans les formes hébéphréniques et apragmatiques des psychoses schizophréniques. Sa posologie est de 1 à 5 mg, soit 20 à 100 gouttes. Les effets secondaires sont sensiblement les mêmes que ceux de l’haloperidol. Les deux drogues sont particulièrement maniables du fait de leur présentation en gouttes et sans saveur.
L’haloanisone (Sedalande *) est une butyrophénone bipérazinée qui a une action rapidement favorable sur l’agitation névrotique et psychotique non confusionnelle aux doses de 1 à 4 ampoules de 20 mg en injection intra musculaire.
Le benperidol (Frenactil*) a une action sur l’excitation psychomotrice des syndromes hypomaniaques, des troubles du caractère de l’agressivité des vieillards et, à doses faibles, sur les tics. Sa posologie moyenne est de 2 à 6 mg. Malgré sa bonne tolérance, il a les effets secondaires des neuro leptiques : somnolence et parkinson thérapeutique.
Le pipanpérone (Dipiperon *) est une butyrophénone qui apporterait d’une manière générale un meilleur contrôle de l’impulsivité et de l’agressivité. Aussi est-il indiqué dans les troubles caractériels des enfants et des ado lescents, dans les troubles du caractère et du comportement des sujets âgés (irritabilité, turbulence, récrimination, colères, opposition, etc.). Il est égale ment indiqué dans les troubles caractériels des alcooliques, des épileptiques, des psychotiques et des oligophrènes. Il se prescrit à la dose moyenne de 1 à 6 comprimés de 40 mg par jour. C’est aussi un inducteur de sommeil.
Le pimozide (Orap *, Opiran *) est un dérivé des butyrophénones, mais diffère de ces dernières par la modicité des effets neurologiques secondaires et aussi des effets dépresseurs sur la vigilance. Comme les butyrophénones il est un neuroleptique antipsychotique incisif : anti-hallucinatoire, anti-délirant et anti-autistique. Il semble qu’il soit indiqué surtout dans les cures d’entretien au cours des psychoses hallucinatoires ou schizophréniques chroniques en raison de sa bonne tolérance et surtout de l’absence habituelle des phéno mènes extra-pyramidaux qui rend plus facile le contact et la réinsertion sociale. D’autre part son action prolongée permet de prescrire une seule prise du médicament le soir aux doses moyennes de 1 à 4 comprimés de 4 mg ou plus.
Les benzamides substitués. — Cette famille de médicaments fit son apparition en psychopharmacologie en 1967 et malgré son originalité propre (Sem. Hôp. Paris, 1976, n° spécial, 52, 32 B, 1-68) on la rattache aux neuroleptiques. Elle comprend actuellement trois représentants : le sulpiride, le sultopride, le tiapride.
Le Sulpiride (Dogmatil*), comme la plupart des neuroleptiques, possède un mode d’action variable avec sa posologie. A faibles doses (2 à 4 gélules à 50 mg) il a une action tranquillisante par un effet anxyolitique, une détente et une prise de distance des problèmes chez les névrotiques. A fortes doses (2 à 4 comprimés de 200 mg ou 4 à 6 ampoules de 100 mg I. M. dans les traitements d’attaque) il convient aux psychotiques par une action sur l’acti vité délirante et hallucinatoire et une action désinhibitrice et stimulante qu’il convient toutefois de surveiller, faute de quoi on provoquerait une irri tabilité, une agitation et une réactivation du délire (Sutter, Scotto et Dufour, 1976).
Le Sultopride (Barnetil *) aux doses de 2 à 6 ampoules I. M. de 200 mg ou de 1 à 3 comprimés de 400 mg aurait un effet antipsychotique et désinhibiteur un peu moindre que le sulpiride mais par contre une action sédative plus mar quée et rapide, aussi trouve-t-il ses indications dans les états d’agitation aigus particulièrement dans les accès maniaques et les accès d’agitation psycho-motrice survenant chez les psychotiques chroniques (Marie-Cardine, Mérel et Cottreaux, 1976).
Le Tiapride (Tiapridal*) recommandé dans les états d’agitation et d’agressi vité, notamment au cours de l’alcoolisme chronique.
Les « effets secondaires » et les accidents au cours des traitements par les neuroleptiques
Sans doute est-il très artificiel de discerner dans l’utilisation des neuro leptiques des effets secondaires et des effets primaires, le médicament a toujours un effet global et une action sur l’organisme tout entier. Force nous est pourtant, en pratique clinique, d’atténuer ou d’éliminer si possible des manifestations non désirées lors de la prescription du traitement, ce sont les « effets secondaires ». Ceux-ci, en général sans gravité, se définissent par rapport à l’effet primaire ou effet thérapeutique recherché, c’est-à-dire la disparition d’un délire, d’hallucinations ou autres « syndrome-cible ». Nous aurons l’occasion de revenir sur les critiques que l’on peut adresser à ce dernier concept.
Nous distinguerons d’autre part les accidents proprement dits qui sont des troubles chroniques ou graves, pouvant entraîner la mort en l’absence d’une surveillance attentive.
1° Les effets secondaires des traitements par les neuroleptiques
— Ces effets secondaires sont généralement bénins, avons-nous dit, à condi tion toutefois de respecter certaines règles de prudence applicables à tous les neuroleptiques.
Les signes neurologiques et neurovégétatifs. — Ce sont les symptômes les plus fréquents et les plus précoces (Sigwald et coll., Sem. Hôp. Paris, 1960, 36, 2215).
Le syndrome akinétique est constitué par une réduction de la mimique, la rareté du clignement, une lenteur de la parole, une maladresse pour l’articu lation des labiales, une marche guindée avec diminution du balancement des bras.
Ce syndrome peut s’accompagner de troubles psychiques : désintérêt, perte de l’initiative, somnolence, hébétude et passivité. C’est le syndrome neuro leptique (Le Guillant, 1957) ou le « comportement de passivité » (P. Balvet, 1959). Le ralentissement, l’asthénie, l’inhibition, l’indifférence affective peu vent devenir très gênants et empêcher toute coopération du malade à sa réadaptation et peuvent même le confiner au lit. Bien entendu à ce stade il est nécessaire de réduire voire d’interrompre le traitement et de corriger les troubles par des analeptiques.
Le syndrome akinéto-hypertonique constitue un syndrome parkinsonien. C’est le syndrome précédent auquel s’ajoute une hypertonie musculaire plus ou moins marquée et des signes de la série parkinsonienne.
Les dyskinésies peuvent être isolées ou associées à l’hypertonie, elles atteignent surtout la région facio-céphalique : la langue (mouvements involontaires incessants de protusion, de rotation, de rétraction), les lèvres (mouvements de succion, de mâchonnements) les mâchoires (mouvements de bâillement). Ces dyskinésies peuvent donner au malade des difficultés pour s’alimenter ou pour absorber les comprimés. Les dyskinésies peuvent s’étendre aux muscles du cou, c’est alors le tableau impressionnant de la dyskinésie bucco-linguo-pharyngo-faciale qui s’accompagne généralement d’angoisse.
Les tremblements dus aux neuroleptiques sont du type parkinsonien et affectent les extrémités. C’est un symptôme difficile à corriger.
On peut assister également à des paresthésies : fourmillements, courba tures, impatiences dans les jambes, phénomène d’akathisie (impossibilité de rester assis) et de tasikinésie (impossibilité de rester en place et besoin impérieux de déambuler.
Les dyskinésies peuvent se présenter à l’état aigu ou à l’état chronique.
Les dyskinésies aiguës consistent en protusion de la langue incoercible, en contraction des muscles bucco-pharyngés, en mouvements axiaux divers notamment de torsion ou de rejet en arrière de la tête (en opisthotonos) et projection des bras en avant. Des crises oculogyres peuvent accompagner ces dyskinésies ou apparaître isolément.
Ces crises aiguës cèdent — parfois difficilement — à la prescription d’un anti-parkinsonien par la voie buccale ou par la voie intramusculaire. Le traitement neuroleptique peut généralement être poursuivi.
Les dyskinésies chroniques surviennent par contre après un traitement de longue durée et leur sensibilité aux correcteurs est très incomplète. Elles se traduisent par des déambulations permanentes (akathisie et tasikinésie), des mouvements de mâchonnement, des tics bucco-linguaux, etc. La mastication et même la déglutition peuvent être gênées mais c’est surtout leur aspect disgrâcieux et grimaçant qui est remarqué par le patient et son entourage. Nous retrouverons plus loin au paragraphe des accidents ces dyskinésies chroniques.
Les crises comitiales constituent un accident peu fréquent du traitement par les neuroleptiques, le rôle épileptogène des neuroleptiques n’est pas formel lement établi.
En dehors de toutes manifestations cliniques les modifications les plus fréquemment rencontrées sur le tracé électro-encéphalographique sont un ralentissement et à une amplitude plus grande du rythme alpha, l’apparition de quelques activités thêta et delta pouvant s’accompagner d’une baisse du niveau de vigilance et d’un état de somnolence, des réponses plus nettes à l’hyperpnée et à la stimulation lumineuse intermittente.
D’une manière générale l’activité électrique cérébrale n’est vraiment modi fiée que pour les doses élevées de neuroleptiques.
Des troubles neuro-végétatifs sont par contre fréquents. Ce sont des troubles visuels : troubles de l’accommodation avec parésie des muscles pupillaires. Toutefois il y a lieu de noter que les anti-parkinsoniens prescrits simultané ment peuvent jouer un rôle dans l’apparition de ce syndrome. On peut également observer de la sécheresse de la bouche (les anti-parkinsoniens peuvent ici encore jouer un rôle) ou au contraire une hypersialorrhée, des troubles respiratoires, des troubles thermiques qu’il ne faut jamais négliger et toujours considérer qu’ils peuvent être un signe d’alarme, notamment d’une hyperthermie maligne sur lesquels nous reviendrons.
Les troubles neurologiques et notamment parkinsoniens étant les plus fréquents et les plus gênants il convient d’associer préventivement, et généra lement de façon systématique, des médicaments anti-parkinsoniens : le trihexyphényle (Ariane*), l’orphénadrine (Disipal*), l’étybenzatropine (Ponalide*), la tropatépine (Lepticure*). Notons qu’il n’y a pas de proportionnalité entre la posologie des anti-parkinsoniens et celle des neuroleptiques.
On peut aussi associer aux neuroleptiques incisifs des neuroleptiques séda tifs : de la lévomépromazine (Nozinan*) ou de la thioridazine (Melleril*) afin de diminuer les effets excito-moteurs des neuroleptiques incisifs.
Troubles cardio-vasculaires. — Ces troubles sont généralement bénins : une hypotension modérée pouvant s’accompagner de lipothymies et surtout une hypotension orthostatique, une tachycardie et très rarement une hypertension.
On admet pourtant maintenant que les substances psychotropes peuvent avoir une action pathogène grave sur le myocarde (Saint-Pierre et coll., 1972) cardiopathies ischémiques, troubles rythmiques dans l’intoxication aiguë et chronique, myocardiopathies d’allure primitive. Divers mécanismes physiopathologiques ont été invoqués notamment l’altération des fibres musculaires, la production de foyers d’ischémie ou de nécrose locale et troubles de la concentration des catécholamines plasmatiques ou myocardiques.
Rappelons le risque grave d’hypertension paroxystique par l’administration de médicaments adrénalinergiques au cours des traitements par les I. M. A. O. (v. p. 197 et 1062).
Il faut encore noter les thromboses vasculaires, les phlébites et surtout les agranulocytoses, d’où la surveillance hématologique des malades soumis à des doses prolongées. Le contrôle électro-cardiographique est surtout utile chez les sujets âgés.
La dihydroergotamine aurait une action préventive en modifiant les condi tions périphériques de l’équilibre vasculaire. De même l’heptaminol peut combattre les troubles cardio-vasculaires bénins.
Les troubles digestifs. — Ils sont constitués par des nausées, des vomisse ments et exceptionnellement par des glossites ou des stomatites.
La constipation est le symptôme qui mérite le plus d’attention. Elle peut être renforcée aussi par les anti-parkinsoniens. Elle nécessite le recours à des médications cholagogues ou cholérétiques.
Les ictères, surtout observés avec la chlorpromazine, sont rares mais appa raissent à n’importe quel moment du traitement, il n’y a pas de corrélation avec la posologie et la durée du traitement. L’évolution de l’ictère peut parfois durer des années, la guérison est toutefois pratiquement toujours obtenue. La prévention en paraît impossible.
Obésité et troubles métaboliques sont constitués par une prise de poids fréquente et souvent considérable, surtout avec les neuroleptiques sédatifs.
Les troubles endocriniens se manifestent par un espacement des règles parfois de l’aménorrhée, de la galactorrhée.
Les troubles cutanés sont constitués par des éruptions, des rashs, des érythèmes solaires par photosensibilisation pouvant aller jusqu’à de véritables brûlures. On a observé aussi des cas d’érythrodermies avec fièvre, asthénie et atteinte de l’état général. Ces accidents cèdent généralement en deux ou trois jours.
Il faut noter aussi des intolérances cutanées présentées par le personnel infirmier.
Les troubles psychiques. — Nous avons déjà parlé des troubles psychi ques les plus banals et les plus fréquents c’est le « syndrome de passivité » généralement associé aux signes neurologiques.
On peut rappeler ici les troubles du sommeil qui, en dehors de la somno lence, peuvent paradoxalement se présenter sous forme d’insomnie ou de sommeil léger entrecoupé de rêves abondants et de cauchemars.
Enfin on peut assister à l’apparition de véritables états confusionnels avec ou sans onirisme ou d’états dépressifs survenant plus particulièrement au cours des traitements de longue durée. Ces derniers états sont favorablement influencés par la prescription des médicaments anti-dépresseurs.
Les signes biologiques. — Ces signes peuvent prendre une certaine impor tance chez des malades traités par des fortes doses de neuroleptiques. Il conviendra de surveiller par des examens répétés ces malades. On peut alors observer des modifications plus ou moins discrètes des tests hépatiques, des inversions du rapport sérines/globulines, d’électrophorèse perturbée avec augmentation soit des alpha-globulines, soit des gamma-globulines, mais surtout des troubles des transaminases.
Le risque d’embryopathie ou de fœtopathies semble minime (Favre, Tissot, 1967). — Néanmoins il paraît prudent de s’abstenir de prescrire des neuro leptiques chez la femme "enceinte ou de déconseiller les grossesses chez les malades en cours de traitement.
Conduite d’automobile ou de machine. — Il est prudent de prévenir tout sujet à qui l’on prescrit un neuroleptique des risques de somnolence. Rappe lons à ce sujet que l’ingestion d’alcool potentialise les effets de somnolence que peuvent provoquer les neuroleptiques.
2° Les accidents des traitements par neuroleptiques
—Les syndromes occlusifs. — Ils apparaissent comme une aggravation de la constipation et peuvent être favorisés comme cette dernière par l’association des anti- parkinsoniens à action atropinique. Ces accidents caractérisés par le météorisme, l’arrêt des matières et de gaz, l’état de choc commande l’arrêt immé diat de la thérapeutique. Ces accidents sont exceptionnels si l’on exerce une surveillance attentive et une prévention des troubles du transit intestinal.
Les syndromes hyperthermiques malins. — Ces syndromes apparaissent la plupart du temps chez les malades traités par les neuroleptiques incisifs (thiopropérazine, Haldol, etc.). Ils sont caractérisés par une fièvre et un tableau de troubles extra-pyramidaux intenses : hypertonie marquée, anxiété, hypersialorrhée, sueurs, troubles de la déglutition, signes pulmonaires : dyspnée, polypnée.
Ce syndrome nécessite l’arrêt immédiat du traitement, l’injection d’antiparkinsoniens, l’administration de perfusion de sérum glucosé avec analep tique, injection systématique d’antibiotiques.
Le traitement ne doit plus être repris.
Les troubles extra-pyramidaux irréversibles. — Il s’agit d’un syndrome parkinsonien qui peut être souvent définitif même après l’arrêt du médica ment. Les troubles sont essentiellement des troubles oraux ou péri-oraux, des mouvements dyskinétiques bucco-linguaux accompagnés de tasikinésie et d’akathisie. Ce syndrome semble rare.
Les troubles oculaires et les pigmentations cutanées. — Il s’agit égale ment de troubles rares ne survenant qu’à des doses extrêmement élevées. Il consiste en pigmentations rétiniennes qui peuvent conduire à la cécité.
Par contre les opacités du cristallin ou de la cornée seraient plus fré quentes. Il s’agit également d’une complication qui survient chez des malades recevant des doses importantes de neuroleptiques. Ces troubles régressent avec la diminution des doses ou l’arrêt du traitement.
On peut observer également, toujours avec de très fortes doses de neuro leptiques, une pigmentation de la peau qui peut aller jusqu’à une couleur ardoisée des téguments.
Intoxications aiguës par les neuroleptiques. — Les intoxications massives par les neuroleptiques se produisent généralement au cours d’une tentative de suicide.
L’examen clinique montrera un coma d’intensité variable caractérisé par un myosis, une hypotonie musculaire, des réflexes ostéo-tendineux d’intensité variable mais généralement vifs, la possibilité d’une hypothermie, l’accéléra tion du pouls, la chute tensionnelle, des troubles respiratoires possibles.
La conduite thérapeutique est celle des comas toxiques.
L’examen cardiologique met en évidence un tracé hypokaliémique.
VIII LES TRANQUILLISANTS
La dénomination de tranquillisant est prise dans des acceptions plus ou moins larges. Dans les pays anglo-saxons (tranquilizer), elle recouvre prati quement tout le groupe des nouveaux psycho-dépresseurs. Nous adopterons la définition par exclusion proposée par Delay et Deniker. Ce groupe assez hétérogène, tant par la provenance chimique de ses composés que par leurs propriétés pharmacologiques, a une relative unité par ses effets cliniques. Ce sont des sédatifs de l’angoisse, se distinguent des neuroleptiques par l’absence de signes neurologiques (modifications neuro-végétatives importantes, inhi bition psychomotrice, effets cataleptiques, troubles du tonus et mouvements anormaux).
Donc, les tranquillisants, comme les neuroleptiques, ont une action psycholeptique qui s’exerce surtout par une diminution de la tension émotionnelle et anxieuse et par une action myo-relaxante.
Les indications générales des tranquillisants sont l’anxiété, l’irritabilité, la tension émotionnelle des états névrotiques, les manifestations neuro végétatives des états psycho-somatiques et beaucoup d’états somatiques avec composante anxieuse. Les tranquillisants n’ont aucune action anti psychotique.
On peut classer les tranquillisants en trois groupes principaux ; d’abord les produits les plus anciens : les carbamates avec leurs congénères les pipérazines et surtout les benzodiazépines dont le nombre des molécules vont continuelle ment croissant dans leur commercialisation et leur emploi peut-être souvent abusif.
Les carbamates. — Ce groupe est assez homogène par ses propriétés chi miques, pharmacologiques et électro-encéphalographiques.
Le méprobamate (Equanil *, Procalmadiol *) est un dérivé d’un myo relaxant non sédatif, le crésoxydiol ou méphénésine (Décontractyl *). Il a été synthétisé par Ludwig et Piech (1950) et constitue le chef de file de cette famille. Il est caractérisé par son action non seulement myo-résolutive due à son effet dépresseur médullaire et central mais aussi psycho-sédative. Ses inconvénients sont la somnolence et l’accoutumance. Celle-ci est d’autant plus dangereuse que le sevrage brusque risque de déclencher un état de mal épileptique. Le méprobamate s’administre par comprimés de 250 ou 400 mg à la dose de 3 à 6 comprimés par jour. Il est indiqué dans tous les états de tension anxieuse, de névrose ou d’instabilité émotionnelle.
En dehors de ses indications tranquillisantes, le méprobamate, sous forme injectable (Equanil * injectable) possède une indication de choix (v. p. 744). dans les états d’agitation et les délires alcooliques : 2 à 10 ampoules de 400 mg par voie intramusculaire.
Les autres représentants de ce groupe sont notamment : l’émylcamate (Statran*) 2 à 8 comprimés de 200 mg, le carbamate de méthylpentynol (N-Oblivon*) 4 à 6 dragées de 0,10 g ou 0,30 g, la butésamide (Modéril*), le cyclohexylpropanol (Equipax*) qui sont essentiellement tranquillisants. Par contre le cyclarbamate (Calmalone*), le carisoprodol (Flexartal*), le gaïaglycol (Calmipan*) ont une action myo-relaxante prévalente, etc.
Le Fenpentadiol (Tredum*) appartient à un groupe très voisin des carba mates, il a une action tranquillisante associée à une action légèrement anti dépressive : 2 à 4 gélules de 100 mg.
Les benzodiazépines. — Le groupe comprend des tranquillisants parmi les plus utilisés actuellement. Nous avons déjà cité les benzodiazépines d’action hypnotique prévalente ainsi que les précautions d’emploi qu’elles exigent. D’autre part, nous trouverons plus loin un tableau récapitulatif (p. 1053) de la plupart d’entre elles actuellement commercialisées avec la posologie moyenne pour chacune, chez l’adulte. Nous ne ferons donc ici que les énumérer, en rappelant qu’il n’existe qu’approximativement une posologie moyenne, la pharmacocinétique (v. p. 1024) étant variable d’un individu à l’autre. A titre d’indication nous donnerons pour chacune la demi-vie, en heures (temps néces saire pour que la concentration plasmatique maximale diminue de moitié et pour que par suite l’on puisse en déduire son accumulation et son élimination ainsi que ses métabolites).
Nous rappellerons préalablement l’essentiel des précautions d’emploi pour toutes benzodiazépines.
Les contre-indications sont les allergies connues aux benzodiazépines ainsi que les insuffisances respiratoires sévères et les insuffisances cardiaques graves. La myasthénie est une contre-indication.
La durée du traitement exige un suivi du malade qui apprécie le maintien de l’efficacité et la nécessité de le poursuivre. Ne jamais interrompre brutale ment un traitement, surtout à doses élevées. Les phénomènes de sevrage seront évités en réduisant progressivement les doses. L’absorption de boissons alcooli sées est formellement déconseillée pendant le traitement. La vigilance est réduite et la somnolence possible. Le malade susceptible de conduire une machine doit en être averti. Éviter la prescription de ces médicaments au cours du premier trimestre de la grossesse et éviter également de prescrire des doses élevées au cours du dernier trimestre (risques d’hypotonie, d’hyperthermie et de détresse respiratoire chez le nouveau-né). Pendant la lactation ces médicaments ne sont pas recommandés. Des interactions médicamenteuses doivent être sur veillées, une synergie avec certains antidépresseurs risque de majorer la sédation et en cas d’arrêt brutal de majorer le syndrome de sevrage. On surveillera, et on instruira, le malade des effets indésirables : somnolence, hypotonie muscu laire, hypotension, sensations ébrieuses, amnésies antérogrades, éruptions cutanées prurigineuses, irritabilité du caractère, exceptionnellement des myoclonies. Les effets indésirables sont fonction des doses, des susceptibilités individuelles, de l’âge, de l’état des émonctoires. Ces effets peuvent être pré venus en débutant le traitement par des doses progressives et éventuellement en le suspendant.
Nous citerons les principales benzodiazépines sans prétention de classement car ni classements cliniques ou biochimiques ne sont possibles. Nous ferons seulement suivre leur dénomination commune internationale (D. C. I.) de leur nom de spécialité en France suivi du nombre d’heures de leur demi-vie. Les benzodiazépines à demi-vie courte, moins de 24 heures, ont un syndrome de sevrage plus rapide et pouvant être accompagnés d’incidents (anxiété, irri tabilité, rebond d’insomnie), exceptionnellement des indicents majeurs, convul sions, états de confusion. Toutefois le concept de demi-vie est relatif, il devrait être tempéré par une meilleure connaissance, encore trop imprécise, des volumes de distribution tissulaire et des sites de réception dans le S. N. C. Nous recen serons : chlordiazépoxide (Librium*, 23 heures), diazépam (Valium*, 32 heures), oxazépam (Séresta*, 8 heures), médazépam (Nobrium*, 2 à 70 heures), lorazépam (Témesta*, 12 heures), clobazam (Urbanil*, 30 heures), nitrazépam (Mogadon*, 23 heures), flunitrazépam (Rohypnol*, 19 heures), triazolam (Halcion*, 2,7 heures), clorazépate dipotassique (Tranxène*, 70 heures), Noc irán* (association, 40 heures), loprazolam (Havlane*, 8 heures), estazolam (Nuctalon*, 24 heures), tétrazépam (Myolastan*, 15 heures), clothiazépam (Vératran*, 4 heures) clonazépam (Rivotril*, 36 heures), tofisopam (Sériel* 8 heures), bromazépam (Lexomil*, 20 heures), prazépam (Lysanxia*, 65 heures), loflazépate (Vician*, 11 heures), alprazépam (Xanax*, 12 à 15 heures), etc.
Les piperazines. — Ce groupe contient les premiers tranquillisants, citons :
L’hydroxyzine (Atarax*) à la dose de 2 à 3 comprimés de 25 ou 100 mg.
La trimétozine (Trioxazine*) 4 à 6 capsules de 300 mg, etc.
La captodiamine (Covatine*) 3 dragées, en 3 fois.
Parmi les divers autres tranquillisants n’appartenant pas aux familles précé dentes nous citerons la benzoctamine (Tacitine*) qui a les indications géné rales des tranquillisants : anxiété, dystonies neuro-végétatives, affections psycho-somatiques ; L’Atrium* (association) comprimés à 100 et 300 mg est aussi utilisé comme tranquillisant mais particulièrement comme antitrémorique.