Chapitre 4
La femme de 18 à 50 ans
L’importance d’une surveillance gynécologique régulière
Les femmes viennent consulter :
 soit en raison de symptômes (douleurs du bas-ventre, pertes vaginales malodorantes ou non, démangeaisons (prurit), saignements en dehors des règles, règles hémorragiques, douleurs lors des rapports sexuels…). L’examen gynécologique permet le plus souvent d’en trouver l’origine ;
soit en raison de symptômes (douleurs du bas-ventre, pertes vaginales malodorantes ou non, démangeaisons (prurit), saignements en dehors des règles, règles hémorragiques, douleurs lors des rapports sexuels…). L’examen gynécologique permet le plus souvent d’en trouver l’origine ;
 soit régulièrement de façon préventive.
soit régulièrement de façon préventive.
Même si tout va bien, un exameàn annuel est conseillé car l’appareil génital féminin est situé en grande partie à l’intérieur du corps et certaines maladies peuvent évoluer sans symptômes. C’est de la médecine préventive. Environ 80 % des femmes acceptent cette surveillance gynécologique régulière.
Au cours de la période de 18 à 50 ans, la femme consulte d’abord pour la contraception, puis la surveillance des grossesses, et ensuite pour la surveillance de la ménopause. L’examen des seins, qui fait partie de l’examen gynécologique, permet de vérifier l’absence de lésion cutanée, de nodule, d’écoulement du mamelon, de ride ou de rétraction de la peau sous forme de capiton, de l’absence de ganglions sous l’aisselle (adénopathie axillaire) ou au-dessus de la clavicule (sus-claviculaire).
Le premier examen
Le premier examen gynécologique est généralement fait dans le cadre d’une demande de contraception. Il n’est pas obligatoire avant une première contraception, surtout si la jeune femme n’a pas encore eu de rapports. Lors de cette première consultation, il est important que le médecin explique son déroulement et son intérêt, ce qui permet d’établir une relation de confiance. L’examen gynécologique n’est pas réalisé si la femme est vierge. Il pourra être fait lors des visites suivantes et sera facilité par le fait que la jeune femme aura déjà eu des rapports. Parfois, le médecin prescrira une pilule, par exemple pour diminuer (voire faire disparaître) les douleurs des règles ou avoir des cycles plus réguliers.
Lors de la prise de rendez-vous, il est préférable de calculer la date pour tomber en dehors de la période des règles.
L’examen gynécologique
Table d’examen gynécologique
L’examen commence par un entretien et un examen général avec prise de tension artérielle, poids, examen de la peau… La patiente se déshabille ensuite en commençant par les vêtements du bas du corps, les vêtements du haut pouvant être retirés secondairement, et s’allonge sur une table d’examen, les talons reposant sur des étriers ou les jambes reposant sur des appuis-jambes le plus souvent.
Le médecin (généraliste ou gynécologue) ou la sage-femme examine les seins et les organes génitaux en commençant par palper le ventre. Il donne les conseils nécessaires pour que la patiente participe activement au dépistage des lésions mammaires en effectuant une autopalpation.
L’autopalpation des seins
Avec la main bien à plat, il faut effectuer des mouvements circulaires afin de s’assurer qu’il n’existe pas de « boule ». On associe à cette autopalpation une inspection devant un miroir de l’aspect des seins lors de la montée et de la descente des bras. On s’assure ainsi que la peau bouge bien avec les mouvements. L’existence d’une tuméfaction, d’un écoulement, d’une ride ou d’un pli sur le sein doit faire consulter un médecin.
Le médecin ou la sage-femme examine la vulve. Avec la main gantée, il mobilise les replis des petites lèvres et de la vulve pour s’assurer de l’absence de lésion. Il cherche à détecter des rougeurs, des lésions érosives ou en relief, des pertes, des kystes ou tout autre problème nécessitant des soins médicaux. Le médecin insère ensuite un spéculum (il en existe de différentes tailles, le plus souvent en plastique à usage unique ou en métal). Il écarte délicatement les petites lèvres pour l’introduire doucement dans l’axe du vagin. Il écarte lentement les « valves » du spéculum afin de voir le fond du vagin où se situe le col de l’utérus. Cet examen n’est pas douloureux mais la femme doit être bien décontractée. Le médecin observe les parois vaginales et procède au frottis. En dépistage systématique, l’examen du frottis est effectué généralement tous les 3 ans entre 25 et 65 ans.
Après avoir retiré le spéculum, le médecin fait un toucher vaginal : il pose une main sur le ventre et introduit délicatement un ou deux doigts (protégés par un doigtier ou un gant) de l’autre main dans le vagin. Il peut ainsi palper l’utérus et les annexes (les ovaires de taille normale ne sont généralement pas perçus). Normalement, cet examen est indolore mais nécessite également une complète décontraction des muscles abdominaux et pelviens.
Le frottis
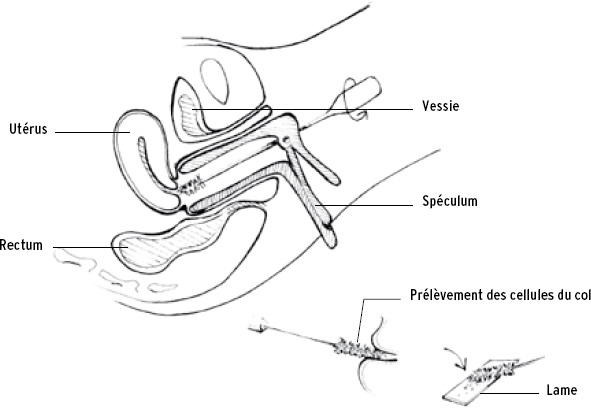
L’examen au spéculum et la réalisation du frottis
Le frottis est le moyen de dépistage des lésions précancéreuses et des cancers du col de l’utérus. Il peut également faire le diagnostic de certaines infections vaginales. Les lésions cancéreuses du col de l’utérus surviennent à la suite d’une infection sexuellement transmissible à papillomavirus humain (HPV). Ces virus, très fréquents, s’attrapent facilement lors des contacts sexuels. Un frottis anormal correspond à une infection par le virus HPV. Dans 80 % des cas, les femmes guérissent spontanément de l’infection. Mais dans 10 % des cas, le virus persiste et pourrait provoquer, en l’absence de traitement, des lésions évoluant vers un cancer quelques années plus tard (voir chapitre 8).
Le frottis est un examen rapide et indolore. Le médecin utilise une petite brosse ou une spatule pour prélever des cellules par de légers frottements au niveau du col. Les prélèvements sont adressés à un laboratoire qui en fait l’analyse dans le mois qui suit. Les résultats sont envoyés au médecin et à la patiente par le laboratoire. Il est convenu, en général, que le médecin ne recontacte la patiente qu’en cas de résultat anormal.
Les femmes concernées par ce dépistage sont celles âgées de 25 à 65 ans ayant une activité sexuelle. La régularité des frottis est indispensable pour que le dépistage du cancer du col de l’utérus soit efficace, car les cellules anormales peuvent mettre un certain temps à apparaître. Les deux premiers frottis sont réalisés à un an d’intervalle, pour éviter les faux négatifs puis généralement tous les trois ans jusqu’à au moins 65 ans.
Une vaccination anti-HPV, très efficace, est actuellement proposée entre 11 et 14 ans. Il existe un rattrapage jusqu’à l’âge de 19 ans révolus en sachant que la vaccination sera d’autant plus efficace que la jeune femme n’a pas eu d’infection au HPV. Cette vaccination est remboursée par la Sécurité sociale (voir chapitre 7).
Se préparer à avoir un enfant
Avoir un enfant est un projet important pour un couple. Il est mieux de consulter avant le début de la grossesse pour rechercher des facteurs de risque, adapter d’éventuels traitements, vérifier les sérologies (recherche d’immunisation, de maladies infectieuses…), le groupe sanguin. Bien des problèmes seraient simples s’ils étaient vus avant le début de la grossesse et non lors de sa déclaration.
Consulter avant la conception
La Haute Autorité de santé recommande cette consultation qui doit comprendre un interrogatoire à la recherche :
 d’une pathologie familiale ;
d’une pathologie familiale ;
 d’une pathologie chronique : hypertension, diabète, thrombophilie, d’une conduite addictive (tabagique, alcoolique, drogues illicites) ;
d’une pathologie chronique : hypertension, diabète, thrombophilie, d’une conduite addictive (tabagique, alcoolique, drogues illicites) ;
 d’un traitement médicamenteux actuel : antiépileptique, psychiatrique…
d’un traitement médicamenteux actuel : antiépileptique, psychiatrique…
L’examen clinique complet comprend :
 la mesure de la taille et du poids, de la tension artérielle ;
la mesure de la taille et du poids, de la tension artérielle ;
 l’examen des seins ;
l’examen des seins ;
 l’examen gynécologique avec un frottis si la femme n’en a pas eu dans les trois dernières années.
l’examen gynécologique avec un frottis si la femme n’en a pas eu dans les trois dernières années.
Le médecin prescrit également un groupe sanguin complet, une prise de sang pour savoir si la patiente a eu la rubéole et la toxoplasmose, et propose une sérologie VIH et de l’hépatite C.
Après l’examen et les prescriptions, le médecin propose, avant l’arrêt de la contraception :
 un rappel du vaccin tétanos-polio-diphtérie si cela s’avère nécessaire ;
un rappel du vaccin tétanos-polio-diphtérie si cela s’avère nécessaire ;
 une vaccination contre la rubéole, les oreillons la varicelle, la coqueluche si la femme n’est pas immunisée ;
une vaccination contre la rubéole, les oreillons la varicelle, la coqueluche si la femme n’est pas immunisée ;
 de modifier les habitudes alimentaires avec l’aide d’une diététicienne en cas d’obésité ;
de modifier les habitudes alimentaires avec l’aide d’une diététicienne en cas d’obésité ;
 d’entamer un sevrage en cas de conduite addictive (tabac, alcool…) ;
d’entamer un sevrage en cas de conduite addictive (tabac, alcool…) ;
 de consulter un conseil génétique en cas de pathologie familiale ;
de consulter un conseil génétique en cas de pathologie familiale ;
 en cas de maladie chronique, il faut envisager, avec éventuellement les conseils d’un spécialiste, d’informer le couple des difficultés que posera la surveillance de la grossesse, d’adapter le traitement et de programmer la grossesse dans les meilleures conditions possibles.
en cas de maladie chronique, il faut envisager, avec éventuellement les conseils d’un spécialiste, d’informer le couple des difficultés que posera la surveillance de la grossesse, d’adapter le traitement et de programmer la grossesse dans les meilleures conditions possibles.
La prescription d’acide folique (vitamine B9), 0,4 mg par jour par voie orale, un mois avant la conception et pendant le premier trimestre de la grossesse, diminue de 80 % le risque d’anomalies fœtales du tube neural (spina bifida), mais aussi une baisse des malformations cardiaques, urinaires, des membres, et une malformation de l’anus (imperforation anale). Chez les femmes prenant un traitement antiépileptique, la posologie d’acide folique est de 4 mg par jour.
FAQ
Combien de temps faut-il pour tomber enceinte ?
Le temps est l’allié du couple : quand une grossesse est désirée, on sait qu’elle peut ne pas être obtenue dès le premier cycle « exposé à la grossesse ». Statistiquement, si l’on se réfère à une population dont la fertilité serait normale, il faut en moyenne 4 à 6 cycles pour obtenir la grossesse. Certains, chanceux, vont l’obtenir dès le premier cycle. D’autres, moins chanceux mais tout aussi normaux, vont mettre jusqu’à 12 cycles.
Le temps est aussi l’ennemi principal du couple qui désire une grossesse. Il est à la fois le témoin qu’il y a peut-être un problème qui pourrait être la cause de l’infécondité actuelle et la cause d’une dégradation supplémentaire de la fertilité. D’où l’urgence ressentie de façon d’autant plus aiguë que le couple approche des âges limites au-delà desquels la fécondité devient aléatoire.
Préserver sa fertilité
L’effet nocif du tabac sur la fertilité naturelle de la femme et de l’homme, et sur les résultats de tous les traitements de l’infertilité, est désormais bien démontré. Le tabagisme augmente le risque d’infertilité féminine, diminue la fécondabilité (la probabilité de concevoir par cycle), allonge le délai naturel de conception par rapport à des femmes qui ne fument pas, et enfin augmente le risque de fausses couches spontanées. Il avance aussi l’âge de la ménopause d’environ 2 ans et augmente le risque d’insuffisance ovarienne prématurée. Chez l’homme aussi, fumer diminue la fertilité et allonge le temps nécessaire pour concevoir. L’arrêt du tabac est donc recommandé à tous les couples qui souhaitent un enfant.
L’effet nocif des autres toxiques est moins bien démontré chez la femme que celui du tabac, mais semble réel : drogues, alcool, café (en excès, plus de 6 à 7 tasses par jour, il faut aussi se méfier de la caféine contenue dans d’autres boissons comme celles à base de cola) nuisent à la fertilité aussi bien féminine que masculine.
De nombreux autres facteurs tels que l’exercice physique excessif, le stress psychologique ou l’exposition à des polluants environnementaux sont également susceptibles d’agir sur la fertilité de la femme. La démonstration de leur effet délétère est nettement moins évidente chez l’homme. Enfin certains traitements médicaux, radiothérapie ou chimiothérapie peuvent altérer la fertilité. Il est possible désormais de proposer de préserver des chances de grossesses ultérieures en congelant soit les ovocytes, soit un fragment d’ovaire avant de débuter ces traitements.
Le principal « toxique » pour la fertilité féminine reste l’âge, problème accentué actuellement par le désir tardif d’enfant. Le slogan du planning familial « un enfant que je veux » a été mal compris. Les femmes l’ont pris au pied de la lettre. Il faudrait le remplacer par « un enfant tant que je peux ». La prise de la pilule contraceptive n’est pas en cause, mais les ovaires vieillissent, ce qui diminue les chances de procréer. L’utérus, lui, reste apte à accueillir une grossesse longtemps après la ménopause, comme l’illustrent les exemples de grossesse à 60 ans et plus, rapportés par les médias.
Il n’y a actuellement aucun moyen de lutter efficacement contre le vieillissement ovarien. Tous les traitements de l’infertilité (stimulation de l’ovulation, inséminations intra-utérines, fécondations in vitro…) voient leurs résultats chuter dès 35 ans, et l’assistance médicale à la procréation (AMP) n’est malheureusement pas la baguette magique qui compense ce vieillissement. Le don d’un ovocyte provenant d’une donneuse jeune remédie certes à l’infertilité liée à l’âge, mais ce bébé n’a plus l’héritage génétique de la femme en désir de grossesse. L’autoconservation des ovocytes proposée jusqu’à maintenant en France, exclusivement avant traitement potentiellement stérilisant, pourrait compenser le vieillissement ovarien, mais n’est pas sans poser quelques problèmes !
L’enfant tarde à venir : le bilan de base
À condition de s’en donner les moyens, un couple peut avoir une vie sexuelle épanouie tout en planifiant les naissances. Mais attention, l’inverse n’est pas toujours aussi simple. Une décision, mûrement réfléchie et partagée à deux, que le moment est venu, peut ne pas être suivie d’effet. Que se passe-t-il ?
FAQ
Quand commencer à s’en préoccuper ?
La définition médicale de la « stérilité » est deux ans de rapports sans précaution. En fait, il est le plus souvent justifié de s’en préoccuper plus tôt. Plus le couple est jeune, plus sa fertilité devrait être élevée. Donc, logiquement, si tout était normal, il devrait rapidement réussir à débuter une grossesse. Inversement, si le couple est plus âgé, avec une fertilité moindre, la période pour parvenir à une grossesse est statistiquement plus longue. L’urgence est donc plus pressante. La plupart des couples commencent à consulter sans attendre deux ans, et ils ont raison.
Quel est le bon moment ? Comment diagnostiquer sa période fertile ?
La femme n’est potentiellement féconde que juste avant l’ovulation. Chez celles qui ont un cycle régulier, un simple calcul permet d’avoir une idée approximative de la période pendant laquelle cette ovulation se produit : 12 à 14 jours après le début de règles, ou encore 12 à 14 jours avant les règles à venir. Si le cycle est très différent des 28 jours « classiques », ou s’il est irrégulier, ce calcul n’est plus possible. Il existe dans le commerce des tests d’ovulation qui permettent de déterminer la période de fécondité. Ils sont principalement à usage contraceptif afin d’éviter les rapports pendant cette période. Ils peuvent aussi être employés dans le but inverse, à condition de ne pas leur faire dire ce qu’ils ne peuvent pas dire : notamment, ils n’ont pas de signification pour ce qui est d’évaluer la qualité de l’ovulation.
FAQ
Est-ce bien nécessaire de diagnostiquer sa période fertile ?
Avec une fréquence habituelle de deux à trois rapports par semaine, quelle que soit la période du cycle de la femme, les besoins sont couverts et la fertilité est optimisée. La recherche de sa période de fertilité ne fait qu’ajouter une part de calcul à un élan qui devrait rester spontané, sans pour autant améliorer les chances de fécondité. Cela aboutit même parfois à l’effet inverse de celui qui est recherché et peut inutilement générer de l’angoisse. Il n’est utile de le faire que si les rapports sexuels sont peu fréquents ou que la vie éloigne régulièrement les deux membres du couple.
Il faut bien entendu qu’il y ait des rapports sexuels entre les deux conjoints. On peut supposer que l’absence de rapport, ou leur réalisation difficile ou incomplète, serait révélée par le couple, ne serait-ce qu’en réponse aux questions que celui-ci ne manquera pas de poser.
« Nos amis n’ont pas de problème : ils en sont déjà à leur deuxième. Que font-ils de plus que nous ? Nous sommes pourtant normaux ! Nous ne sommes pas malades. » On dit qu’il ne faut pas y penser. Alors on fait semblant d’oublier, mais en fait on y pense toujours, on ne peut pas faire autrement. Quand on fait l’amour, on vérifie que c’est le bon moment (mais c’est quoi le bon moment ?). On espère toujours que, cette fois, ça va être productif. L’arrivée des règles est une nouvelle déception de plus en plus difficile à surmonter. On s’isole, on refuse les invitations des amis pour le week-end ; c’est trop dur de voir les enfants des autres courir, et surtout, de risquer de se faire poser la question qui fait si mal : « Alors, quand vous y mettez-vous ? »
Dans ces circonstances, les couples n’ont besoin ni de « bons conseils », ni de commisération. Ils ont surtout besoin de comprendre. Il ne faut pas hésiter à s’adresser à son médecin qui saura prescrire les examens de base et orienter vers un médecin spécialiste afin d’y recevoir l’aide appropriée.
FAQ
Médecin généraliste ? Gynécologue ? Spécialiste de la reproduction ? Qui consulter ?
Pour commencer son bilan, il faut s’adresser à son médecin traitant, spécialiste de médecine générale, ou à un gynécologue, spécialiste de gynécologie médicale ou de gynécologie-obstétrique. Les médecins généralistes ont la compétence requise pour vous faire réaliser le bilan de base. Au-delà, il vous adressera à un spécialiste. Le spécialiste luimême peut être amené, en fonction des résultats du bilan de base, à demander l’intervention d’un andrologue (qui s’occupe des problèmes masculins) ou d’un endocrinologue (pour les problèmes métaboliques et hormonaux).
Si vous avez besoin d’avoir recours à l’assistance médicale à la procréation, seuls des centres ayant une autorisation administrative peuvent y procéder.
Vaut-il mieux s’adresser directement à un centre ultra-spécialisé ? C’est vraiment affaire de circonstances, différentes d’une ville à une autre, variables aussi selon les cas individuels. La seule règle générale est de ne pas perdre de temps. Le temps qui passe joue en effet contre le couple, les résultats potentiels des traitements étant grandement affectés lorsqu’ils sont réalisés tardivement. Il faut donc privilégier « l’accessibilité », l’essentiel étant de demander un avis médical sans attendre. Il vous faut ensuite, bien entendu, établir une relation de confiance avec votre médecin, obtenir des réponses claires aux questions que vous vous posez et comprendre la logique des propositions de prise en charge qui vous sont faites.
La conception et le développement harmonieux de la grossesse sont de véritables miracles de la nature. Quand le bébé naît, l’émerveillement est à la hauteur de la finesse des phénomènes qui se sont déroulés. Comment peut-il être si bien fait et si beau ? Qu’est-ce que ça doit être compliqué ! Il n’est pas étonnant que, de temps en temps, cela puisse dérailler et ne pas marcher aussi bien que ce qu’il le faudrait ! En fait, sans minimiser la complexité des processus biologiques qui aboutiront à la fécondation d’un ovocyte (la cellule initiale issue de la femme) par un spermatozoïde (la cellule initiale issue de l’homme), puis à l’implantation de l’embryon nouvellement formé dans l’utérus maternel, l’initiation d’une grossesse peut se résumer à la mise en œuvre harmonieuse de quelques grandes fonctions.
La fonction d’ovulation
L’ovulation est la production par la femme de l’ovocyte qui, on l’espère, va pouvoir être fécondé. Ces ovocytes, présents dans les ovaires dès la naissance, sont encore immatures, non fécondables en l’état (voir chapitre 1). À chaque cycle, la femme en émet un qui a pu bénéficier de tous les processus de maturation qui le rendent fécondable. L’émission de l’ovocyte mature (l’ovulation) s’accompagne d’une modification hormonale tout à fait particulière : la sécrétion de progestérone, qui se détecte de plusieurs façons.
 La disparition de la glaire cervicale. La glaire cervicale est spécialement abondante pendant l’ovulation et bien utile pour permettre le passage des spermatozoïdes vers la cavité utérine afin de rejoindre l’ovocyte pour le féconder. Dès que la progestérone commence à être sécrétée, la glaire se tarit. C’est cependant un signe clinique peu sensible et qui peut passer inaperçu. Il n’est pas suffisant pour affirmer qu’il y a eu ovulation et surtout pour en évaluer la qualité. L’absence de glaire cervicale peut aussi être due à d’autres causes.
La disparition de la glaire cervicale. La glaire cervicale est spécialement abondante pendant l’ovulation et bien utile pour permettre le passage des spermatozoïdes vers la cavité utérine afin de rejoindre l’ovocyte pour le féconder. Dès que la progestérone commence à être sécrétée, la glaire se tarit. C’est cependant un signe clinique peu sensible et qui peut passer inaperçu. Il n’est pas suffisant pour affirmer qu’il y a eu ovulation et surtout pour en évaluer la qualité. L’absence de glaire cervicale peut aussi être due à d’autres causes.
 L’apparition des règles. Le corps jaune, qui s’est formé juste après l’ovulation à la surface de l’ovaire et qui sécrète la progestérone, a une durée de vie limitée de 10 à 12 jours. C’est au terme de cette durée que, en l’absence de grossesse, la sécrétion de progestérone diminue et provoque l’apparition des règles. Mais, là encore, l’apparition des règles et la régularité des cycles ne peuvent être retenues comme des preuves suffisantes de l’ovulation.
L’apparition des règles. Le corps jaune, qui s’est formé juste après l’ovulation à la surface de l’ovaire et qui sécrète la progestérone, a une durée de vie limitée de 10 à 12 jours. C’est au terme de cette durée que, en l’absence de grossesse, la sécrétion de progestérone diminue et provoque l’apparition des règles. Mais, là encore, l’apparition des règles et la régularité des cycles ne peuvent être retenues comme des preuves suffisantes de l’ovulation.
 Le changement de la température basale. La progestérone, entre autres effets, augmente de quelques dixièmes de degré la température basale. Ce n’est pas de la « fièvre » et cette augmentation n’est visible que si la femme a pris sa température après la nuit, avant de se lever, avant toute activité, et de façon quotidienne, et a reporté chaque température matinale sur un graphique approprié. En cas d’ovulation, une légère augmentation thermique (+ 0,4 °C) apparaît aux alentours du milieu du cycle et se maintient pendant 10 à 12 jours. Ce phénomène est le témoin de la sécrétion de progestérone par le corps jaune qui s’est formé à la surface de l’ovaire après l’ovulation. La courbe de température est donc un moyen peu coûteux, qui ne nécessite pas de prescription médicale, pour vérifier si une ovulation est présente. Il y a cependant des limites : certaines femmes n’ont pas de décalage thermique alors que leur ovulation est normale ; inversement, l’existence d’un décalage thermique ne signifie pas pour autant que l’ovulation est de bonne qualité.
Le changement de la température basale. La progestérone, entre autres effets, augmente de quelques dixièmes de degré la température basale. Ce n’est pas de la « fièvre » et cette augmentation n’est visible que si la femme a pris sa température après la nuit, avant de se lever, avant toute activité, et de façon quotidienne, et a reporté chaque température matinale sur un graphique approprié. En cas d’ovulation, une légère augmentation thermique (+ 0,4 °C) apparaît aux alentours du milieu du cycle et se maintient pendant 10 à 12 jours. Ce phénomène est le témoin de la sécrétion de progestérone par le corps jaune qui s’est formé à la surface de l’ovaire après l’ovulation. La courbe de température est donc un moyen peu coûteux, qui ne nécessite pas de prescription médicale, pour vérifier si une ovulation est présente. Il y a cependant des limites : certaines femmes n’ont pas de décalage thermique alors que leur ovulation est normale ; inversement, l’existence d’un décalage thermique ne signifie pas pour autant que l’ovulation est de bonne qualité.
La courbe de température n’est pas un outil mathématique !
Certains voudraient une courbe thermique « parfaite » constituée d’une première phase de 12 à 13 jours où la température se situe en-dessous de 37 °C, puis d’une période de « décalage » étalée sur 1 à 2 jours, qui franchit la barre des 37 °C, puis d’un plateau thermique au-dessus de 37 °C d’une durée de 12 jours, avant la chute de température qui accompagne l’arrivée des règles.
Il n’est le plus souvent pas possible d’évaluer la qualité de l’ovulation à partir de la seule courbe thermique. L’ampleur du décalage thermique n’a pas de signification. Le franchissement de la barre des 37 °C non plus. Certaines femmes sont plus « froides » que d’autres (on fait référence ici à leur métabolisme de base !). Ce qui compte, c’est l’existence ou non d’un décalage thermique qui témoignerait de l’existence d’une ovulation sans qu’on puisse pour autant en déduire avec certitude qu’il s’agit d’une ovulation de qualité satisfaisante.
Et attention de ne pas se servir de ce décalage thermique pour « centrer » les rapports sur la période supposée fertile : quand le décalage est là, il est trop tard ! Les jours les plus fertiles précèdent le décalage thermique.
 Le dosage de la progestérone en deuxième partie de cycle, habituellement aux alentours du 22e au 24e jour du cycle, renseigne sur la présence ou non de l’ovulation. Si l’ovulation est normale, la concentration plasmatique (dans le sang) de la progestérone sécrétée par le corps jaune est de l’ordre de 10 ng/ml. Un dosage proche de zéro signifie qu’il n’y a pas eu d’ovulation. Un résultat intermédiaire fait suspecter une insuffisance du corps jaune (insuffisance lutéale), en général consécutive à une ovulation de qualité insuffisante.
Le dosage de la progestérone en deuxième partie de cycle, habituellement aux alentours du 22e au 24e jour du cycle, renseigne sur la présence ou non de l’ovulation. Si l’ovulation est normale, la concentration plasmatique (dans le sang) de la progestérone sécrétée par le corps jaune est de l’ordre de 10 ng/ml. Un dosage proche de zéro signifie qu’il n’y a pas eu d’ovulation. Un résultat intermédiaire fait suspecter une insuffisance du corps jaune (insuffisance lutéale), en général consécutive à une ovulation de qualité insuffisante.
D’autres dosages hormonaux permettent d’évaluer la réserve ovarienne et le « climat hormonal ».
FAQ
Faut-il avoir des rapports tous les jours pour augmenter les chances d’être enceinte ?
Seuls les rapports en période féconde, habituellement vers le milieu du cycle, peuvent conduire à la grossesse. Certains couples s’arrangent pour avoir un rapport par jour durant cette période pour être sûrs de ne pas laisser passer leur chance. En fait, il n’est pas démontré qu’une augmentation de la fréquence des rapports au-delà de deux à trois rapports par semaine augmente les chances de grossesse. Des rapports trop fréquents pourraient conduire à un appauvrissement de la concentration spermatique et diminuer la fécondité. Surtout, si le couple limite ses rapprochements à cette période supposée féconde, le risque est grand qu’il se trompe et qu’il compromette involontairement ses chances. Quant aux sentiments qui accompagnent normalement la vie sexuelle, ils risquent d’être perturbés…
L’ÉVALUATION DE LA RÉSERVE OVARIENNE
Une femme a un nombre limité d’ovocytes disponibles dans ses ovaires, qui ne cesse de diminuer après la naissance et après la puberté jusqu’à leur disparition complète à la ménopause, qui survient en général autour de la cinquantaine. Mais une diminution significative de la réserve ovarienne survient de nombreuses années avant la ménopause. Vers l’âge de 35 ans, une femme n’a plus que la moitié de son capital initial qui ne cesse ensuite de diminuer. Cette baisse de la réserve ovarienne accompagne la baisse de fécondité avec l’âge, si bien que les deux phénomènes sont souvent confondus. Si la baisse de la réserve ovarienne n’est pas directement la cause de la baisse de la fécondité, sauf quand elle est considérablement diminuée, elle a en revanche une double signification pronostique :
 le temps est d’autant plus compté que la réserve ovarienne est basse ;
le temps est d’autant plus compté que la réserve ovarienne est basse ;
 certains traitements nécessitent une réserve normale pour pouvoir être mis en œuvre.
certains traitements nécessitent une réserve normale pour pouvoir être mis en œuvre.
L’évaluation de la réserve ovarienne se fait à l’aide d’examens en début du cycle :
 des dosages de la FSH (hormone folliculostimulante), de la LH (hormone lutéinisante), du 17-bêta-œstradiol, et surtout de l’AMH (hormone antimüllérienne). Ce dernier dosage n’est pas pris en compte dans les remboursements de l’assurance maladie (et c’est bien entendu une anomalie !), mais il est important de le réaliser car c’est celui qui a la signification la plus précise ;
des dosages de la FSH (hormone folliculostimulante), de la LH (hormone lutéinisante), du 17-bêta-œstradiol, et surtout de l’AMH (hormone antimüllérienne). Ce dernier dosage n’est pas pris en compte dans les remboursements de l’assurance maladie (et c’est bien entendu une anomalie !), mais il est important de le réaliser car c’est celui qui a la signification la plus précise ;
 l’échographie des ovaires réalisée avec une sonde vaginale qui permet de visualiser les petits follicules prêts à être réactivés pour conduire à l’ovulation (voir chapitre 1). Un compte normal est de l’ordre de 7 follicules par ovaire.
l’échographie des ovaires réalisée avec une sonde vaginale qui permet de visualiser les petits follicules prêts à être réactivés pour conduire à l’ovulation (voir chapitre 1). Un compte normal est de l’ordre de 7 follicules par ovaire.
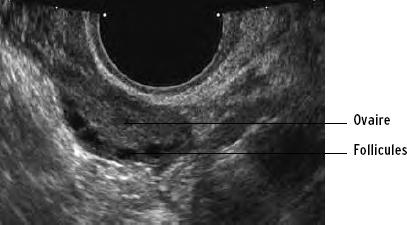
Échographie d’un ovaire normal
L’EXAMEN DU CLIMAT HORMONAL
Il n’a pas de signification directe par rapport à l’ovulation. En revanche, quand l’ovulation est absente ou de qualité insuffisante, les dosages hormonaux permettent de classer le type d’anomalie, ce qui permet le choix thérapeutique le plus pertinent.
L’évaluation des spermatozoïdes
Le but des examens masculins est essentiellement de s’assurer que le sperme se situe dans une fourchette de normalité. En pratique, au-delà de l’interrogatoire médical et de l’examen clinique qui doivent concerner l’homme comme ils ont concerné la femme, la fonction masculine s’explore par la réalisation d’un spermogramme qui mesure plusieurs paramètres :
 le nombre de spermatozoïdes, normalement supérieur à 20 millions par ml. En-dessous de 10 millions, on parle d’oligospermie ; au-dessus de 100 millions, ce n’est pas normal non plus, on parle de polyzoospermie ;
le nombre de spermatozoïdes, normalement supérieur à 20 millions par ml. En-dessous de 10 millions, on parle d’oligospermie ; au-dessus de 100 millions, ce n’est pas normal non plus, on parle de polyzoospermie ;
 la mobilité des spermatozoïdes, qui doivent en effet être mobiles pour pouvoir être fécondants. Une mobilité « fléchante », avec un trajet rectiligne (a), est meilleure qu’une mobilité désordonnée (b), et à plus forte raison qu’une mobilité sur place ou pas de mobilité du tout. Ces différents types de mobilité font l’objet d’un classement et on considère comme normal une mobilité a + b (les deux premiers types de mobilité) supérieure ou égale à 50 %. En cas d’insuffisance de mobilité, on parle d’asthénospermie ;
la mobilité des spermatozoïdes, qui doivent en effet être mobiles pour pouvoir être fécondants. Une mobilité « fléchante », avec un trajet rectiligne (a), est meilleure qu’une mobilité désordonnée (b), et à plus forte raison qu’une mobilité sur place ou pas de mobilité du tout. Ces différents types de mobilité font l’objet d’un classement et on considère comme normal une mobilité a + b (les deux premiers types de mobilité) supérieure ou égale à 50 %. En cas d’insuffisance de mobilité, on parle d’asthénospermie ;
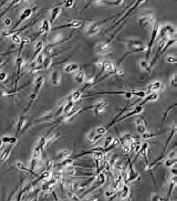
Examen des spermatozoïdes
 la morphologie des spermatozoïdes. Est-ce l’effet de leur grand nombre ? Il y a beaucoup de spermatozoïdes malformés qui ont une anomalie de la tête ou du flagelle. Le taux d’anomalies peut atteindre jusqu’à 70 % des spermatozoïdes ! En cas de taux trop élevé de spermatozoïdes anormaux, on parle de tératospermie.
la morphologie des spermatozoïdes. Est-ce l’effet de leur grand nombre ? Il y a beaucoup de spermatozoïdes malformés qui ont une anomalie de la tête ou du flagelle. Le taux d’anomalies peut atteindre jusqu’à 70 % des spermatozoïdes ! En cas de taux trop élevé de spermatozoïdes anormaux, on parle de tératospermie.
FAQ
Y a-t-il un risque de malformation fœtale au cas où un spermatozoïde anormal venait à féconder un ovocyte ?
Heureusement non ! Les processus de régulation sont nombreux, parmi lesquels en premier lieu la moindre fécondance des spermatozoïdes anormaux.
En cas de sperme anormal, l’oligospermie, l’asthénospermie et la tératospermie sont souvent associées. Attention cependant à ne pas prendre la conclusion du spermogramme au pied de la lettre. Il n’a qu’une valeur d’orientation. En effet, si un sperme « normal » a de bonnes chances d’être aussi fécond, ce n’est pas absolument certain. Inversement, si le sperme est anormal, sa fécondance (capacité de féconder un ovocyte) peut être diminuée, mais ici encore la certitude n’est pas acquise. On dit toujours qu’il suffit d’un seul…
La perméabilité de l’utérus et des trompes
Si l’ovulation a lieu et si le sperme est normal, il faut encore que la rencontre ovocyte-spermatozoïde se produise dans le tiers externe de la trompe. Cela suppose qu’il n’y ait pas d’obstacle. En pratique, la normalité de la filière génitale (pas d’obstacle dans l’utérus et les trompes) s’évalue par la réalisation d’une échographie pelvienne, le plus souvent à l’aide d’une sonde d’échographie par voie vaginale. Elle permet de vérifier la forme de l’utérus, de mesurer l’épaisseur de l’endomètre (la couche cellulaire qui tapisse la cavité utérine), de vérifier la présence d’ovaires normaux et de faire le compte de leurs follicules.
En revanche, l’échographie peut difficilement évaluer les trompes qui sont habituellement trop fines pour être visibles et encore moins leur perméabilité. Ce rôle est confié à l’hystérosalpingographie. Comme son nom l’indique, cet examen est une radiographie des organes génitaux, réalisée avec injection d’un produit de contraste qui opacifie les cavités dans lesquelles il s’écoule, c’est-à-dire l’utérus et les trompes. Il permet de vérifier la normalité de la cavité utérine, de forme grossièrement triangulaire, ainsi que la perméabilité des trompes qui doivent laisser s’écouler le liquide de contraste dans la cavité abdominale sans qu’il y ait de stagnation ou d’accumulation. Pour un rappel des organes génitaux internes, voir le schéma de la page 7.
L’hystérosalpingographie
Cet examen se fait juste après les règles. Les saignements doivent être terminés pour éviter de fausses images liées à la présence de caillots, et l’examen doit être réalisé suffisamment tôt au cours du cycle pour que la femme ne soit pas, par une fâcheuse coïncidence, enceinte lors de sa réalisation.
Le gynécologue, ou le radiologue, met en place, dans le col de l’utérus, une canule reliée à la seringue qui contient le produit de contraste. La prise de clichés au fur et à mesure de l’injection permet de visualiser l’écoulement du liquide, et donc la perméabilité des organes concernés. Au-delà du simple diagnostic de perméabilité, les images obtenues permettent d’accéder à certains diagnostics qui peuvent avoir de l’importance pour la suite de la prise en charge du couple.
L’hystérosalpingographie, essentiellement en raison de l’injection du produit de contraste, est perçue comme un examen désagréable. Il doit théoriquement ne pas être douloureux. La douleur est le fait d’une anomalie d’écoulement que certains médecins essayent de vaincre en exagérant la pression d’injection. Or, une anomalie d’écoulement est peut-être le signe d’une pathologie qui nécessitera autre chose que la simple hystérosalpingographie pour un diagnostic précis. Il est donc inutile de pousser les choses au-delà du seuil raisonnable de tolérance.
Enfin, il arrive dans de rares cas que l’hystérosalpingographie puisse réveiller un foyer inflammatoire pelvien. Le risque est plus élevé quand la patiente a un antécédent d’infection des trompes, qu’elle a eu un ou plusieurs épisodes de salpingite, ou encore, même si elle n’a pas d’antécédent notable, qu’elle est à risque d’être porteuse de germes transmis sexuellement en raison de la multiplicité de ses partenaires ou de la rencontre récente d’un nouveau partenaire (voir chapitre 6). C’est pourquoi la réalisation de l’hystérographie s’accompagne de la prise préventive d’un antibiotique.
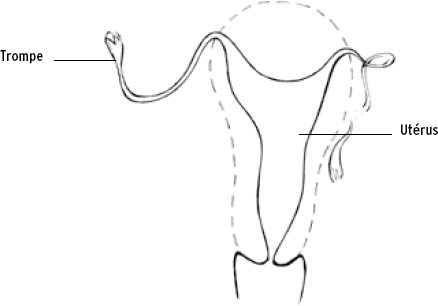
Hystérographie montrant l’utérus avec une anomalie sur la trompe droite
La fonction d’implantation
L’embryon formé grâce à la réunion de l’ovocyte et du spermatozoïde doit encore s’implanter dans l’utérus maternel pour que la grossesse puisse se développer. Cette phase est reconnue comme étant la plus mystérieuse et la moins accessible aux examens complémentaires. Si la grossesse commence, il est facile d’en déduire que l’implantation a bien eu lieu. Mais, dans le cas contraire, on ne sait pas bien ce qui s’est passé. Ici, encore plus que pour les autres fonctions, le médecin va extrapoler selon que l’utérus est normal ou non. Si l’utérus est normal, la fonction d’implantation est probablement satisfaisante.
S’il est anormal (fibrome, malformation, endométriose…), l’embryon a statistiquement moins de chances de s’implanter convenablement.
L’utérus s’examine à l’aide des mêmes examens complémentaires, échographie et hystérographie, que ceux qui explorent la perméabilité de la filière génitale féminine. L’évaluation de cette dernière fonction ne vient donc pas alourdir le fardeau des explorations à réaliser.
Les résultats du bilan initial
Au terme de ce bilan initial, il est habituellement possible de savoir quelle est la cause probable pour laquelle le couple n’a pas réussi jusqu’ici à obtenir de grossesse. Les causes d’infécondité peuvent être classées de la façon suivante :
 Infécondité par anomalie de l’ovulation : absence ou irrégularité des cycles génitaux, courbe de température plate, absence de progestérone en deuxième partie de cycle. En revanche, spermogramme, échographie et hystérographie sont normaux.
Infécondité par anomalie de l’ovulation : absence ou irrégularité des cycles génitaux, courbe de température plate, absence de progestérone en deuxième partie de cycle. En revanche, spermogramme, échographie et hystérographie sont normaux.
 Infécondité de cause masculine : le spermogramme avec peu de spermatozoïdes, à faible mobilité, de formes anormales (oligoasthéno-tératospermie), voire absents. En revanche, l’ovulation et la morphologie de la filière génitale féminine sont normales.
Infécondité de cause masculine : le spermogramme avec peu de spermatozoïdes, à faible mobilité, de formes anormales (oligoasthéno-tératospermie), voire absents. En revanche, l’ovulation et la morphologie de la filière génitale féminine sont normales.
 Infécondité mécanique, le plus souvent par imperméabilité tubaire : les trompes sont bouchées. L’hystérographie est anormale alors que le spermogramme et l’évaluation de l’ovulation sont normaux.
Infécondité mécanique, le plus souvent par imperméabilité tubaire : les trompes sont bouchées. L’hystérographie est anormale alors que le spermogramme et l’évaluation de l’ovulation sont normaux.
 Infécondité de cause utérine : fibrome, malformations, endométriose interne déformant l’utérus : la fonction d’implantation peut être atteinte.
Infécondité de cause utérine : fibrome, malformations, endométriose interne déformant l’utérus : la fonction d’implantation peut être atteinte.
Il arrive cependant que tout soit normal. C’est paradoxalement la situation la plus stressante pour le couple qui ne comprend pas ce qui se passe et pourquoi la grossesse ne s’installe pas. On parle d’infécondité inexpliquée. Sur le plan pronostique cependant, la situation est loin d’être désespérée parce que, d’une part, il y a toujours une chance que la grossesse survienne spontanément (puisque, apparemment, « tout marche ») et que, d’autre part, grâce aux techniques d’aide médicale à la procréation, il y a des thérapeutiques efficaces à proposer.
Établir la stratégie quand la grossesse se fait attendre
L’objectif est fixé : que la grossesse puisse s’installer pour donner naissance à l’enfant tant désiré. Le diagnostic est posé. Il faut maintenant examiner la stratégie qui, en tenant compte de la multiplicité des facteurs qui peuvent intervenir, permettra de maximaliser les chances d’aboutir à l’objectif. Pour ce faire, il faut garder la tête sur les épaules et ne pas risquer de confondre vitesse et précipitation. Il ne faut pas oublier non plus que la meilleure technique n’est pas forcément celle qui a la réputation de donner les meilleurs résultats statistiques. C’est celle qui va être la mieux adaptée au cas individuel du couple.
Le médecin doit faire sa part : être très professionnel, ne rien laisser au hasard, expliquer, beaucoup, rassurer, mais aussi dire la vérité. Elle est parfois difficile à entendre, mais la vérité exposée vaut toujours mieux que la vérité cachée. Le couple la découvrira inéluctablement et la souffrance n’en sera que plus vive.
Le couple aussi doit faire sa part : écouter, faire l’effort de comprendre, poser toutes les questions nécessaires et dire son opinion, son désir et sa volonté. Mais ne rien exiger. La pression exercée sur le médecin, volontairement ou non, peut conduire à des erreurs de stratégie qui peuvent diminuer les chances d’aboutir à l’objectif recherché.
La première action à entreprendre est l’élimination des toxiques, en particulier du tabac qui agit négativement par toute une série de mécanismes. Certes, être fumeur n’est pas en soi une cause de stérilité, mais le fait d’être fumeur, ou surtout fumeuse, diminue significativement les chances d’être enceinte. Le sevrage tabagique total des deux membres du couple doit donc débuter sans attendre, dès les premières consultations. En fécondation in vitro (FIV), les femmes fumeuses ont des taux de succès moindres : diminution du nombre d’ovocytes recueillis, diminution du taux de fécondation, altération de la qualité embryonnaire, diminution des taux d’implantation et des taux de grossesse. Et puis l’enfant une fois né, il est mieux pour lui de ne pas respirer la fumée de ses parents !
Outre le tabac qui mérite une place à part en raison de sa fréquence, de sa nocivité sur la fertilité et surtout de la possibilité d’arrêter son addiction pour peu que le couple décide de s’imposer une nouvelle hygiène de vie, de nombreux paramètres doivent être intégrés dans la réflexion sur la stratégie.
La baisse régulière de la fécondité de la femme avec l’âge est un phénomène bien connu. Ce qui l’est moins, c’est l’intensité et la précocité de cette baisse. À 35 ans, on estime que la femme a déjà perdu la moitié du potentiel qu’elle avait quelques années auparavant. À 40 ans, il n’en reste plus que le quart et le phénomène s’accélère au cours des années suivantes. À l’âge de 43 ans, les chances d’être enceinte deviennent quasi nulles, mises à part les quelques grossesses ponctuelles que chacun a connu dans son entourage et qui, bien souvent, sont une surprise alors que le couple pensait en avoir terminé avec la fécondité. Une recommandation forte rédigée par le Collège national des gynécologues et obstétriciens français (CNGOF) indique qu’il n’y a pas lieu de prendre en charge une infécondité, ni sur le plan diagnostique ni sur le plan thérapeutique, chez un couple dont la femme a atteint ou dépassé l’anniversaire de ses 43 ans. L’assurance maladie ne rembourse les soins ayant trait à l’infécondité que jusqu’à cet âge.
L’incidence de l’âge sur la fertilité est telle que les résultats de toutes les thérapeutiques doivent être révisés à la baisse lorsque l’âge de la femme augmente. C’est la raison pour laquelle l’âge doit conduire à accélérer les procédures de prise en charge médicale et à limiter le choix stratégique aux techniques dont les chances statistiques de réussite sont les meilleures. L’âge de l’homme intervient lui aussi négativement, bien que de façon moins précoce et moins brutale que chez la femme. Il n’y a pas de seuil aussi marqué que chez sa conjointe. On estime cependant que la limite se situe aux alentours de 63 ans.
Plus l’infécondité est ancienne et plus il y a eu de traitements tentés en vain, plus le pronostic est réservé. De nombreux autres paramètres tels que les antécédents éventuels de grossesses, la présence d’enfants à la maison, la recomposition d’un nouveau couple, l’existence éventuelle de pathologies (hypertension artérielle, diabète…) qui risquent d’altérer la santé et viennent compliquer la réalisation des traitements… doivent être pris en compte pour que le choix thérapeutique soit le plus pertinent possible, en maximalisant les chances de résultat tout en minimisant le plus possible les risques encourus. La stratégie de prise en charge n’est donc pas univoque et ne dépend pas seulement de l’anomalie diagnostiquée comme pouvant être la cause de l’infécondité.
L’infécondité par anomalie de l’ovulation
Dans un premier temps, il faut découvrir le pourquoi de l’anomalie de l’ovulation. Le médecin fera ce diagnostic à partir d’un bilan hormonal et de l’échographie des ovaires. En fonction du type d’anomalie de l’ovulation, il prescrira un traitement d’induction de l’ovulation qui consiste à stimuler l’ovulation en se rapprochant le plus possible de ce qui se produit lors de l’ovulation normale.
Les causes d’anomalie de l’ovulation
 Le syndrome des ovaires polykystiques.
Le syndrome des ovaires polykystiques.
 La déficience ovarienne prématurée ou ménopause précoce.
La déficience ovarienne prématurée ou ménopause précoce.
 Les insuffisances hypophysaires (maladie de l’hypophyse, adénome à prolactine).
Les insuffisances hypophysaires (maladie de l’hypophyse, adénome à prolactine).
 Les insuffisances hypothalamiques (notamment en cas d’antécédent d’anorexie).
Les insuffisances hypothalamiques (notamment en cas d’antécédent d’anorexie).
Il arrive aussi qu’une anomalie transitoire soit provoquée par un choc émotionnel, ce qui montre l’influence involontaire du cortex cérébral sur un certain nombre de fonctions, notamment celle de l’ovulation !
La femme n’ovule qu’un seul ovocyte fécondable par cycle, ce qui doit, on l’espère, permettre d’obtenir une grossesse monofœtale. C’est pourquoi un traitement par induction de l’ovulation est toujours entrepris de façon très progressive et prudente tant dans le choix des médicaments que des doses prescrites. On commence habituellement avec des médicaments dits de « premier degré » ou de « première intention » qui se prennent par voie orale et comportent un risque limité de grossesse multiple.
En cas d’efficacité insuffisante, on passe au « deuxième degré », avec des produits injectables qui nécessitent un suivi attentif tout au long du cycle, appelé « monitorage ». Il se fait à l’aide de dosages hormonaux (prise de sang), souvent quotidiens, et d’échographies. Le but est de vérifier que la croissance folliculaire a lieu, pouvant aboutir à l’ovulation, mais aussi qu’il n’y a pas un trop grand nombre de follicules en évolution, ce qui risquerait de mener à une grossesse multiple ou à un syndrome d’hyperstimulation.
L’induction de l’ovulation n’est proposée que si le recours à l’assistance médicale à la procréation n’est théoriquement pas indiqué. L’AMP (inséminations, FIV, ICSI) peut cependant être envisagée en cas de difficultés particulières pour faire ovuler convenablement la patiente, ou en cas de persistance de l’infécondité malgré une bonne correction apparente de l’anomalie ovulatoire au cours de 6 cycles de traitement.
L’infécondité de cause tubaire (trompes)
Lorsque l’hystérographie ne démontre pas une perméabilité satisfaisante de la filière génitale féminine (des trompes), il faut réaliser une cœlioscopie. Cet examen de l’abdomen et du pelvis de la femme à l’aide d’une optique munie d’une mini-caméra qui pénètre par le nombril se fait bien entendu sous anesthésie générale (voir chapitre 8). Il s’agit d’une chirurgie « ambulatoire » et l’hospitalisation est le plus souvent limitée à la journée. Cet examen est indispensable parce qu’il est le seul qui puisse confirmer la présence ou non d’un obstacle mécanique, et évaluer les possibilités de le supprimer. Lorsqu’une anomalie est confirmée et qu’elle est opérable, le geste chirurgical a lieu immédiatement. La cœlioscopie a donc un double but, diagnostique et thérapeutique.
Il arrive que certaines lésions soient inopérables en raison de l’extension des dégâts sur la trompe. Dans ce cas, le seul recours étant la fécondation in vitro, le chirurgien peut être amené à proposer à la patiente l’ablation des trompes afin de supprimer des trompes malades souvent pleines de liquide inflammatoire qui peut nuire, en s’écoulant dans l’utérus, à l’implantation de l’embryon obtenu en fécondation in vitro.
La fécondation in vitro est donc un recours fréquent en cas d’infécondité de cause tubaire, soit d’emblée lorsqu’il n’y a pas d’autre option thérapeutique, soit secondairement si la chirurgie réparatrice des trompes n’a pas permis d’obtenir la grossesse espérée.
L’infécondité de cause utérine
C’est le diagnostic retenu lorsque l’examen clinique, l’échographie, ou encore l’hystérographie, démontrent l’existence d’une anomalie de la cavité utérine qui pourrait gêner l’implantation de l’embryon.
Ici, c’est une hystéroscopie qu’il convient de pratiquer. Grâce à l’introduction d’un appareil optique (hystéroscope) par les voies naturelles, vagin puis canal cervical, il est possible de visualiser l’intérieur de la cavité utérine, et d’en examiner les contours et le relief muqueux (voir chapitre 8). L’hystéroscopie est à l’infécondité utérine ce que la cœlioscopie est à l’infécondité tubaire. Elle permet de confirmer l’existence ou non de lésions, d’en évaluer le caractère curable ou non, et même, dans certains cas, de réaliser le geste opératoire qui pourrait améliorer la fonction d’implantation comme l’ablation d’un polype, d’un fibrome, d’une cloison utérine.
FAQ
Une assistance médicale à la procréation est-elle possible en cas d’infécondité de cause utérine ?
Théoriquement non, car si l’embryon n’arrive pas à s’implanter en passant par les voies naturelles, il n’y a guère de raisons qu’il s’implante mieux sous prétexte qu’on l’injecte directement dans la cavité utérine. Certains spécialistes pensent cependant que, avec la fécondation in vitro qui permet de réaliser des transferts embryonnaires multiples (plusieurs embryons à la fois), le nombre pourrait venir compenser le défaut statistique de l’implantation. Ce raisonnement a cependant ses limites, et la stérilité de cause utérine, en cas d’absence de résultat obtenu par la chirurgie, fait partie des causes de stérilité définitives, non curables.
Le cas particulier de l’endométriose
L’endométriose est une affection curieuse très fréquente : il s’agit de l’implantation, dans l’abdomen de la patiente, d’îlots de muqueuse utérine qui réagissent, comme la muqueuse utérine normale, aux influences hormonales, notamment en sécrétant des règles (voir page 194). Petit à petit, les sortes de kystes sanguins qui se forment provoquent une réaction inflammatoire de défense de l’organisme qui tente de les résorber. Une nouvelle menstruation se produisant à chaque cycle, l’endométriose peut quand même avoir tendance à se développer. Ces implants d’endométriose peuvent être la cause de douleurs, notamment lors des règles. Mais heureusement c’est loin d’être toujours le cas. De la même façon, ils peuvent gêner la fonction de reproduction en intervenant négativement à plusieurs niveaux : ovaires, trompes, utérus. Le médecin propose d’effectuer une cœlioscopie à la recherche d’une endométriose s’il y a des signes d’appel. Mais, même en l’absence de signes d’appel, en cas de normalité du bilan initial (infécondité inexpliquée), il peut proposer une cœlioscopie car l’endométriose peut n’engendrer aucun signe clinique particulier.
L’endométriose peut se traiter médicalement, en supprimant les règles, ce qui évite la recontamination de l’abdomen par du sang menstruel qui pourrait refluer par les trompes et permet à l’organisme de faire cicatriser les îlots de muqueuse présents. Mais, dans le contexte de désir de grossesse, ce temps prolongé de cicatrisation voit son intérêt limité par le temps qui passe. C’est pourquoi l’endométriose découverte dans un contexte d’infécondité conjugale est essentiellement traitée chirurgicalement, par cœlioscopie. Il est en effet démontré que le traitement chirurgical de l’endométriose permet d’espérer le doublement des chances de grossesse dans les mois qui suivent. L’assistance médicale à la procréation est utile en deuxième recours si la grossesse n’est pas obtenue rapidement.
L’infécondité de cause masculine
Un médecin andrologue recherche la cause de l’anomalie spermatique chez le conjoint. En plus de l’analyse du sperme, il pourra prescrire des examens d’imagerie (échographie des testicules, de la prostate), des prélèvements bactériologiques dans le sperme ou encore des dosages hormonaux (prise de sang). Dans de rares cas, et toujours en coordination avec un centre d’assistance médicale à la procréation, le médecin sera amené à proposer une biopsie testiculaire, pour voir si l’on peut trouver des spermatozoïdes dans le testicule ou s’il n’en fabrique pas.
Les causes curables d’anomalie spermatique sont peu nombreuses. Les tentatives de traitement sont souvent décevantes. C’est pour cela que l’infécondité de cause masculine a pendant longtemps été considérée comme la plus difficile à traiter, celle dont le pronostic est le plus réservé. La pratique de l’assistance médicale à la procréation, en particulier l’injection de spermatozoïdes dans l’ovule ou ICSI (Intra Cytoplasmic Sperm Injection), qui n’a besoin que d’un très faible nombre de spermatozoïdes mobiles pour pouvoir être pratiquée, a provoqué une révolution. Ce n’est qu’en cas d’insuffisance spermatique extrême, quasi-azoospermie, ou en l’absence totale de spermatozoïdes que l’ICSI pourrait ne pas être possible et que le recours à un sperme de donneur serait éventuellement proposé.
L’infécondité inexpliquée
Le bilan de fertilité ne peut pas tout explorer. Il n’est qu’une évaluation somme toute assez grossière de certaines fonctions indispensables à la procréation, mais il est très loin de pouvoir explorer en détail l’ensemble du processus. C’est pourquoi un bilan chez les deux membres du couple peut, apparemment, être normal.
Dans ce type de situation, il est logique d’aller jusqu’au bout des explorations en pratiquant chez la femme une cœlioscopie et une hystéroscopie. Ces examens permettent de faire un diagnostic utile dans environ la moitié des cas. Par ailleurs, s’ils sont normaux, ils confirment qu’il est possible de pratiquer une technique d’assistance médicale à la procréation, insémination ou fécondation in vitro, avec une chance raisonnable de réussite.
Il est possible de proposer au couple, selon son cas particulier, de tenter quelques cycles d’insémination avant de faire ces explorations complémentaires. Mais, en cas d’échec, il faut savoir ne pas insister et aller d’abord jusqu’au bout du bilan.
L’assistance médicale à la procréation (AMP)
L’AMP a pris une place majeure dans l’arsenal thérapeutique de la lutte contre l’infécondité conjugale. Elle s’applique en effet à divers types de causes d’infécondité et ses résultats sont parfois spectaculaires. Elle regroupe l’ensemble des techniques médicobiologiques qui font intervenir la manipulation de l’un ou des deux gamètes (ovocytes/spermatozoïdes). Il n’est pas toujours nécessaire que la fécondation ait lieu in vitro. Par exemple, l’insémination est une technique d’AMP puisqu’elle comporte la manipulation des gamètes masculins (spermatozoïdes) injectés directement dans l’utérus de la conjointe (après préparation biologique), la fécondation ayant lieu (on l’espère !) in vivo. Les techniques d’AMP recouvrent donc :
 les inséminations avec sperme du conjoint (IAC) ou avec sperme d’un donneur (IAD) ;
les inséminations avec sperme du conjoint (IAC) ou avec sperme d’un donneur (IAD) ;
 la fécondation in vitro, dite FIVETE (fécondation in vitro et transfert d’embryons) ;
la fécondation in vitro, dite FIVETE (fécondation in vitro et transfert d’embryons) ;
 l’ICSI (intra cytoplasmic sperm injection) qui n’est autre qu’une fécondation in vitro au cours de laquelle le spermatozoïde est injecté directement dans l’ovocyte. Cette technique est utilisée quand le sperme est trop déficient ou dans certains cas qui nécessitent le contrôle du processus de fécondation.
l’ICSI (intra cytoplasmic sperm injection) qui n’est autre qu’une fécondation in vitro au cours de laquelle le spermatozoïde est injecté directement dans l’ovocyte. Cette technique est utilisée quand le sperme est trop déficient ou dans certains cas qui nécessitent le contrôle du processus de fécondation.
Une technique bien rodée
En France, chaque année, près de 25 000 enfants naissent grâce à l’AMP, ce qui représente un peu plus de 3 % des naissances. Il est loin derrière nous le temps où l’on s’interrogeait sur la « normalité » des enfants issus de l’assistance médicale à la procréation.
Ces techniques d’AMP sont essentiellement destinées à permettre aux couples qui n’arrivent pas à concevoir naturellement d’obtenir la grossesse désirée. Dans certains cas, l’AMP est indiquée chez des couples qui n’ont pas de problème de fécondité, mais qui risqueraient de donner naissance à un enfant atteint d’une maladie génétique grave et incurable. En effet, la possibilité d’analyser l’embryon avant son transfert dans l’utérus maternel (diagnostic pré-implantatoire, DPI) permet de sélectionner les embryons non porteurs de l’anomalie génétique et d’éviter au couple l’angoisse de donner naissance à un enfant très gravement malade, ou d’avoir à procéder à une interruption médicale de grossesse.
Les erreurs à éviter
 Vouloir avoir recours d’emblée à l’AMP sans prendre le temps de rechercher la cause de l’infécondité.
Vouloir avoir recours d’emblée à l’AMP sans prendre le temps de rechercher la cause de l’infécondité.
 Court-circuiter les étapes en faisant reposer tous les espoirs sur une seule méthode. Aussi performante soit-elle, elle n’obtiendra jamais ce que l’ensemble des prises en charge possibles permettent d’obtenir en additionnant leur potentiel.
Court-circuiter les étapes en faisant reposer tous les espoirs sur une seule méthode. Aussi performante soit-elle, elle n’obtiendra jamais ce que l’ensemble des prises en charge possibles permettent d’obtenir en additionnant leur potentiel.
 Ne compter que sur la médecine : le couple a aussi sa part de chemin à faire, notamment en cas de tabagisme.
Ne compter que sur la médecine : le couple a aussi sa part de chemin à faire, notamment en cas de tabagisme.
 Laisser passer le temps : c’est le principal ennemi du couple infécond. il faut agir tant qu’il est « encore » temps !
Laisser passer le temps : c’est le principal ennemi du couple infécond. il faut agir tant qu’il est « encore » temps !
Le déroulement d’un cycle d’AMP
LA PRÉPARATION DE L’OVULATION
Le « bilan pré-AMP » réunit des renseignements complémentaires du bilan d’infertilité, d’ordre technique, qui vont permettre d’adapter l’AMP au cas individuel de la patiente. Il faut connaître le niveau de la réserve ovarienne (ce qui va permettre d’adapter l’intensité de la stimulation de l’ovulation), avoir une spermoculture récente, un test de préparation-migration du sperme (ce qui est important pour choisir le type d’AMP possible et adapter la façon dont le sperme doit être préparé). Il faut encore faire pratiquer un ensemble de sérologies (prises de sang) afin de dépister l’homme ou la femme porteurs de virus qui pourraient induire un risque pour le personnel de santé et nécessiteraient une prise en charge adaptée. Enfin, un « test de transfert » vérifie qu’il y a un accès facile à la cavité utérine par le col utérin. Lors d’une consultation, le médecin introduit le même type de cathéter que celui qui servira à faire une insémination intrautérine ou un transfert embryonnaire, ce qui a en outre l’intérêt de montrer à la patiente que le geste est parfaitement indolore. Elle pourra de ce fait être plus détendue le jour venu.
Tabagisme
Certains centres exigent un sevrage tabagique absolu avant de débuter un cycle d’AMP, la réalité du sevrage étant vérifiée à l’aide d’un capteur d’oxyde de carbone.
Le couple, dont l’indication de recours à l’AMP a été retenue avec le gynécologue, doit rencontrer le biologiste. Ce dernier engage lui aussi sa responsabilité et il demande logiquement à connaître le couple. Un certain nombre de processus biologiques sur lesquels le couple a un avis à donner doivent être discutés au préalable, par exemple le nombre d’embryons qui seront transférés et l’éventualité du recours à une congélation embryonnaire.
Médecin clinicien et biologiste se retrouvent autour d’une table (réunion clinico-biologique ou « staff ») pour revoir ensemble une ultime fois le dossier médical des patients et préciser ensemble un certain nombre de points organisationnels et techniques.
La patiente débute ensuite son traitement de stimulation de l’ovulation. Divers protocoles sont prescrits en fonction des caractéristiques individuelles de la patiente (âge, indice de masse corporelle, données sur la réserve ovarienne, antécédents de chirurgie ou de kystes sur les ovaires, cause du recours à l’AMP, etc.). Le traitement consiste en une série d’injections que la patiente peut le plus souvent réaliser elle-même à l’aide d’un stylo injecteur.
Au bout d’un certain nombre de jours, la surveillance par échographie des ovaires (monitorage) permettra de vérifier le nombre de follicules dont la croissance a été stimulée et leur degré d’avancement. Il faut en effet conclure ce traitement de stimulation de l’ovulation, par une injection de « déclenchement » qui permet d’induire la maturation finale des follicules et des ovocytes, et de programmer l’ovulation de la patiente.
L’INSÉMINATION
Si c’est une insémination qui est pratiquée, le couple est convoqué peu avant l’ovulation de façon à ce que le conjoint prélève son sperme au laboratoire. Après une préparation biologique qui dure deux heures, une fraction du sperme préparé, sélectionnée pour contenir les spermatozoïdes les plus mobiles et les plus normaux, est injectée dans l’utérus de la patiente. Ceci clôt la procédure. Il ne reste plus qu’à attendre le résultat qui ne pourra être connu que dans quinze jours.
LA FÉCONDATION IN VITRO ET L’ICSI
Si c’est une fécondation in vitro, les follicules (qui contiennent les ovocytes) doivent être récupérés par aspiration. La patiente est donc hospitalisée (en ambulatoire) et l’aspiration folliculaire a lieu au bloc opératoire par l’introduction de l’aiguille de ponction ovarienne par voie vaginale sous contrôle échographique. Anatomiquement, les ovaires sont en effet situés à proximité du fond du vagin.
Cette ponction a lieu sous simple anesthésie locale associée à une analgésie assurée par un anesthésiste, mais à la demande de la patiente, elle peut avoir lieu sous anesthésie générale ou parfois sous anesthésie péridurale.

Ponction ovarienne par voie vaginale
Une fois cette ponction réalisée, les liquides folliculaires, maintenus à une température de 37 °C, sont immédiatement préparés par le biologiste afin d’isoler les ovocytes et de les placer en culture. Après prélèvement du sperme du conjoint et préparation biologique, les ovocytes sont inséminés et replacés en culture.

Fécondation in vitro
Si c’est une ICSI qui est pratiquée, le biologiste injecte directement un spermatozoïde dans chaque ovocyte.
S’ensuit une phase de culture d’environ 3 jours au cours desquels la fécondation et les premières divisions embryonnaires se produisent.
Au bout de ce laps de temps, les embryons dont l’apparence est la plus normale (en nombre et en régularité des cellules) sont transférés dans l’utérus maternel. Le nombre d’embryons transférés est soigneusement calibré en fonction des chances d’implantation. Il faut optimiser les chances d’obtenir une grossesse et éviter autant que possible une grossesse multiple qui pourrait poser des problèmes obstétricaux parfois gravissimes. En raison de l’amélioration constante des performances de la fécondation in vitro et de la congélation embryonnaire, et du risque que ferait courir une grossesse multiple aux enfants à naître, c’est de plus en plus souvent un transfert électif d’un seul embryon qui est proposé au couple. Les autres embryons, en position surnuméraire, sont mis en réserve par congélation ultrarapide (vitrification) si leur qualité laisse l’espoir qu’ils puissent eux aussi conduire à une éventuelle grossesse.
Après le transfert embryonnaire dans l’utérus, la période qui suit est une phase d’incertitude, qui se conclura au bout de quinze jours par l’apparition des règles, ce qui signerait l’échec, ou par un test de grossesse positif, résultat tant espéré.
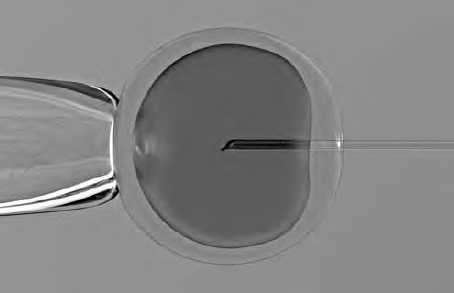
Injection intracytoplasmique d’un spermatozoïde
Les résultats de l’AMP
Les résultats s’expriment en pourcentage de cycles qui conduisent à une grossesse. Il faudrait, pour être rigoureux, les exprimer en pourcentage de cycles qui conduisent à une grossesse évolutive permettant la naissance d’un enfant en bonne santé, parce que c’est cela l’objectif poursuivi. Un certain nombre d’implantations embryonnaires donnent en effet lieu à un test de grossesse positif, mais malheureusement sans lendemain, l’embryon implanté arrêtant rapidement son développement. La patiente a des règles comme s’il n’y avait pas eu d’implantation. On parle de « grossesse biochimique » ou « d’avortement pré-clinique ».
À la suite d’une AMP, comme c’est le cas pour toute grossesse quelle que soit la façon dont elle a été obtenue, il y a aussi le risque d’avortement spontané (fausse couche) qui, en dehors des pathologies maternelles éventuelles et des anomalies de l’utérus, est le plus souvent lié à la qualité de l’œuf, l’avortement précoce étant alors considéré comme un « tri naturel » afin de ne laisser évoluer que les grossesses normales. Le risque de fausse couche est grandement augmenté par l’âge de la patiente et un éventuel tabagisme.
Les résultats de l’AMP varient beaucoup en fonction d’un grand nombre de paramètres pronostiques : l’âge des conjoints, la cause de l’infécondité, les éventuels échecs thérapeutiques déjà constatés, la manière dont les ovaires ont répondu à la stimulation de l’ovulation, etc. Il y a probablement aussi des résultats différents d’un centre à un autre, mais ils sont très difficiles à apprécier d’un point de vue statistique parce qu’ils dépendent tout autant du type de patientes qui y sont traitées que de la qualité technique du centre en question. Les meilleurs centres ne sont pas toujours ceux qui affichent les meilleurs résultats, mais souvent ceux qui s’occupent le mieux de leurs patientes et qui vont jusqu’au bout d’une démarche avec sérieux et ténacité, même si, parfois, les résultats statistiques peuvent avoir à en souffrir.
Pour donner un ordre de grandeur, les inséminations donnent entre 15 et 20 % de chances de grossesse par cycle de traitement, et la fécondation in vitro (ou l’ICSI) aux alentours de 30 % par tentative.
FAQ
Est-il vrai qu’il faut faire une première tentative pour se régler et que les résultats sont meilleurs lors d’une deuxième tentative ?
C’est parfaitement faux. Les résultats vont au contraire en diminuant au fur et à mesure des tentatives, toujours pour la même raison. Si un couple a un pronostic favorable, il obtiendra plus facilement la grossesse dès la première tentative. Si le pronostic est moins bon, il y a des risques que la grossesse soit obtenue avec plus de difficultés. Les couples dont le pronostic peuvent effectuer plus souvent une deuxième ou une troisième tentative.
Après un échec, il faut, avant de faire une nouvelle tentative, examiner les raisons qui ont pu conduire à l’échec afin de les corriger si possible. Il faut s’interroger sur la légitimité de faire une nouvelle tentative qui conduirait, logiquement, au même échec que la précédente, si la cause de l’échec initial n’a pas été corrigée. Les résultats de l’AMP ne sont en effet pas une loterie, même si, effectivement, il y aussi une part d’inconnu qui ne peut pas être maîtrisée et pour laquelle il faut s’en remettre au destin…
FAQ
Quand doit-on réfléchir à l’usage de gamètes de donneur ?
Il arrive que les chances d’obtenir une grossesse soient nulles, par exemple quand ce sont les gamètes eux-mêmes (spermatozoïde chez l’homme, ovocyte chez la femme) qui font défaut. Le diagnostic est souvent porté d’emblée quand la pathologie est connue parce qu’elle s’est déjà exprimée cliniquement. Mais il arrive que le diagnostic ne soit porté qu’à la suite des échecs répétés des traitements. C’est l’analyse attentive des raisons de ces échecs et l’examen des chances pronostiques qui conduisent à faire envisager le recours à un don de sperme ou un don d’ovocytes.
Quand faut-il arrêter tout traitement ?
• Quand la cause de l’infécondité est non curable, par exemple une anomalie majeure de l’utérus. Le caractère curable ou non est affaire de cas particuliers et c’est avec son médecin qu’il convient d’en discuter.
• Quand tout a échoué, y compris les tentatives d’assistance médicale à la procréation. L’assurance maladie prend en charge jusqu’à 6 cycles d’insémination et 4 cycles de fécondation in vitro. Cela ne veut cependant pas dire qu’il faut aller jusqu’au bout de ces tentatives. Chaque tentative réalisée doit faire l’objet d’une discussion avec son médecin afin de déterminer si c’est justifié ou non d’en faire une autre.
• Quand la femme atteint l’âge de 43 ans ou l’homme celui de 63 ans.
• Quand le pronostic est trop réservé. Dans ce cas, la balance bénéfices/risques (les bénéfices sont les chances d’obtenir enfin la grossesse désirée ; les risques sont les risques médicaux, auxquels il faut ajouter les perturbations de la vie quotidienne, les frais engendrés, les espoirs déçus…) devient négative. Il faut toujours demander à son médecin l’évaluation du pronostic, les éléments sur lesquels il se fonde pour donner cette estimation, et les risques médicaux à court, moyen, ou long terme, suivant le traitement proposé.
La congélation des ovocytes
La compréhension des processus qui contribuent à l’obtention d’une grossesse et la maîtrise chaque jour plus grande des techniques d’AMP ont conduit au concept de « préservation de la fertilité », initialement développé pour les patients atteints d’un cancer qui nécessitent le recours à des traitements potentiellement stérilisants (chimiothérapie, radiothérapie, chirurgie). Chez l’homme, la mise en réserve du sperme par congélation est pratiquée depuis longtemps. Chez la femme, la congélation des ovocytes a longtemps posé des problèmes techniques, aujourd’hui résolus. Mais sa pratique nécessite des ovaires matures (ce n’est pas possible avant la puberté), ainsi que la possibilité de subir un traitement de stimulation de l’ovulation et un prélèvement folliculaire, et si possible plusieurs pour qu’un nombre suffisant d’ovocytes puisse être mis en réserve.
Il existe deux types de préservations possibles de la fertilité avant traitement à risque d’infertilité :
 Faire une fécondation in vitro d’urgence avant de débuter une chimiothérapie (avec stimulation de l’ovulation et ponction des ovocytes), et congeler les embryons obtenus pour les utiliser quand la femme sera guérie de sa maladie. Encore faut-il que la femme soit en couple au moment où se déclare le cancer ou la maladie grave.
Faire une fécondation in vitro d’urgence avant de débuter une chimiothérapie (avec stimulation de l’ovulation et ponction des ovocytes), et congeler les embryons obtenus pour les utiliser quand la femme sera guérie de sa maladie. Encore faut-il que la femme soit en couple au moment où se déclare le cancer ou la maladie grave.
 Si elle est seule, on peut désormais aussi faire une induction pour prélever et congeler les ovocytes obtenus, la technique de congélation rapide (encore appelée vitrification) ayant été autorisée par la loi de bioéthique de 2011.
Si elle est seule, on peut désormais aussi faire une induction pour prélever et congeler les ovocytes obtenus, la technique de congélation rapide (encore appelée vitrification) ayant été autorisée par la loi de bioéthique de 2011.
 Il est aussi possible de prélever et de congeler du tissu ovarien et de le remettre en place quand la femme est guérie. Cette dernière possibilité est surtout intéressante pour les petites filles, non encore réglées. Grâce à cette technique, le nombre de grossesses obtenues dans le monde reste faible (moins de 20), la conservation ovocytaire ou embryonnaire est donc préférable chaque fois que cela est possible.
Il est aussi possible de prélever et de congeler du tissu ovarien et de le remettre en place quand la femme est guérie. Cette dernière possibilité est surtout intéressante pour les petites filles, non encore réglées. Grâce à cette technique, le nombre de grossesses obtenues dans le monde reste faible (moins de 20), la conservation ovocytaire ou embryonnaire est donc préférable chaque fois que cela est possible.
Par extension, on songe aujourd’hui à appliquer ces mêmes techniques à celles dont la fertilité est mise en danger en raison de leur âge. Le phénomène de retard de plus en plus marqué de l’âge du désir de grossesse, phénomène sociétal lié à de nombreuses causes non médicales, s’accompagne d’un risque accru d’infécondité définitive. La femme qui approcherait de l’âge de 36 ans sans avoir eu d’enfant serait tentée de préserver ses chances quelques années supplémentaires, en ayant recours à une congélation de ses ovocytes. Les problèmes que cela peut poser sont nombreux, mais la réflexion est lancée…
Plusieurs arguments plaident en faveur de l’autoconservation ovocytaire. Le désir d’enfant est de plus en plus tardif. Études, carrières féminines, hasards de la vie ne permettent pas toujours aux femmes de fonder une famille au moment où leur fertilité est optimale. Seul le don d’ovocytes peut compenser le vieillissement ovocytaire, aussi les candidates au don d’ovocytes sont-elles de plus en plus nombreuses, or il y a une pénurie réelle de don d’ovocytes en France. Congeler ses ovocytes avant qu’il ne soit trop tard (avant 35 à 38 ans) permettrait à une femme qui n’aurait pas pu procréer au moment où sa fertilité est optimale, d’utiliser ultérieurement ses ovocytes congelés. Néanmoins cette technique risque d’encourager encore plus les grossesses tardives dont les risques sont réels pour la mère (hypertension, diabète…) et pour l’enfant : enfant de petit poids, prématuré. Ces risques s’élèvent dès 40 ans et sont franchement majorés après 45 ans. De plus, la grossesse n’est pas garantie et cette possibilité risque de donner un faux espoir aux femmes qui, ayant leurs ovocytes au congélateur, penseraient pouvoir attendre sans souci…
Remarque
L’autoconservation ovocytaire de convenance n’est pas possible en France à l’heure où ces lignes sont écrites. Depuis quelques années, la conservation d’ovocytes est proposée dans certains pays (États-Unis, Espagne), aux femmes pour compenser l’horloge biologique (contre quelques milliers de dollars ou d’euros…).
 soit en raison de symptômes (douleurs du bas-ventre, pertes vaginales malodorantes ou non, démangeaisons (prurit), saignements en dehors des règles, règles hémorragiques, douleurs lors des rapports sexuels…). L’examen gynécologique permet le plus souvent d’en trouver l’origine ;
soit en raison de symptômes (douleurs du bas-ventre, pertes vaginales malodorantes ou non, démangeaisons (prurit), saignements en dehors des règles, règles hémorragiques, douleurs lors des rapports sexuels…). L’examen gynécologique permet le plus souvent d’en trouver l’origine ; soit régulièrement de façon préventive.
soit régulièrement de façon préventive.




 Le syndrome des ovaires polykystiques.
Le syndrome des ovaires polykystiques.

