46.5.3.3 Anpassung der Pflegemaßnahmen
Wenn Beschwerden auftreten oder zunehmen, müssen die pflegerischen Interventionen angepasst werden. Folgende Maßnahmen sollten dann geändert werden:
-
Mundspülhäufigkeit steigern (6 – 8-mal pro Tag)
-
bei der Mundspüllösung von Tee zu Stomatitislösung wechseln
-
Zähneputzen bei Blutungen unterlassen
-
Zahnprothese bei einer Stomatitis nur zum Essen und in der Öffentlichkeit tragen
-
Ernährung und Speisen an die Bedürfnisse des Patienten anpassen (Milchshakes, Pudding, Milchsuppen u. a.)
-
von enteraler auf parenterale Ernährung umstellen
-
gezielte Schmerzeinschätzung (gezielte Schmerzabfrage mittels Schmerzskala) und Schmerzmedikation (nach WHO-Stufenkonzept)
Merke
Das oberste Ziel ist, die enterale Nahrungs- und Flüssigkeitsaufnahme so lange wie möglich aufrechtzuerhalten, da Essen und Trinken zu den wichtigsten Reinigungsmechanismen des Mund- und Rachenraumes zählen.
Lebensphase Kind
Lars Wicher
Mukositis
Die Versorgung und Behandlung einer beginnenden oder ausgeprägten Mukositis (Entzündung der Mundschleimhaut) ist ohne die Hilfe der Eltern meist nur schwer möglich. Gerade Kleinkinder stehen den Maßnahmen teilweise ablehnend gegenüber, oft aus Angst vor dem Neuen oder einem unangenehmen Geschmack.
Anleitung und Beratung
Die Pflegenden beraten die Eltern bei der Wahl einer geeigneten Mundspüllösung und bieten Unterstützung bei der Durchführung der Mundpflege an. Die Kinder werden in die Beratung und Anleitung integriert. Dies erfordert eine altersgerechte Sprache und bei Klein- und Schulkindern einen spielerischen Umgang v.a. bei der Mundinspektion. Häufig wird dadurch die Bereitschaft des Kindes gestärkt, die Mundpflege zu tolerieren oder diese sogar selbst durchzuführen.
Mukositis lindern
Bei Säuglingen und Kleinkindern bietet es sich an, einen Stieltupfer mit einer Mundspüllösung zu tränken und die Mundschleimhaut damit zu pinseln (Rinner 2012). Für Schulkinder und Jugendliche können verschiedene Teesorten als Eiswürfel oder Eis am Stiel eingefroren werden. Sie werden meist sehr gut toleriert. Neben dem Effekt der Reinigung und Befeuchtung der Mundschleimhaut wirkt die Kälte schmerzlindernd. Inwieweit sich therapeutische Mundspüllösungen einfrieren lassen, sollte von den Pflegenden mit der Klinikapotheke abgesprochen werden.
Schmerzerfassung
Eine adäquate Schmerzerfassung im Rahmen der Mukositis ist gestaltet sich nicht immer leicht. Kinder sind erst ab dem 3.–4. Lebensjahr in der Lage, mittels einer altersgerechten Schmerzskala den Schmerz selbst einzuschätzen. Erst dann können sie zwischen vorhandenem Schmerz und Schmerzfreiheit unterscheiden und Schmerz mit einfachen Wörtern verbalisieren.
Säuglinge und Kleinkinder können erlebten Schmerz gar nicht verbalisieren. Sie geben durch eine Veränderung der Mimik und der Körperhaltung sowie durch vermehrtes Weinen und Unruhephasen erste Hinweise auf eine mögliche Schmerzsituation. Die Schmerzerfassung erfolgt hier nur über eine Fremdeinschätzung durch die Eltern und das behandelnde Team (Wagner et al. 2015). Dem behandelnden Team stehen dazu für jede Altersgruppe verschiedene Schmerzscores zur Verfügung ( ▶ Tab. 46.10 ).
|
Bezeichnung der Skala |
Kennzeichen |
|
Kindliche Unbehagens- und Schmerz-Skala (KUSS) |
|
|
Faces-Pain-Scale |
|
|
Numerische Rating-Skala (NRS) |
|
Merke: Eine Schmerzeinschätzung anhand der Faces-Pain-Scale fällt Kindern unter dem 6. Lebensjahr oft schwer und verhindert eine adäquate Schmerzeinstellung.
46.5.4 Therapiebedingte Diarrhö
Da nicht nur die Mundschleimhaut betroffen sein kann, sondern auch die (gastro)intestinale Schleimhaut, reagieren Patienten während einer medikamentösen Tumortherapie oder einer Strahlentherapie im Abdominal- und Beckenbereich häufig mit starken Durchfällen (Diarrhöen). Da auch hier die Epithelzellen und die Submukosa gleichermaßen betroffen sind, bilden sich Nekrosen und Ulzerationen. Die Folge dieses entzündlichen Prozesses sind Resorptionsstörungen, die dann zu starken Diarrhöen führen. Der Wasser- und Elektrolytverlust führt zu Symptomen und klinischen Befunden, die in ▶ Tab. 46.11 zusammengefasst sind.
|
Verlust von |
subjektive Symptome |
klinische/laborchemische Befunde |
|
Wasser |
|
|
|
Natrium |
|
|
|
Kalium |
|
|
|
Bikarbonat |
|
|
|
Kohlenhydrate/Proteine |
|
|
Wie schwer die Nebenwirkungen und Folgen für den Patienten sind, ist individuell sehr unterschiedlich. Neben der Chemo- oder Strahlentherapie spielt die patientenspezifische Prädisposition eine wichtige Rolle. Diarrhöen können die Befindlichkeit des Patienten erheblich beeinträchtigen, sodass sich zeitgerechte Therapien dadurch verzögern können.
46.5.4.1 Pflegemaßnahmen
Folgende pflegerische Interventionen bei Diarrhö sollten durchgeführt werden:
-
Informationen an Patienten und Angehörigen:
-
hinsichtlich des Auftretens einer Diarrhö
-
dass eine verzögerte Diarrhö bei Gabe des Zytostatikums Irinotecan nach 2 – 4 Tagen auftreten kann
-
über die Folgen und Auswirkungen einer Diarrhö
-
über Medikamente und Interventionen
-
-
gute Patientenbeobachtung:
-
Stuhlgang (Häufigkeit, Konsistenz, Farbe, Beimengungen, Volumen)
-
Schmerzen, Krämpfe
-
Zeitpunkt der Schmerzen
-
klinische Zeichen eines Volumenmangels
-
Zustand der Haut im Analbereich
-
ausreichende Flüssigkeits- und Elektrolytzufuhr
-
-
sorgfältige Analhygiene:
-
Vermeidung von Verletzungen
-
Wundprophylaxe mit fetthaltigen Salben
-
sanfte Pflege (weiches Toilettenpapier, pH-neutrale Seife)
-
Vorsicht mit Suppositorien
-
keine rektale Temperaturmessung
-
-
angepasste Ernährung:
-
leicht, fett-, milchzucker- und ballaststoffarm
-
kleine Mahlzeiten
-
Fencheltee, schwarzer Tee
-
Medikamentengabe nach Anordnung
-
46.5.5 Therapiebedingte Blutbildungsstörungen
Definition
Die Knochenmarkdepression (syn. Myelosuppression) ist die Schädigung des Knochenmarks, die mit der Verminderung aller zellulären Anteile der Blutbildung einhergeht. Eine Knochenmarkschädigung ist häufige Nebenwirkung von Zytostatika- und Radiotherapien. Bei sehr schwerer Schädigung im Rahmen einer Knochenmarktransplantation (KMT) oder peripheren Stammzelltransplantation (PBSZT) spricht man häufiger von der Knochenmarkaplasie als von der Knochenmarkdepression.
Die zytotoxischen Effekte der Zytostatika auf das Knochenmark (Myelotoxizität) führen zu einem raschen Abfall der zirkulierenden Blutzellen. Die Auswirkungen zytostatischer Therapien auf die Blutbildung (Myelopoese) hängen sehr stark vom Zytostatikum, der Kombination der Wirkstoffe, der Dosis und der Dauer der Behandlung ab.
Bei einer Hochdosistherapie liegen z. B. die Dosen der zellwachstumshemmenden Medikamente um das 3 – 10-fache über der üblichen Zytostatikadosierung. Das Ziel einer Hochdosistherapie ist, alle Tumorzellen im Körper komplett zu zerstören, was bei einigen Tumoren mit einer Dosissteigerung möglich wird. Eine Steigerung der Zytostatikadosis über den festgelegten Grenzwert ist aber nur dann möglich, wenn die Nebenwirkungen erfolgreich behandelt werden können. Im Falle der Myelotoxizität bedeutet dies, dass dem Patienten unmittelbar nach einer Hochdosistherapie gesunde Blutstammzellen übertragen werden (KMT, PBSZT), die die Blutbildung nach kurzer Zeit wieder in Gang setzen.
Ziel der Strahlentherapie ist die maximale Schädigung des Tumorgewebes durch ionisierende Strahlen bei gleichzeitig maximaler Schonung des umgebenden gesunden Gewebes. In bestrahlten Regionen mit Beteiligung des blutbildenden Gewebes kann es zu einer Verminderung der Blutzellen und bei entsprechender Dosis sogar zur Knochenmarkaplasie kommen. Die Ganzkörperbestrahlung (TBI engl.: total body irradiation) wird in manchen Fällen vor einer allogenen (Fremdspender) Knochenmarktransplantation durchgeführt. Das Ziel dieser Bestrahlungsmethode ist die Abtötung der i. A. sehr strahlenempfindlichen Leukämie- oder Lymphomzellen sowie die Zerstörung der Knochenmarkzellen und Zellen des Immunsystems (B- und T- Lymphozyten), um das Anwachsen der Fremdspenderzellen zu ermöglichen. Vergleichsweise sind bei einer Ganzkörperbestrahlung 100 % und bei einer Bestrahlung des Beckens 15 – 35 % des gesamten blutbildenden Knochenmarks betroffen.
Im Rahmen zytostatischer Chemotherapien kommt es relativ häufig zur Einschränkung der Knochenmarkfunktion und dadurch zu einer unterschiedlich ausgeprägten Beeinflussung des peripheren Blutbildes. Die Folgen sind:
-
Leukozytopenie
-
Thrombozytopenie
-
Anämie
46.5.5.1 Leukozytopenie
Definition
Leukozytopenie (syn. Leukopenie) bezeichnet eine Verminderung der Gesamtleukozytenzahl (Granulozyten, Lymphozyten, Monozyten) unter 4000/µl. Dieser Wert ist unabhängig von Alter und Geschlecht. Unterschieden werden:
-
Granulozytopenie (syn. Neutropenie): Verminderung der Granulozyten auf unter 1500/µl. Betroffen sind v. a. die neutrophilen Granulozyten, die den weitaus größten Anteil der Granulozyten ausmachen (die Neutropenie ist die häufigste Form der Leukozytopenie)
-
Agranulozytose: Leukozytopenie unter 1000/µl mit weitgehendem oder völligem Fehlen der Granulozyten im peripheren Blut
-
Lymphozytopenie: Verminderung der Lymphozyten unter 1000/µl im peripheren Blut bei Patienten mit Infektionskrankheiten, Morbus-Hodgkin-Lymphomen und bei fortgeschrittener HIV- Erkrankung
Zum besseren Verständnis sind in ▶ Tab. 46.12 die Normalwerte des Blutes aufgeführt.
|
Parameter |
Konventionelle Einheit |
|
Erythrozyten
|
|
|
Retikulozyten |
5 – 24 ‰ |
|
Thrombozyten |
150 000 – 400 000/µl |
|
Leukozyten |
4800 – 10 000/µl |
|
|
|
Lymphozyten |
25 – 40 % |
|
Monozyten |
2 – 8 % |
|
Hämoglobin (Hb)
|
|
|
Hämatokrit (HK)
|
|
Die Leukozytopenie ist i. d. R. die Folge einer Chemo- und/oder Radiotherapie. Sie kann aber auch durch den Tumor selbst bedingt sein (z. B. akute Leukämie, myeloplastisches Syndrom MDS, aplastisches Syndrom) oder in seltenen Fällen durch allergische oder toxische Reaktionen auf bestimmte Medikamente oder durch virale Infektionen ausgelöst werden.
Bei der Leukozytopenie können alle Leukozyten oder nur bestimmte Unterformen verringert sein. Sie kann isoliert oder in Kombination mit einer Anämie und/oder Thrombozytopenie auftreten.
Symptome und Komplikationen einer Infektion bei Neutropenie
Die neutrophilen Granulozyten sind Teil des unspezifischen Abwehrsystems und wichtig für die Abwehr von Infektionen. Da die Neutrophilen ca. zwei Drittel der Leukozyten ausmachen, steigt das Infektionsrisiko bei Granulozytenwerten unter 1000/µl merklich an. Das Infektionsrisiko hängt in erster Linie von der Schwere der Neutropenie ab. Für die therapeutischen und pflegerischen Maßnahmen spielen aber nicht nur die Granulozytenwerte, sondern auch die Dauer der Neutropenie, die Grunderkrankung, der Allgemeinzustand des Patienten sowie die Form der Behandlung (Hochdosistherapie, KMT) eine wichtige Rolle. Patienten mit einer länger als 10 Tage anhaltenden schweren Neutropenie (< 100 Neutrophile/µl) entwickeln in mehr als 80 % der Fälle Infektionen.
Merke
Das Risiko einer Infektion wird entscheidend durch das Ausmaß und die Dauer der Neutropenie bestimmt.
Klinische Symptome wie Müdigkeit, Schwäche und Schweißausbrüche können während der neutropenischen Krankheitsphasen ohne Beteiligung einer Infektion auftreten.
In erster Linie ist bei neutropenischen Patienten das Risiko für bakterielle Infektionen erhöht. Diese können durch grampositive oder gramnegative Erreger hervorgerufen werden, die v. a. physiologisch im Mund-Rachen-Bereich, Rektal-Genital-Bereich und auf der Haut lokalisiert sind und sich durch das Fehlen der Neutrophilen ungestört vermehren und im Körper verteilen können. Bis zu 80 % der Infektionserreger stammen aus der endogenen Flora des Patienten.
Es sind aber nicht nur die körpereigenen Erreger, die Infektionen auslösen können. Die sog. nosokomialen Infektionen (Krankenhausinfektionen, Kreuzinfektionen) stellen für den abwehrgeschwächten Patienten ein besonders hohes Risiko für eine Infektion dar. Quellen solcher ▶ nosokomialen Infektionen sind:
-
Patienten
-
Personal (Pflegende, Ärzte, Physiotherapeuten, MTA)
-
Besucher
-
Blutderivate, transplantiertes Knochenmark
-
invasive medizinische Hilfsmittel (Venenkatheter, Harnwegskatheter, Endotrachealtuben)
-
Infusionen
-
Luft
Intensive Chemotherapien können z. T. eine erhebliche Schädigung der Schleimhäute verursachen, was sich in Erosionen und Ulzera äußert. Die Schädigung der natürlichen Mukosabarriere ermöglicht dann eine deutliche Zunahme der Keimeinschwemmung, der langfristig neutropenische Patienten nahezu schutzlos ausgeliefert sind.
Die klinischen Symptome von Infektionen bei leukopenischen Patienten variieren in Abhängigkeit von der Art des Krankheitserregers, der jeweiligen Abwehrlage des Patienten und der betroffenen Gewebe und Organe. Anfangs bestehen grippeähnliche Symptome wie erhöhte Körpertemperatur (> 38 °C), Schüttelfrost, Kopfschmerzen, Halsschmerzen, allgemeine Gelenkbeschwerden, Appetitlosigkeit und Übelkeit. Im weiteren Krankheitsverlauf können eine Tonsillitis, eine Otitis media, eine Mukositis des Verdauungstraktes und/oder Urogenitaltraktes folgen.
Bei langandauernden Neutropenien kommt es häufig zu pulmonalen Infektionen und durch intensive Antibiotikatherapien auch zu Pilzinfektionen (insbesondere Candida albicans und Aspergillus).
Merke
Aus kleinen Verletzungen oder banalen Erkältungen kann sich in kürzester Zeit ein lebensbedrohlicher Zustand entwickeln.
Sepsis Die größte Gefahr der Neutropenie ist die Entstehung einer Sepsis – einer Allgemeininfektion des Patienten, die sich über das Blut in alle Organe verteilen kann. Die gefährlichen Komplikationen ergeben sich aus den jeweiligen Organbeteiligungen. So können sich Krankheitserreger im Gehirn absiedeln und eine massive Zerstörung von Nervenzellen verursachen. Eine mögliche Folge der schweren Kreislaufschwäche des Sepsispatienten ist das sog. Multiorganversagen. Es kann im weiteren Verlauf zu Störungen des Gerinnungssystems mit spontanen Blutungen im Körperinneren kommen. Die Überschwemmung des Organismus mit Giftstoffen, die von den Erregern freigesetzt werden, bewirkt schließlich einen Schockzustand. Jede einzelne dieser Komplikationen kann zum Tod des Patienten führen.
Merke
Eine akute febrile Leukopenie ist immer ein medizinischer Notfall!
Prophylaktische Maßnahmen zur Infektionsvermeidung
Infektionen bei Tumorpatienten zählen zu den häufigsten Morbiditäts- bzw. Mortalitätsursachen. Die prophylaktischen Maßnahmen zur Infektionsvermeidung erhalten im stationären wie auch im ambulanten Bereich dadurch einen hohen Stellenwert.
Vor und während einer Tumortherapie müssen Patienten und deren Angehörige sowohl über die Wirkungsweise als auch über mögliche Auswirkungen einer Tumortherapie sowie über Verhaltensweisen und vorbeugende Maßnahmen ausreichend informiert werden.
Die hygienischen Vorsichtsmaßnahmen variieren z. T. von Klinik zu Klinik. Die folgenden Informationen gelten nicht nur für Patienten, sondern auch für das therapeutische Team und Besucher der Patienten:
-
▶ konsequente Händedesinfektion immer vor Kontakt mit dem Patienten durchführen (Ärzte, Pflegende, Patienten untereinander, MTA, Physiotherapeuten, Besucher)
-
Händedesinfektion nach jedem Toilettengang durchführen
-
therapeutisches Team trägt Mundschutz bei Hochrisikopatienten (Leukozytenwerte < 1000/µl)
-
Besucher tragen Mundschutz und Kittel bei Hochrisikopatienten
-
Patienten tragen Mundschutz und Kittel beim Verlassen des Zimmers bei Leukozytenzahlen < 1000/µl
-
Sprühdesinfektion/Wischdesinfektion von Dusche, WC, Toilettenstuhl, Stethoskop täglich durchführen
-
Zimmerhygiene (tägliche Wischdesinfektion) durchführen
-
für eine adäquate Patientenunterbringung sorgen (1 – 2-Bettzimmer mit eigener Nasszelle oder sterile Einheit nach allogener KMT)
-
Vernebler vermeiden
-
Besuch von Kindern unter 10 Jahren nicht gestatten (virusbedingte „Kinderkrankheit“)
-
keinen Besuch von erkrankten Besuchspersonen zulassen
-
Menschenansammlungen meiden
-
potenziell hochkontaminierte Nahrungsmittel meiden (frisches Obst und Gemüse, rohes Fleisch, roher Fisch, Produkte mit rohen Eiern, Frischkäse, Schimmelkäse, Nüsse, Müsli, Trockenobst, Fruchtsäfte)
-
Obst und Gemüse stets schälen bzw. intensiv abwaschen
-
keine Topfpflanzen oder Schnittblumen mitbringen
-
Kontakte mit Haustieren vermeiden
Medizinische Maßnahmen bei Neutropenie
Folgende medizinische Maßnahmen müssen/sollten durchgeführt werden:
-
Eine prophylaktische Antibiotikagabe bei Leukozytenwerten < 1000/µl und bei Hochdosistherapie ab Beginn der Zytostatikatherapie sollte erwogen werden.
-
Bei ersten klinischen Verdachtszeichen einer Infektion muss die sofortige Gabe von Antibiotika erfolgen, bevor Kulturresultate und Resistenzbestimmungen vorliegen.
-
Antimykotische Prophylaxe (z. B. Ampho-Moronal) bei Leukozytenwerten < 1000/µl, bei Hochdosistherapie ab Beginn der Zytostatikagabe verabreichen.
-
Antivirale Prophylaxe nur nach allogener Transplantation, ansonsten antivirale Therapie bei Auftreten von Virusinfektionen durchführen.
-
Prophylaktische Gabe hämatopoetischer Wachstumsfaktoren (G-CSF) bei hoher Wahrscheinlichkeit infektiöser Komplikationen während der Neutropenie erwägen.
-
Täglich Blutbildkontrollen durchführen.
-
Blutkulturen und Resistenzbestimmungen bei Fieber > 38 °C anlegen.
-
Symptomatische Maßnahmen durchführen.
Pflegerische Maßnahmen bei Neutropenie
Pflegerische Maßnahmen haben bei Patienten mit langandauernder Neutropenie einen hohen Stellenwert. Die natürlichen Haut- und Schleimhautbarrieren sind durch lang liegende zentralvenöse Verweilkatheter, Haut- und Schleimhautläsionen im Rahmen der Radio- und/oder Chemotherapie gestört und können zu Eintrittspforten für pathogene Krankheitserreger werden. Daher ist es für das therapeutische Team, die Patienten und Angehörigen besonders wichtig, auf Anzeichen einer möglichen Infektion zu achten, damit eine entsprechende Therapie rechtzeitig eingeleitet werden kann.
Merke
Die 5 Kardinalsymptome einer Infektion sind:
-
Schwellung (Tumor)
-
Schmerz (Dolor)
-
Rötung (Rubor)
-
Überwärmung (Calor) → Fieber !
-
Funktionseinschränkung (Functio laesa)
Weitere Zeichen sind:
-
Geruch (Odor)
-
Taschenbildung (z. B. Zahnfleisch)
-
Laborwerte (CRP erhöht)
Folgende Maßnahmen sollten von Pflegenden durchgeführt werden:
-
täglich Haut- und Schleimhautbereiche und alle Kathetereintrittsstellen inspizieren
-
Beschwerden beim neutropenischen Patienten beachten:
-
erhöhte Körpertemperatur (> 38 °C) mit oder ohne Schüttelfrost
-
Schmerzen, Juckreiz, Druckempfindlichkeit
-
Diarrhöen
-
Husten und Atemnot
-
Schmerzen beim Wasserlassen oder häufiges Wasserlassen
-
-
täglich Vitalparameter (Temperatur, Blutdruck, Puls) erfassen
-
bei Verbands- und Zuleitungswechsel hygienisch arbeiten (alle 48 Std., außer wenn Verbände durchfeuchtet sind, dann häufiger)
-
bei der Portpflege aseptisch arbeiten
-
Hautpflege mit neutraler Creme oder Lotion auf Wasser-Öl-Basis durchführen
-
beim Patienten auf Körperhygiene achten:
-
sorgfältige perineale Hygiene nach jedem Toilettengang (Intimpflege, Händewaschen)
-
Nägel schneiden vermeiden
-
täglich Wäschewechsel (möglichst Baumwolle tragen)
-
Badeschuhe beim Duschen tragen (Schutz vor Fußpilz)
-
Körperpflege mit (Einmal-)Waschlappen
-
unnötige invasive Eingriffe vermeiden
-
Patienten zum regelmäßigen Atemtraining auffordern
-
Besucher auf Infektionsanzeichen überprüfen
-
ärztliche Anordnungen ausführen
Häusliche Pflege im Fokus
Bei ambulanten Patienten mit einer Neutropenie ist es erforderlich, die häusliche Umgebung der veränderten Lebenssituation anzupassen. Es ist daher wichtig, Patienten und Angehörige von Beginn der Therapie an in pflegerische Maßnahmen einzubeziehen und pflegerische Handlungsabläufe mit ihnen einzuüben, damit ambulante Therapien möglichst ohne Komplikationen ablaufen.
46.5.5.2 Thrombozytopenie
Definition
Die Thrombozytopenie ist die Verminderung von Thrombozyten, die mit einer erhöhten Blutungsneigung einhergeht. Bereits bei Thrombozytenzahlen von < 150 000/µl spricht man von einer Thrombozytopenie. Die Blutungsbereitschaft steigt mit abnehmender Thrombozytenzahl, wobei sie sich bei Thrombozytenwerten < 30 000/µl beträchtlich verstärkt (Normalwerte s. ▶ Tab. 46.12 ).
Symptome
Thrombozytopenien haben ein weites Ursachenspektrum. Der menschliche Körper toleriert erniedrigte Thrombozytenwerte ohne merkliche Schäden oder klinische Ausfallerscheinungen. Es kann bei den betroffenen Patienten zu kleineren Hämatomen, Nasen- und Zahnfleischbluten oder zu Einblutungen in die Gelenke kommen. Hierbei merken die Patienten häufig selbst, dass Blutungen bei Verletzungen länger dauern als üblich (Blutungszeit überschreitet den Normwert von 6 Min.). Das Risiko für eine Blutung steigt, je niedriger die Thrombozytenwerte sind. Für das Auftreten von Blutungen kann leider kein allgemeingültiger Grenzwert angegeben werden, da dieser von Patient zu Patient erheblich schwanken kann. Bei Thrombozytenzahlen von < 30 000/µl kann es aber ohne äußere Einwirkungen zu Einblutungen an Haut und Schleimhäuten, in schweren Fällen sogar zu lebensbedrohlichen Spontanblutungen (z. B. Hirnblutungen) kommen.
Häufig auftretende Blutungen sind:
-
rezidivierende Nasen- oder Zahnfleischblutungen
-
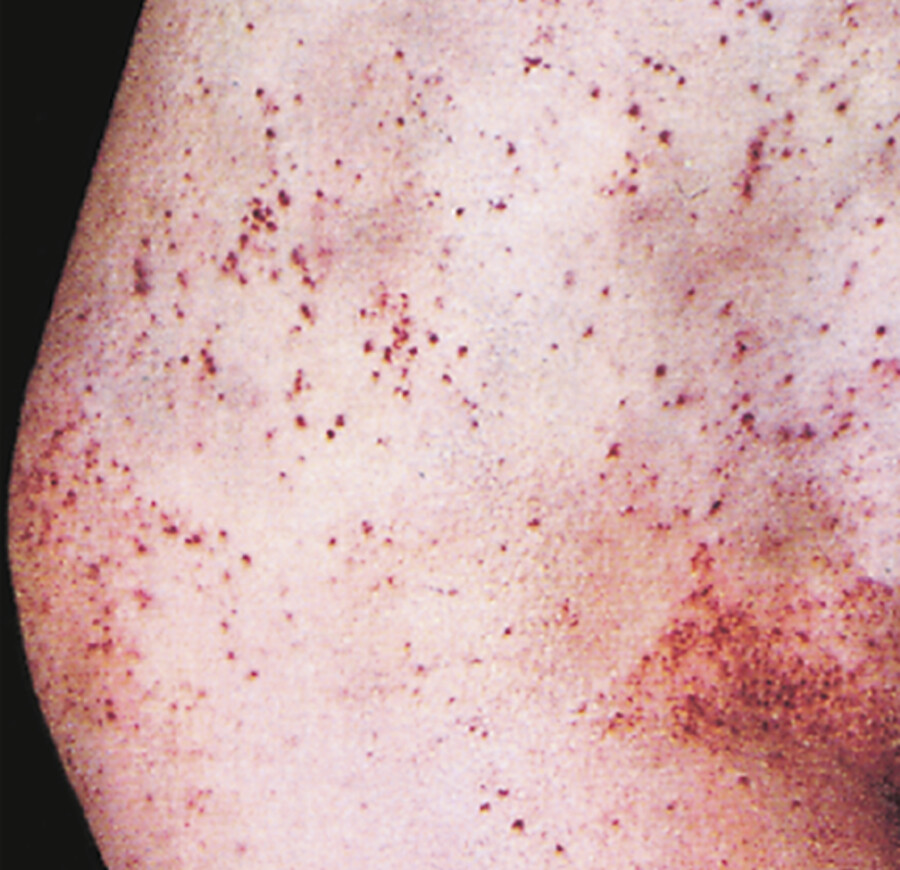
Petechien, oft primär an den unteren Extremitäten ( ▶ Abb. 46.14)
Petechien.
Abb. 46.14 Zu sehen sind stecknadelkopfgroße, flohstichartige Blutungen bei Thrombozytopenie.
-
flächenhafte Hautblutungen (Hämatome)
-
Blutungen des Gastrointestinaltraktes
-
Blutungen des Urogenitaltraktes
-
Blutungen des Atemtraktes
-
intrazerebrale Blutungen
-
Blutungen von Wunden mit verlängerter Blutungszeit bei invasiven Eingriffen
-
Blutungen aus Einstichstellen, z. B. nach venöser oder kapillärer Blutentnahme
Medizinische Maßnahmen
Die medizinischen Maßnahmen richten sich nach den jeweiligen Thrombozytenwerten. Im Allgemeinen werden Patienten mit Thrombozytenwerten < 20 000/µl symptomatisch mit Thrombozytentransfusionen (TK) behandelt. Dies umfasst:
-
regelmäßige Kontrolle der Thrombozytenwerte
-
Thrombozytentransfusion (bei niedrigen Thrombozyten und/oder bei Blutungszeichen)
-
diagnostische Maßnahmen bei auftretenden Symptomen, z. B. Gastroskopie, CT, MRT
-
Verabreichung fibrinolysehemmender Medikamente (z. B. Anvitoff)
Merke
Patienten mit einer Thrombozytopenie sollten keine Medikamente einnehmen, die die Thrombozytenaggregation hemmen, z. B. Acetylsalizylsäure.
Häusliche Pflege im Fokus
Prophylaktische Maßnahmen zur Vermeidung von Blutungen
Im Hinblick auf die ambulante Weiterbehandlung stellt die Weitergabe von umfassenden Informationen an den Patienten und seine Angehörigen einen wichtigen Pfeiler der Pflege dar. Vor der Entlassung stationärer und ambulanter Patienten ist ein ausführliches Gespräch über die Blutungszeichen sowie die prophylaktischen und therapeutischen Maßnahmen bei potenziellen bzw. auftretenden Blutungen zu führen.
Folgende detaillierte Informationen sollten in dem Gespräch vermittelt werden:
-
übermäßige Anstrengungen vermeiden
-
unnötige invasive Eingriffe, z. B. Punktionen, Injektionen, Katheterisierung, vermeiden
-
im Umgang mit spitzen Gegenständen (Nagelschere, Nassrasierer) vorsichtig sein
-
Nassrasur vermeiden
-
keine einengende, abschnürende Kleidung tragen
-
Nasenschleimhaut feuchthalten:
-
durch Nasensalben und Nasenöle
-
genügende Trinkmenge
-
angefeuchtete Luft, gut belüftete Räume
-
-
Nase nur sanft schnäuzen
-
weiche Zahnbürste zur Zahnreinigung verwenden, ggf. Watteträger
-
auf Druckstellen von Zahnprothesen achten
-
Lippen feucht und geschmeidig halten, z. B. mit Vaseline; keine glyzerinhaltigen Lippenpflegemittel benutzen, da dies zu weiterer Austrocknung führt
-
auf den Konsum von harten, heißen oder stark gewürzten Speisen verzichten
-
Stuhl weich halten, z. B. durch Aufnahme von Dörrobst, Sauerkrautsaft, Milchzucker
-
auf rektale Temperaturmessung verzichten
-
Gleitmittel beim Geschlechtsverkehr benutzen
-
Menstruationsblutung durch Hormongaben unterdrücken
Die Patienten und ihre Angehörigen müssen auf eine gute Haut- und Schleimhautbeobachtung hingewiesen werden. Schon während des Krankenhausaufenthalts sollten sie mit in die Haut- und Schleimhautbeobachtung bzgl. Blutungszeichen einbezogen werden. So erlangen sie Kompetenz und Sicherheit für die Versorgung im häuslichen Umfeld.
Pflegerische Maßnahmen
Höchste Priorität hat die sorgfältige Beobachtung des Patienten hinsichtlich auftretender Blutungen und Blutungsanzeichen. Mögliche Zeichen einer ausgeprägten Blutung sind z. B. Tachykardie und Hypotonie; bei intrazerebraler Blutung kann es zu Vigilanzveränderungen kommen. Es ist wichtig, diese Zeichen sofort zu erkennen und schnellstens zu reagieren, um mögliche Komplikationen zu verhindern.
Maßnahmen bei auftretenden Blutungen
Sofern man bei Patienten Blutungszeichen erkennt, sollte Rücksprache hinsichtlich der Thrombozytenwerte und weiterer Maßnahmen mit dem behandelnden Arzt erfolgen.
Maßnahmen bei Nasenbluten
-
in Schutzhülle eingewickeltes Coldpack in den Nacken legen (Vasokonstriktion)
-
Kopf nach vorne beugen
-
Nasenflügel zusammendrücken
-
Nasentropfen (z. B. Nasivin) verabreichen (Vasokonstriktion)
-
ggf. Nasentamponade anlegen, befeuchtet mit blutungsstillenden Medikamenten, z. B. Anvitoff
Maßnahmen bei Blutungen im Magen-Darm-Trakt
-
Symptome wie Teerstuhl, blutiges Erbrechen beachten
-
Vitalzeichenkontrolle (insbesondere Blutdruck und Puls)
-
Medikamente nach Anordnung des Arztes verabreichen (z. B. Pantozol)
Maßnahmen bei Hautblutungen
-
Druckverband bei stark blutenden Wunden anlegen
-
Coldpacks verwenden (Vasokonstriktion)
Bei der Transfusion von Thrombozytenkonzentraten muss die Überwachung des Patienten nach den Transfusionsvorschriften erfolgen.
46.5.5.3 Anämie
Die Anämie stellt die häufigste hämatologische Komplikation bei onkologischen Patienten dar.
Definition
Die Anämie ist ein Abfall der Erythrozyten, des Hämoglobins und des Hämatokrits. Nach den Leitlinien der EORTC (European Organisation for Research on Treatment of Cancer) wird eine Anämie als Abfall des Hämoglobin(Hb)-Spiegels < 12 g/dl definiert. Umgangssprachlich wird die Anämie auch als Blutarmut bezeichnet. Zum besseren Verständnis s. Normalwerte ( ▶ Tab. 46.12 ).
Es gibt verschiedene Formen der Anämie:
-
Anämie durch einen erhöhten Blutverlust
-
Anämie durch verminderte Erythropoese (z. B. Eisenmangelanämie)
-
▶ aplastische Anämie, eine Knochenmarkinsuffizienz mit Störung aller 3 Zellreihen der Blutbildung
-
Anämie infolge eines erhöhten Erythrozytenabbaus (z. B. Sichelzellanämie)
Die Ursachen der Anämie können bei Tumorpatienten sowohl tumor- als auch therapiebedingt sein.
Symptome
Die Auswirkungen der Anämie auf die Funktion verschiedener Organe, die körperliche Leistungsfähigkeit und die Psyche der Betroffenen sind individuell sehr unterschiedlich.
Ältere Patienten mit Herz-Kreislauf-Erkrankungen reagieren, im Gegensatz zu jüngeren Patienten, oft schon bei geringgradigen Anämien, mit ausgeprägten Symptomen. Im Vordergrund steht die verminderte körperliche Leistungsfähigkeit. Bei zunehmender Anämie kann es soweit gehen, dass die Betroffenen unfähig sind, ihre alltäglichen Verrichtungen auszuüben. Der Tumorerschöpfung, eine mit Anämie auftretende quälende Müdigkeit (Fatigue), kommt hierbei eine besondere Bedeutung zu, da diese die Lebensqualität der Patienten erheblich einschränken kann.
Mögliche Krankheitszeichen und Symptome einer Anämie sind:
-
Haut- und Schleimhautblässe
-
Tachykardie (Herzrasen)
-
Kurzatmigkeit, Schwäche, Kopfschmerzen
-
Müdigkeit (Fatigue), Antriebslosigkeit
-
Schwindel, Benommenheit
-
orthostatische Regulationsstörungen, Übelkeit
-
Sehstörungen (z. B. Flimmern)
-
verminderte Leistungsfähigkeit
-
Libidoverlust
-
schwache oder aussetzende Menstruationsblutung
-
Sturzneigung
In der Regel treten mehrere Symptome gleichzeitig auf. Die Schwere der genannten Symptome hängt vom Allgemeinzustand des Patienten ab und davon, wie schnell sich die Anämie entwickelt hat.
Da Erythrozyten eine Lebensdauer von 100 – 120 Tagen haben, entwickelt sich eine Anämie i. d. R. nicht so schnell wie eine Thrombo- bzw. Leukozytopenie, da diese Zellen wesentlich kurzlebiger sind. Der Körper hat dadurch mehr Zeit, sich den veränderten Verhältnissen anzupassen.
Medizinische Maßnahmen
Die medizinischen Maßnahmen hängen von der Höhe des Hämoglobinwertes und den auftretenden Symptomen ab. Es ist wichtig,
-
die Ursache der Anämie abzuklären,
-
regelmäßige tägliche Blutbildkontrollen durchzuführen,
-
die Transfusion von Erythrozyten je nach Wert bzw. Symptomatik anzuordnen (i. d. R. bei Hb-Wert < 8,0 g/dl) und
-
ggf. Wachstumsfaktoren zu verabreichen (z. B. Erythropoetin).
Pflegerische Maßnahmen
Aufgabe der Pflegenden ist es, den Patienten sorgfältig zu beobachten und das Aktivitätsspektrum den aufgetretenen Symptomen anzupassen. Ein Problembewusstsein muss sowohl bei Patienten als auch bei Angehörigen und Fachpersonal geschaffen werden, da die Symptome der Anämie, insbesondere von Fatigue, häufig unterschätzt werden.
Folgende Maßnahmen werden durchgeführt:
-
über Symptome der Anämie aufklären
-
Hilfestellungen geben
-
für ausreichend Erholungsphasen sorgen
-
Aktivitäten priorisieren
-
langsam aufstehen, ggf. Mobilisation unterstützen
-
ausreichend Flüssigkeit zuführen
-
Vitalzeichen kontrollieren
-
Hilfsmittel für die Klinik und zuhause beantragen (z. B. Rollator)
-
Wohnraum anpassen, um Stürze zu vermeiden
-
Krankenhausumgebung sicher gestalten
-
bei Erythrozytentransfusionen den Patienten nach Transfusionsvorschriften überwachen
Merke
Die subjektiven Empfindungen des Patienten müssen in der Planung der Pflegemaßnahmen stets berücksichtigt werden.
Lebensphase Kind
Lars Wicher
Knochenmarksdepression
Von einer Knochenmarksdepression spricht man, wenn es zu einer Schädigung von Blutstammzellen im roten Knochenmark kommt und die Bildung neuer Blutzellen dadurch verhindert wird. Davon betroffen sind alle Reihen der Blutzellen, also die Erythrozyten, die Leukozyten sowie die Thrombozyten.
Anleitung der Eltern
Die bereits dargestellten pflegerischen Maßnahmen bei Neutropenie, Thrombozytopenie und Anämie gelten auch für die Versorgung von Kindern und Jugendlichen. Da die Grundpflege größtenteils von den Eltern durchgeführt wird, ist eine intensive Anleitung und Begleitung besonders wichtig. Sie müssen über mögliche Symptome aufgeklärt werden und wissen, wie sie beim Auftreten der Symptome handeln müssen.
Die Krankenbeobachtung erfolgt nun vermehrt durch die Eltern. Deshalb sollte für ein Informationsgespräch genügend Zeit veranschlagt werden.
Merke: Die Übernahme der Krankenbeobachtung durch die Eltern entbindet die Pflegenden nicht von einer eigenen Einschätzung auftretender Veränderungen und Auffälligkeiten.
Informationsgespräch
Nach Möglichkeit werden die Kinder in das Informationsgespräch mit einbezogen. Bereits Kleinkinder beobachten und interpretieren ihr Umfeld. Sie nehmen Gefühlsregungen wahr, ohne sie verstehen zu können. Dennoch sind sie in der Lage, z.B. das Weinen der Mutter als etwas Negatives zu interpretieren. Sie sollten deshalb in die Abläufe der Therapie integriert und nicht außen vor gelassen werden.
Jugendliche hingegen setzen sich bereits mit ihrer Erkrankung und den Nebenwirkungen der Therapie auseinander und fühlen die Bedrohung, die von ihr ausgeht (Gutjahr 2009). Das Informationsgespräch sollte immer altersentsprechend geführt werden, ohne den Jugendlichen zu überfordern. Ängste können so im Vorfeld reduziert werden (Rinner 2012).
Psychosoziale Aspekte
Die Auswirkungen der Krebstherapie verdeutlichen den Kindern und Jugendlichen und ihren Eltern, wie sehr ihr bisheriges Leben aus den Angeln gehoben und verändert wird. Während der Therapie dürfen die Kinder und Jugendlichen nicht mehr in den Kindergarten oder in die Schule. Freunde dürfen nur zu Besuch kommen, wenn sie infektfrei sind. Kino- oder Konzertbesuche sind untersagt. Dies kann sich negativ auf soziale Beziehungen und die Integration in den Schulverband auswirken.
Gleichzeitig haben sich die Jugendlichen vor ihrer Erkrankung einen Freiraum der Selbstständigkeit und der Unabhängigkeit von ihren Eltern geschaffen. Aufgrund der Erkrankung und der Nebenwirkungen der Therapie verlieren sie einen Teil davon (Labouvie u. Bode 2006, Gutjahr 2009). Sie sind nun vermehrt auf die Hilfe der Pflegenden und der Eltern angewiesen. Dem Auftreten von Schmerzen, Fieber, Blutungen oder dem Warten auf „gute Blutwerte“ stehen sie machtlos gegenüber. Nicht selten ziehen sich gerade Jugendliche mit der Zeit in sich zurück. Deshalb ist es auf kinderonkologischen Stationen besonders wichtig, eine offene Kommunikation zu leben und eine Integration am Behandlungsgeschehen zu ermöglichen. Dadurch nehmen sie angebotene Maßnahmen eher an und unterstützen so aktiv den Heilungsprozess.
46.5.6 Therapiebedingte Ernährungsstörungen
Ernährungsstörungen treten i. d. R. bei allen Tumorpatienten im Laufe ihrer Erkrankung und während der Behandlung auf. Die Folge von Ernährungsstörungen ist fast immer ein ungewollter Gewichtsverlust, der schließlich zu einer Mangelernährung führt.
Definition
Eine Mangelernährung entsteht, wenn die Aufnahmemenge an Energie und Nährstoffen nicht den Energie- und Nährstoffbedürfnissen einer Person entspricht.
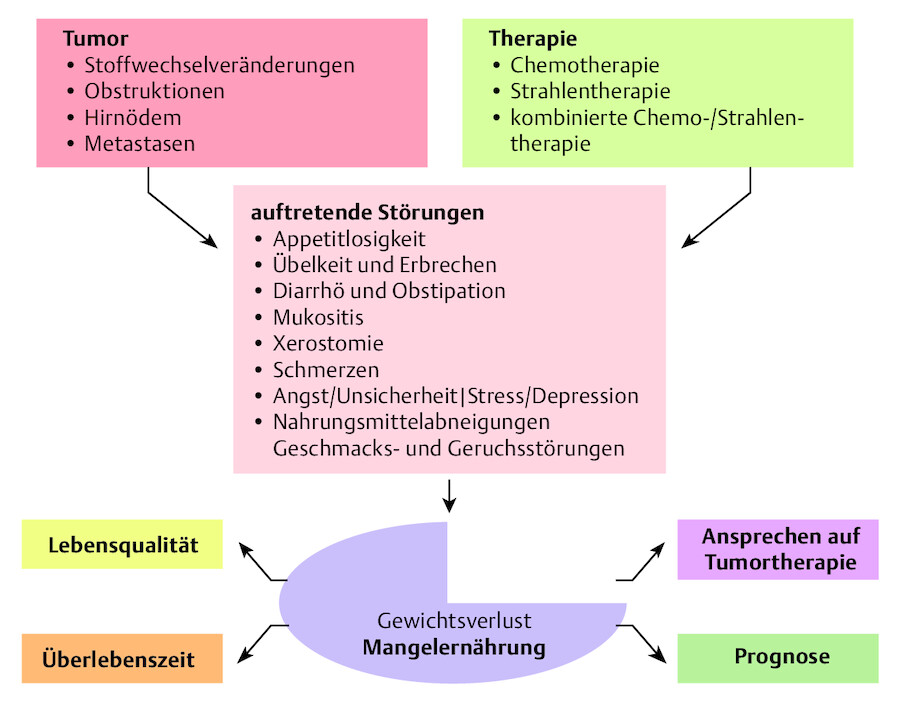
Viele Krebspatienten haben bereits vor der Diagnosestellung erheblich an Gewicht verloren, bevor sie selbst oder der behandelnde Arzt auf die Erkrankung aufmerksam werden. Ernährungszustand und Gewichtsverlust bei Tumorpatienten haben einen gravierenden Einfluss auf die Lebensqualität, den Behandlungsverlauf und -erfolg sowie auf die Überlebenszeit ( ▶ Abb. 46.15). Nahezu alle Krebserkrankungen verursachen in den letzten Monaten vor dem Tod einen dramatischen Gewichtsverlust.
Auswirkungen von Gewichtsverlust und Mangelernährung.
Abb. 46.15
46.5.6.1 Ursachen ungewollten Gewichtsverlusts und einer Mangelernährung
Die Ursachen des krankheitsbedingten Gewichtsverlusts sind sehr vielfältig. Neben dem erhöhten Energie- und Nährstoffbedarf des Körpers infolge zehrender Tumoren und Therapien sind häufig die auftretenden Nebenwirkungen der Therapien Ursache des Gewichtsverlusts und der Mangelernährung. In jedem Stadium einer Krebserkrankung kann ein Gewichtsverlust auftreten. Folgende Ursachen führen zu Gewichtsverlust und Mangelernährung:
Stoffwechselveränderungen beim Tumorpatienten Sie führen zu Verlust an Fett und Muskelmasse (Glukoseumsatz erhöht, Fettabbau erhöht, Abbau von Muskeleiweiß).
Störungen der Nährstoffaufnahme Die Nahrungsaufnahme ist gestört durch:
-
Appetitlosigkeit
-
unzureichende Ernährung, bedingt durch Schmerzen und Tumor
-
verändertes Geschmacks- und Geruchsempfinden
-
Kau-/Schluckbeschwerden
-
Mundtrockenheit, Mukositis
-
Speichelveränderungen
-
Obstipation, Völlegefühl und Blähungen
-
erhöhten Bedarf an Kalorien und Nährstoffen, bedingt durch die Grunderkrankung
-
krankheitsbedingte Angst und Beklemmungszustände
-
Tumorbehandlungen (Chemo-, Strahlentherapie, Operation)
-
Erschöpfung, Atemnot, Muskelschwäche
Verlust an Nährstoffen Wichtige Nährstoffe gehen verloren bei:
-
Diarrhö, Verdauungsstörungen
-
Übelkeit und Erbrechen (Zytostatika, Bestrahlung)
Störungen des Nährstoffstoffwechsels Der Nährstoffwechsel ist gestört
-
nach Operationen,
-
durch Komplikationen wie Fieber,
-
durch Entzündungen.
46.5.6.2 Folgeerscheinungen der Mangelernährung
Mangelernährte Patienten haben deutlich mehr Nebenwirkungen unter der Tumortherapie. Neben der starken Beeinträchtigung und zusätzlichen Belastung bedeutet dies für viele eine erhöhte Pflegebedürftigkeit und einen längeren Krankenhausaufenthalt.
Es gibt viele Untersuchungen, die belegen, dass eine krankheitsbedingte Mangelernährung zu einer erhöhten Morbidität, zu verminderter Lebensqualität, zu reduzierter Muskelkraft und zu Einschränkungen anderer Körperfunktionen führt. Neben der Verschlechterung der Prognose erhöht sich bei vorliegender Mangelernährung die Komplikations- und Sterberate.
Eine Mangelernährung führt zu
-
schlechtem Allgemeinzustand,
-
erhöhten Komplikationsraten nach Operationen (verlängerte Konvaleszenz und längere Klinikaufenthalte),
-
Schwächung des Immunsystems (Steigerung der Infektanfälligkeit),
-
Verschlechterung der Wundheilung (z. B. verzögertes bzw. Nicht-Abheilen von Dekubitus),
-
Muskelschwäche (führt zu reduzierter Mobilität und erhöhtem Sturzrisiko),
-
Beeinträchtigung des Stoffwechsels (s. o.),
-
verringerter Verdauungs- und Resorptionsfunktion,
-
Verminderung von Enzymaktivitäten,
-
Störungen der Organaktivität (z. B. reduziertes Herzvolumen),
-
verminderter Toleranz gegenüber onkologischer Therapien,
-
verzögertem Wachstum und gestörter Entwicklung bei Kindern,
-
geschwächten psychologischen Funktionen (Apathie und Depressionen, schlechte Konzentrationsfähigkeit),
-
reduzierter Lebensqualität (Stimmung und Wohlbefinden),
-
Verschlechterung der Prognose.
46.5.6.3 Diagnostik der Mangelernährung
Es gibt verschiedene Möglichkeiten, eine Mangelernährung zu diagnostizieren:
-
Körpergewichtsbewertung nach ▶ Body-Mass-Index, kurz BMI; Formel: Körpergewicht in kg geteilt durch die Körperlänge in m2 (< 18 = Mangelernährung bezogen auf Energie, Nähr- und Wirkstoffe)
-
bioelektrische Impendanzanalyse (BIA): unter Berücksichtigung von Körpergröße, Gewicht, Alter, Geschlecht wird computergestützt der Wassergehalt, die Fettmasse, die fettfreie Masse, die Körperzellmasse, die Körperdichte und der Grundumsatz berechnet
-
Laborparameter (z. B. Albumin, CRP, Elektrolyte, Vitamine u. a.)
-
klinischer Blick
46.5.6.4 Tumorkachexie
Die schwerste Form der krankheitsbedingten Mangelernährung bei Tumorpatienten ist die Tumorkachexie (griech: „schlechter Zustand“). Die Kachexie ist eine spezielle metabolische Form der tumorassozierten Mangelernährung, die v. a. in fortgeschrittenen Tumorsituationen auftritt. Die Kriterien für eine Tumorkachexie sind die Kombination aus Mangelernährung und systemischer Entzündungsreaktion:
-
Mangelernährung: Gewichtsverlust von mind. 10 % des gesunden Ausgangsgewichts
-
Nachweis systemischer Entzündungsmarker, z. B. Anstieg von CRP und Abfall von Albumin
Um den Beginn einer Kachexieentwicklung möglichst früh zu erfassen, sollte regelmäßig das Gewicht kontrolliert (alle 1 – 2 Wochen) sowie der Gewichtsverlauf dokumentiert werden. Die Kontrolle der Laborparameter (CRP und Albumin im Serum alle 4 Wochen) zeigen frühzeitig die Aktivierung systemischer Entzündungsprozesse. Der Appetit und die Nahrungsaufnahme des Tumorpatienten müssen bei der Einschätzung mit berücksichtigt werden. Müdigkeit, Erschöpfung und ein schlechtes Allgemeinbefinden können erste Anzeichen einer Mangelernährung sein.
46.5.6.5 Situation des Patienten
Die Mangelernährung stellt nicht nur für den Betroffenen, sondern auch für die Angehörigen und das therapeutische Team ein großes Problem und damit eine große Herausforderung dar. Fast jeder Krebspatient hat Angst vor dem Abnehmen, weil der Gewichtsverlust unbewusst mit einem Fortschreiten der Tumorerkrankung verbunden wird. Die Angehörigen versuchen alles, um das Fortschreiten der Gewichtsabnahme zu verhindern. Mit dem Kochen von Lieblingsgerichten und dem häufigen Auffordern, etwas zu essen, kommt es nicht selten zu Konflikten zwischen den Partnern oder Eltern und ihren Kindern. Angehörige und Pflegende sollten keinen Druck betreffend der Nahrungsaufnahme auf den Patienten ausüben. Die Beteiligten sollten herausfinden, was in der gegenwärtigen Situation dem Patienten am besten hilft.
Wenn während der Chemo- und/oder Strahlentherapie keine Ernährungsstörungen auftreten, benötigt der Tumorerkrankte meist keine spezielle Nahrung. Er kann sich mit einer ausgewogenen, leicht verdaulichen, abwechslungsreichen sowie vitamin- und mineralstoffreichen Kost, die nach seinen Wünschen und Bedürfnissen (Wunschkost) zusammengestellt ist, ernähren.
Prävention und Gesundheitsförderung
Tipps für eine leicht verdauliche Vollwertkost:
-
abwechslungsreiches Essen
-
mehrere kleine Mahlzeiten
-
reichlich Gemüse (gekocht, Gemüsesaft)
-
regelmäßig Obst (Zitrusfrüchte, Schälobst)
-
keine Nüsse
-
Getreide- und Getreideerzeugnisse aus Vollkornprodukten bevorzugen
-
Milchprodukte, Frischkäse, milde Käsesorten
-
pflanzliche Fette (Öle) verwenden
-
reichlich trinken
-
blähende Lebensmittel meiden
-
gut kauen und langsam essen
-
Alkohol in Maßen
Sinnvolle Ziele einer Ernährungstherapie bei Tumorpatienten sind:
-
Verhinderung oder Behandlung einer Mangelernährung
-
Erhalt bzw. Stärkung der körperlichen und geistigen Mobilität
-
Verbesserung der subjektiven Lebensqualität
-
Reduktion unerwünschter Effekte antitumoraler Therapien
-
störungsfreie Ernährung
46.5.6.6 Ernährungsberatung
Während des Klinikaufenthalts ist die Zusammenarbeit des therapeutischen Teams (Pflegende, Ernährungsberaterinnen, Ärzte) von enormer Bedeutung. Die Pflegenden ermitteln die Menge der Nahrungszufuhr mittels einer mündlichen Ernährungsanamnese. Gleichzeitig gibt die Anamnese Aufschluss über die individuellen Ernährungsgewohnheiten und Ernährungsbedürfnisse des Patienten. Da die Pflegenden den Patienten während der Therapie intensiv betreuen und begleiten, erkennen sie frühzeitig, wenn die Nährstoffaufnahme aufgrund von therapiebedingten Störungen (Mukositis, Diarrhö, Schmerzen, Erbrechen) nicht mehr ausreichend ist.
Während des Klinikaufenthalts kann jederzeit eine Ernährungsfachkraft hinzugezogen werden, besonders dann, wenn der Patient die Nahrungsaufnahme immer mehr einschränkt und anfängt, Gewicht zu verlieren. Eine gezielte Ernährungsberatung beseitigt Unsicherheiten auf Seiten des Patienten, schützt vor einseitiger Ernährung und lässt Ernährungsfehler schnell erkennen. Hier ist es sinnvoll, die Bezugspersonen mit zu schulen, da i. d. R. nach der stationären Therapie immer eine ambulante Weiterbehandlung erfolgt. Es ist auch Aufgabe der Ernährungsfachkraft, den Patienten über Ernährungsumstellungen bei besonderen Tumortherapien aufzuklären (z. B. Aplasiekost nach Stammzelltransplantation).
46.5.6.7 Therapieansätze bei Tumorkachexie
Zur Behandlung einer Tumorkachexie sollte zunächst versucht werden, die orale Energieaufnahme anzuheben. Behindernde gastrointestinale Faktoren sollten gesucht und behandelt werden. Eine vom Arzt eingeleitete Ernährungstherapie muss regelmäßig auf ihre Wirksamkeit überprüft werden. Bei unzureichendem Erfolg (weitere Gewichtsabnahme) muss die Behandlung intensiviert werden. Reicht die orale Nahrungsaufnahme trotz Behandlung nicht aus, kommen künstliche, d. h. enterale oder parenterale Ernährungskonzepte infrage. Bei tumorbedingten gastrointestinalen Fehlfunktionen (z. B. Stenosen), bei therapiebedingten Störungen (z. B. Emesis, Diarrhö, Mukositis u. a.) oder anderen schweren Dünndarmstörungen ist eine enterale Ernährung oft nicht mehr möglich oder ausreichend wirksam. Die parenterale Ernährung ist dann die einzige Möglichkeit, dem Tumorpatienten die nötigen Nährstoffe zuzuführen.
46.5.6.8 Maßnahmen bei Ernährungsstörungen
Die Ernährungsstörungen, die während einer Chemo- oder Strahlentherapie auftreten, können durch vielfältige Maßnahmen und Informationen an die Betroffenen gelindert oder sogar beseitigt werden. Die folgenden Abschnitte geben Hinweise zur Ernährung.
Ernährung bei Kachexie
Folgende Maßnahmen werden empfohlen:
-
schmackhafte, optisch ansprechende, dem Patientenwunsch entsprechende hochkalorische nähr- und wirkstoffreiche Kost anbieten
-
individuelle Nahrungsaversion (z. B. Fleisch) berücksichtigen
-
häufig veränderte Geschmacksempfindung beachten
-
viele kleine kalorienreiche Mahlzeiten anbieten
-
pflanzliches Eiweiß bevorzugen (tierisches Eiweiß wird meist schlechter vertragen)
-
Wunschkost anbieten
-
gekochtem Gemüse Butter oder Sahne, Käsesaucen zusetzen
-
Pudding, Quark und Joghurtspeisen mit Sahne oder Eiscreme anreichern
-
zur Kalorienanreicherung Maltodextrin oder Honig einsetzen
-
Röststoffe und Kurzgebratenes anbieten (regen den Appetit an)
-
Mehlschwitze und kalorienreiche Gemüse- und Bratensauce zubereiten
-
energiereiche Brotaufstriche auf pflanzlicher Basis anbieten
-
falls gewünscht, panierte bzw. frittierte Speisen zubereiten
-
hochwertige Pflanzenöle und Margarine einsetzen
-
Snacks und Süßigkeiten für zwischendurch anbieten
-
Fertigprodukte mit 3,5 % Milch oder Sahne zubereiten
-
Cracker, kandierte Früchte, Nüsse, Trockenobst usw. verzehren (nicht bei Patienten mit Aplasie!)
-
Eiweißkonzentrate, Sojabohnengranulate, Pepsinwein und andere kraftspendende Speisen verzehren
-
in Gesellschaft essen
Appetitlosigkeit (Anorexie)
Definition
Hunger ist ein rein physiologisches Verlangen nach Nahrung. Es ist keine Krankheit und verschwindet bei der richtigen Ernährung.
„Appetit“ stammt vom Wort Appetenz und bedeutet im ursprünglichen Sinn Zuwendung. Im Gegensatz zu Hunger ist Appetit stimmungsabhängig und lustbetont (nach Juchli 1997).
Folgende Maßnahmen werden empfohlen:
-
immer dann essen, wenn man Lust und Appetit hat
-
Lieblingsspeisen aussuchen
-
stark riechende Speisen vermeiden
-
häufige und kleine Mahlzeiten anbieten
-
Zubereitung des Essens variieren
-
gehaltvoll frühstücken
-
zwischen den Mahlzeiten und nicht während des Essens trinken
-
kalorienreiche Naschereien bereithalten
-
für zwischendurch kühle Milchmixgetränke anbieten
-
Speisen appetitlich anrichten
-
appetitanregende Getränke (Sherry, Tees aus Wermut, Schafgarbe, Salbei) 10 Min. vor dem Essen trinken
-
für Ablenkung beim Essen sorgen
-
in Gesellschaft essen
-
körperliche Bewegung anregen
-
ggf. medikamentöse Therapie mit Gestagenen, Kortikosteroiden, Cannabinoiden
Verändertes Geschmack- und Geruchsempfinden
Vieles schmeckt anders als gewohnt. Die Wahrnehmung von süß, sauer, bitter, salzig kann sich verfälschen. Süße Speisen müssen häufig noch stärker gesüßt werden. Leibgerichte werden nicht mehr gegessen. Gerüche werden anders wahrgenommen. Häufig tritt ein Metallgeschmack bei bestimmten Chemotherapien auf.
Folgende Maßnahmen werden empfohlen:
-
Nahrungsmittel im Hinblick auf geschmackliche Akzeptanz berücksichtigen
-
starke Essensgerüche vermeiden (Abdeckungen der Speisen vor dem Auftragen entfernen)
-
neutrale Lebensmittel ohne starken Eigengeschmack auswählen (Brot, Kartoffeln, Teigwaren, Reis) → sind besser verträglich
-
wenn Fleisch zu bitter schmeckt, andere eiweißreiche Nahrungsmittel wählen
-
Speisen mit Kräutern, Kräutersalz, Gewürzen und Saucen abschmecken
-
Kaugummi zwischen den Mahlzeiten kauen
-
saure Nahrungsmittel und Getränke wählen, da sie den Schleim im Mund etwas lösen und so das Geschmacksempfinden verbessern
Völlegefühl und Blähungen (Tenesmen)
Bei Völlegefühl und Blähungen werden folgende Maßnahmen empfohlen:
-
Tees wie Pfefferminze, Kamille, Fenchel, Kümmel anbieten (lindern leichtere Beschwerden)
-
Küchenkräuter und Gewürze, wie Basilikum, Bohnenkraut, Dill, Liebstöckel, Koriander, Thymian, Anis, Wachholderbeeren und Zimt einsetzen
-
keine einengende Kleidung tragen und mit leicht erhöhtem Kopf schlafen
-
langsam essen und gut kauen
-
mehrere kleine Mahlzeiten anbieten
-
auf blähende Nahrungsmittel verzichten (Kohl, Zwiebeln)
-
Wärmflasche oder feuchte Wärme anbieten
-
Patienten zum Bewegen auffordern
Übelkeit und Erbrechen (Nausea und Emesis)
Bei Übelkeit und Erbrechen werden folgende Maßnahmen empfohlen:
-
starke Essensgerüche meiden, geruchsarme Zubereitungsarten wählen
-
kalte, erfrischende Speisen und Getränke anbieten
-
zwischen den Mahlzeiten viel, langsam und schluckweise (leicht gezuckerten) Tee, fettfreie Bouillon, kalte Getränke, z. B. Cola, trinken
-
Knäckebrot, Zwieback, Biskuits knabbern, evtl. schon vor dem Aufstehen
-
Reis, Kartoffeln, Teigwaren, Grieß, Mais, Milchprodukte sind besser verträglich
-
nach dem Essen Pfefferminztee trinken und eine Weile ausruhen
-
bei Sodbrennen den Kaffee- und Schwarzteegenuss, Nikotin- und Alkoholgenuss einschränken
-
Haferschleimsuppe, Grießbrei oder gekochtes Früchtekompott sind empfehlenswert
Verstopfung (Obstipation)
Bei Verstopfung werden folgende Maßnahmen empfohlen:
-
ballaststoffreiche Nahrungsmittel (Vollkornprodukte) essen
-
viel Flüssigkeit trinken, mind. 1,5 – 2,0 Liter täglich
-
für Bewegung sorgen (bei Bettlägerigkeit können leichte Muskelspannungs- und entspannungsübungen anregend wirken)
Verschiedene Naturprodukte haben eine leicht abführende Wirkung (Vorsicht bei Patienten mit Aplasie!):
-
Most, Traubensaft, Feigensaft, Pflaumensaft
-
über Nacht eingeweichtes Trockenobst
-
evtl. morgens auf nüchternen Magen ein Glas warmes Wasser oder Kaffee
Durchfall (Diarrhö)
Bei Durchfall werden folgende Maßnahmen empfohlen:
-
Flüssigkeits- und Mineralstoffverlust ersetzen durch:
-
reichlich Schwarztee (5 Min.), gesalzene Gemüsebrühe, Tomatensaft, verdünnte Fruchtsäfte (1:3)
-
Kümmel- Fenchel-, Brombeertee mit etwas Salz, Mineralwasser ohne Kohlensäure, Reiswasser
-
kaliumreiche Nahrungsmittel (Bananen, Aprikosen)
-
-
vorübergehende Fett- und ballaststoffarme Ernährung:
-
Früchte und Gemüse meiden
-
fein geraffelter Apfel (nicht bei Aplasiepatienten!)
-
gekochte Möhren, gedämpftes Gemüse, Zwieback
-
keine eisgekühlten Lebensmittel, keinen Kaffee und keine kohlensäurehaltigen Getränke
-
Mundtrockenheit (Xerostomie)
Bei Mundtrockenheit werden folgende Maßnahmen empfohlen:
-
wasserhaltige Nahrungsmittel (Obst, Obstkompotte, flüssige Milchprodukte, Suppen)
-
2-stündlich den Mund spülen
-
lauwarmer oder kalter Kamillen-, Salbei-, Thymian- oder Kräutermischtee, lauwarmes Wasser mit einer Prise Salz
-
gehackte Kräuter (regen den Speichelfluss an)
-
Zahnpasta und Mundwasser nach dem Zähneputzen gründlich wegspülen
-
immer etwas lutschen (z. B. Zitronenbonbons, Kaugummi, Ananasstücke, Eiswürfel)
-
reichlich Saucen zu den Speisen servieren
-
täglich die Lippen mit einer dünnen Schicht Vaseline eincremen
Kau- und Schluckbeschwerden (Dysphagie)
Bei Kau- und Schluckbeschwerden werden folgende Maßnahmen empfohlen:
-
feste, bröselige oder trockene Speisen meiden
-
Kleingeschnittenes, Weichgekochtes oder Püriertes bevorzugen (rutscht besser)
-
ideal sind weiche, milde Nahrungsmittel, wie Milchsuppen, Cremesuppen, weicher Käse, Joghurts, cremiger Quark, pürierte Kost, gekochte Salate
-
Gerichte lauwarm servieren
-
sehr heiße, stark gesalzene oder geräucherte Lebensmittel, saure Früchte und Säfte, alkoholische oder kohlensäurehaltige Getränke meiden
-
evtl. mit Strohhalm trinken
-
dickflüssige Getränke bevorzugen (vereinfachen den Schluckvorgang)
-
evtl. flüssige Lebensmittel andicken mit „ThickenUp“ oder „Thick&Easy“
46.5.6.9 Ernährung nach allogener und autologer Stammzelltransplantation
Patienten, die eine Hochdosis-Chemotherapie vor einer allogenen oder autologen Stammzelltransplantation erhalten haben, sind bis zum Anwachsen der Stammzellen im Knochenmark und bis zur Regeneration des Blutbilds (i. d. R. 2 – 3 Wochen) stark abwehrgeschwächt (Aplasie). Sie haben in dieser Zeit ein erhöhtes Risiko für Infektionen über Keime in Lebensmitteln. Um die Keimbelastung während dieser Zeit möglichst gering zu halten, müssen in diesem Zeitraum eine keimarme Ernährung und bestimmte Hygienerichtlinien eingehalten werden. Die Dauer der keimarmen Ernährung hängt von der Art der Transplantation, von der Anzahl der Blutzellen (Leukozyten, Granulozyten) und von krankenhausinternen Regelungen ab (KMT-Zentren, Umkehrisolation).
Ziel der Ernährung ist es, die Keimbelastung möglichst gering zu halten und trotzdem eine gesunde Ernährung zu gewährleisten.
Prävention und Gesundheitsförderung
Was bei der Zubereitung und beim Kochen beachtet werden muss:
-
vor der Essenszubereitung Hände waschen
-
Speisen aus einwandfreien Lebensmitteln oder Tiefkühlprodukte immer frisch zubereiten und sofort verzehren
-
kein frisches Obst und Gemüse (alles gekocht oder als Konserve)
-
Tees nur mit kochendem Wasser übergießen
-
keine Nüsse, keine Müslimischungen, keine Schokolade mit Nüssen, kein Vollkornbrot
-
kein rohes oder halbgares Fleisch (z. B. Mett, Tatar)
-
Hackfleisch am Einkaufstag verbrauchen
-
keinen Schimmelkäse, Mozzarella, Quark, Softeis
-
keine Holzbretter bei der Zubereitung benutzen (Keimbesiedelung)
-
Fleisch, Geflügel oder Fisch im rohen Zustand nicht mit anderen Lebensmitteln in Berührung bringen, besonders nicht mit solchen, die roh gegessen werden
-
Speisen nicht über längere Zeit warmhalten
-
zum Abschmecken immer saubere Löffel und Gabeln nehmen
-
Konservendosen vor dem Öffnen mit heißer Spüllauge abwaschen
-
Gewürze immer mitkochen
-
alles in den kleinstmöglichen Abpackungen kaufen
-
keine Mikrowelle benutzen (zerstört keine Bakterien)
-
auf absolute Sauberkeit achten (Arbeitsfläche, Geschirr, Kleidung)
-
Haltbarkeitsdatum beachten
-
Kühlkette bei Tiefkühlprodukten nicht unterbrechen
-
keine Lebensmittel in beschädigten Verpackungen oder mit geblähtem Deckel kaufen
-
angebrochene Lebensmittel im Kühlschrank innerhalb von 24 Std. verbrauchen
-
Lebensmittel vor Insekten schützen
46.6 Lern- und Leseservice
46.6.1 Literatur
[2386] Arends J. Tumorinduzierte Stoffwechselveränderungen und Tumorkachexie. Ursachen und Wirkungen sowie Diagnostik und Therapiekonzepte. Trava Care, Hrsg. Ausgabe 2005
[2387] Bäumer R, Maiwald A. Hrsg. Thiemes Onkologische Pflege. Stuttgart: Thieme; 2008
[2388] Bayerische Krebsgesellschaft e.V. Neutropenie. Unerwünschte Begleiterscheinung der Chemotherapie. München; 2005
[2389] Berger DP, Engelhardt R, Mertelsmann R. Das Rote Buch. Hämatologie und Internistische Onkologie. Landsberg/Lech: ecomed Medizin; 2006
[2390] Böhles H. Wasser-, Elektrolyt- und Säure-Basen-Haushalt. In Gortner L, Meyer S, Sitzmann FC. Hrsg. Duale Reihe Pädiatrie. 4. Aufl. Stuttgart: Thieme; 2012: 85–93
[2391] Bokemeyer C. Anämie bei Tumorpatienten. Lebensqualität verbessern – Transfusionen reduzieren, EORTC-Richtlinien 2007. Kombination von ESF mit iv. Eisen-Supplementation. Der Onkologe 2007; 13 (5), Beilage
[2392] Classen M et al. Innere Medizin. München: Urban & Fischer; 2003
[2393] Deutsche Gesellschaft für Hämatologie und Onkologie. Infektionen bei hämatologischen und onkologischen Erkrankungen (Stand Okt. 2004)
[2394] Gadner H et al. Pädiatrische Hämatologie und Onkologie. Heidelberg: Springer; 2006
[2395] Gutjahr P. Kurzlehrbuch Kinderkrebs. Pädiatrische Onkologie für Nicht-Onkologen. Aachen: Shaker Verlag; 2009
[2396] Hoehl M. Essen und Trinken. In: Hoehl M u. Kullick P. Hrsg. Gesundheits- und Kindekrankenpflege. 4. Aufl. Stuttgart: Thieme; 2012: 279–313
[2397] Juchli L. Pflege. 8. Aufl. Stuttgart: Thieme; 1997
[2398] Jürgens H et al. Übelkeit und Erbrechen bei onkologischen Patienten. Ein Kompendium für Pflegekräfte. GlaxoSmithKline; o. J.
[2399] Link H et al. Supportivtherapie bei malignen Erkrankungen. Köln: Deutscher Ärzte Verlag; 2005
[2400] Löser AP. Ambulante Pflege bei Tumorpatienten. Hannover: Schlütersche; 2000
[2401] Ludwig H, Luhan Ch. Knochenmarkdepression. In: Margulies A et al. Hrsg. Onkologische Krankenpflege. 4. Aufl. Heidelberg: Springer; 2006
[2402] MSD Sharp & Dohme GmbH. Fachinformation Emend (März 2016). Im Internet: http://www.msd.de/fileadmin/files/fachinformationen/emend.pdf; Stand: 18.12.2016
[2403] Pflege Heute. 5. Aufl. München: Urban & Fischer bei Elsevier; 2011
[2404] Phillips RS, Friend AJ, Gibson F, Houghton E, Gopaul S, Craig J V, Pizer B. Antiemetic medication for prevention and treatment of chemotherapy-induced nausea and vomiting in childhood 2016 DOI: 10.1002/14651858.CD007786.pub3 – Cochrane Library
[2405] Rinner B. Pflege von Kindern mit onkologischen Erkrankungen. In: Hoehl M u. Kullick P. Hrsg. Gesundheits- und Kinderkrankenpflege. 4. Aufl. Stuttgart: Thieme; 2012: 537–551
[2406] Richter, W. Schmerzdiagostik. Im Internet http://www.dgpsf.de/schmerzmessung.html; Stand: 18.12.2016
[2407] Robert Koch Institut. Richtlinien für Krankenhaushygiene und Infektionsprävention. Lieferung 21. München: Urban & Fischer bei Elsevier; 2003
[2408] Scholz N. Ernährung bei Krebserkrankung. Hilfestellungen, Tipps und Empfehlungen. 3. Aufl. GlaxoSmithKline; 2004
[2409] Schwegler J, Lucius R. Der Mensch. Anatomie und Physiologie. 6. Aufl. Stuttgart: Thieme; 2016
[2410] Silbernagl S, Despopoulos A. Taschenatlas der Physiologie. 7. Aufl. Stuttgart: Thieme; 2007
[2411] Stratton R. Behandlung krankheitsbedingter Mangelernährung. Eine Bestandsaufnahme, wie eine Ernährungstherapie Prognose und Kosteneffizienz positiv beeinflussen kann. Pfrimmer Nutricia; 2002
[2412] Wagner J, Hechel T, Hünseler C u. Zernikow B. Messen und Erfassen von Schmerz. In: Zernikow B. Hrsg. Schmerztherapie bei Kindern, Jugendlichen und jungen Erwachsenen. 5. Aufl. Heidelberg: Springer; 2015: 77–104
46.6.2 Weiterführende Literatur
[2413] Margulies A. et al. Hrsg. Onkologische Krankenpflege. 5. Aufl. Heidelberg: Springer; 2010
46.6.3 Internetadressen
[2414] http://deutschekrebshilfe.de; Stand: 18.12.2016
[2415] http://www.msd-gesundheit.de/erbrechen-nach-chemotherapie/; Stand: 18.12.2016
[2416] http://www.kok-krebsgesellschaft.de; Stand: 18.12.2016
[2417] http://www.krebsinformationsdienst.de; Stand: 18.12.2016
[2418] http://www.onko-kids.de; Stand: 18.12.2016