39.2.3.4 Ernährungsberatung
Es gibt mittlerweile für die meisten Gelenkerkrankungen spezifische Empfehlungen für eine angepasste Ernährung. Grundsätzlich sollten sich alle Betroffenen mit Übergewicht kalorienbewusst ernähren, da eine übermäßige Gewichtsbelastung die Gelenke zusätzlich schädigt.
Ernährung bei rheumatoider Arthritis
Nahrungsmittel tierischer Herkunft enthalten Arachidonsäure. Diese bildet entzündungsfördernde Botenstoffe und soll deshalb nicht oder nur in geringem Maße konsumiert werden. Umgekehrt wird versucht, mit Hilfe von Antioxidanzien (Vitamin C + E, Selen) die überschießende rheumatische Entzündungsreaktion einzudämmen.
Ernährungsempfehlungen
-
wenig Fleisch und Wurst, besser sind Gemüse, Obst und Nüsse
-
Einsatz magerer Milchprodukte und Reduktion fettreicher Käsesorten
-
2 Fischmahlzeiten pro Woche und Fischöl-Supplementierung
-
täglich zusätzlich 200 mg Vitamin E und 200 µg Selen
-
bei Risikogruppen (Senioren, postmenopausale Frauen, Kortisontherapie) Supplementierung von Kalzium (1000 mg/d) und Vitamin D (20 µg/d)
-
beim Kochen sollten schonende Zubereitungsmethoden und Garen bevorzugt werden, um die Vitamine und Spurenelemente in den Nahrungsmitteln zu erhalten
Ernährung bei Arthrose
Ernährungsempfehlungen
-
antioxidanzienreiche Ernährung: Gemüse, Obst und Nüsse
-
Beim Kochen sollten schonende Zubereitungsmethoden und Garverfahren bevorzugt werden, um die Vitamine und Spurenelemente in den Nahrungsmitteln zu erhalten.
-
Supplementierung von Knorpelnährstoffen (Chondroprotektiva): z.B. Glucosamin oder Chondroitinsulfat
-
Bei den schweren Formen einer „aktivierten Arthrose“ gelten die gleichen Empfehlungen wie bei der rheumatoiden Arthritis.
Medikamente und Ernährung
Der Patient erhält mehrere kleine Mahlzeiten am Tag. Damit werden folgende Ziele verfolgt:
-
korrekte Medikamenteneinnahme
-
verringerten Appetit kompensieren
-
Magenbeschwerden reduzieren
-
Durch die Kortisongabe kann sich ein steroidinduzierter Diabetes mellitus ausbilden, der eine Diabeteskost nach sich zieht.
-
Flüssigkeitszufuhr: Diese sollte der Aktualität des Krankheitsgeschehens angepasst werden. Bei gleichzeitiger Kortisongabe und entsprechender Disposition wird eine ▶ 24-Stunden-Bilanzierung durchgeführt.
Arzneimittel im Fokus
Kortison
Bei Kortisonpräparaten ist der Zeitpunkt der Einnahme dem physiologischen Produktionsrhythmus anzupassen. In den meisten Fällen ist eine frühe Gabe gegen 7.00 Uhr morgens indiziert. Dem Patienten wird gleichzeitig eine kleine Mahlzeit gereicht.
Nichtsteroidale Antirheumatika
Sie werden morgens nach dem Frühstück und abends vor dem Schlafengehen in Verbindung mit einer kleinen Mahlzeit verabreicht. Die Medikamente sollten nicht unmittelbar vor dem Zubettgehen und nicht im Liegen genommen werden, um eine Reizung der Speiseröhre durch einen möglichen Reflux zu vermeiden.
Antazida
Säurebindende Magenmittel werden zwischen den Mahlzeiten und niemals zusammen mit anderen Arzneimitteln eingenommen.
Prävention und Gesundheitsförderung
Eine Ernährungsberatung ist von großer Bedeutung, um einen individuellen Kostplan erstellen zu können. Den Patienten werden wertvolle Tipps für die weitere Ernährung zu Hause vermittelt.
39.2.3.5 Naturheilkundliche Behandlungsprinzipien
Neben der Schulmedizin werden auch häufiger naturheilkundliche Behandlungsprinzipien in Erwägung gezogen. Die Pflegeperson sollte den Therapieansatz als Ausdruck einer ganzheitlichen Betrachtungsweise kennen. Auch wenn für die meisten Methoden kein sicherer Wirkungsnachweis geführt werden kann, so können die Betroffenen im Einzelfall sehr von solchen Angeboten profitieren:
Akupunktur Die Traditionelle Chinesische Medizin bildet die Grundlage für die Akupunktur. Sie darf nicht als Einzeltherapie aufgefasst werden, sondern als ein Baustein im Therapiekonzept. Die Akupunktur zählt nicht zu den klassischen Naturheilverfahren, kann aber ergänzend zu naturheilkundlichen Behandlungen eingesetzt werden.
Ausleitende Verfahren Hierzu gehören z. B. das blutige und unblutige Schröpfen und die Blutegeltherapie. Sie sollen das Immunsystem stimulieren, die Schmerz- und Entzündungsauslöser ausschalten und die Stoffwechseltätigkeit verbessern.
Eigenblutinjektionen Sie regen die Selbstheilungskräfte des Körpers an. Es kommt zu einer sog. Umschaltung. Aus einer Vene wird Blut entnommen, das dem Patienten später wieder subkutan oder intramuskulär injiziert wird. Dabei kann das Blut zuvor verändert werden, z. B. durch Aktivierung oder Potenzierung.
Neuraltherapie Die Neuraltherapie beseitigt Störfelder im Körper. Dabei wird in bestimmte Stellen des Körpers ein Lokalanästhetikum injiziert. Es kann auf den Gesamtorganismus wirken und eine positive Wirkung auf den Heilungsprozess erzielen.
Phytotherapie Die ▶ Phytotherapie ist ein sehr weitreichendes Behandlungsfeld, bei der pflanzliche Wirkstoffe zur Anwendung kommen.
Hydrotherapie Wasser als therapeutisches Mittel ist seit je bekannt. Die Hydrotherapie erreichte einen besonderen Stellenwert durch die Behandlungskonzepte von Kneipp. Die morgendliche kühle Waschung nach kneippschen Prinzipien verbessert die Durchblutung und fördert die Stoffwechseltätigkeit. Die lokale Anwendung ca. 42 °C warmer, feuchter Heublumensäcke wirkt schmerzlindernd.
Heliotherapie Die positive Wirkung des Sonnenlichts macht sich die Heliotherapie zunutze. Die Behandlung mit natürlichem oder künstlich erzeugtem Sonnenlicht bewirkt eine Steigerung der Abwehrkräfte. Zudem ist die positive Beeinflussung der psychischen Befindlichkeit von großer Bedeutung.
Merke
Heublumensäcke und heliotherapeutische Anwendungen dürfen nicht im akuten Schub angewendet werden.
39.3 Pflege von Patienten mit Erkrankungen der Bandscheiben
Anatomie und Physiologie im Fokus
(nach Schwegler u. Lucius 2016)
Wirbelsäule und Bandscheiben im Überblick
Wirbelsäule
Die Wirbelsäule ist ein komplexes Gebilde. Sie besteht aus Wirbeln, Bandscheiben und verbindenden Bandsystemen ( ▶ Abb. 39.12). Die Wirbel besitzen jeweils 4 Wirbelgelenke. Zwischen 2 Wirbelkörpern, also in unmittelbarer Nähe der Bandscheiben, treten einzelne Nerven aus. Wichtig für die Beweglichkeit und die aktive Stabilisierung der Wirbelsäule ist die Rücken- und Rumpfmuskulatur.
Wirbelsäule.
Abb. 39.12 a Längsschnitt der Wirbelsäule, b ein Lendenwirbel von der Seite, c von oben gesehen.

Die Wirbelsäule besteht aus insgesamt 24 freien Wirbeln – 7 Halswirbeln, 12 Brustwirbeln, 5 Lendenwirbeln –, dem aus 5 Wirbeln zusammengewachsenen Kreuzbein (Os sacrum) und dem Steißbein (Os coccygis). Die Wirbel werden von oben nach unten nummeriert, also C1–C7, Th1–Th12, L1–L5. Es gibt in der Längsachse 4 Krümmungen: Hals- und Lendenlordose nach vorne und Brust- und Sakralkyphose nach hinten ( ▶ Abb. 39.12 a).
Bandscheiben
Es gibt 23 Bandscheiben. Zwischen dem Schädel und dem ersten Halswirbel sowie zwischen dem ersten und zweiten Halswirbel sind keine. Die Bandscheiben machen etwa 25 % der Gesamtlänge der Wirbelsäule aus. Eine Bandscheibe ist durchschnittlich 7 bis 12 Millimeter hoch und zur Mitte hin flacher als an den Rändern. Sie wird von Bändern gehalten.
Die Bandscheiben sind flexible Verbindungen zwischen den Wirbelkörpern, die einerseits ein Abkippen bzw. eine Rotationsbewegung der Wirbelsäule gestatten, andererseits für einen festen Halt der Wirbelkörper aufeinander sorgen. Sie dienen darüber hinaus als Puffer gegen kurze, harte Stöße. Jede Bandscheibe gleicht einem Sandwich mit zwei festen Platten aus hyalinem Knorpel, zwischen denen sich ein derber, zwiebelschalenähnlicher Faserring (Anulus fibrosus) um einen zentralen Gallertkern (Nucleus pulposus) herum ausbreitet ( ▶ Abb. 39.12 b, c). Der Gallertkern zieht aufgrund seiner hohen osmotischen Konzentration Wasser aus der Umgebung an und schwillt in unbelastetem Zustand (im Liegen, unter Wasser, in Schwerelosigkeit) an. Dadurch verlängert sich die Wirbelsäule um bis zu 2 cm und der Faserring gerät unter Spannung. Quetscht man den Gallertkern zusammen (Druckbelastung), dann versucht er seitlich auszuweichen. Die gitterartig vernetzten kollagenen Fasern des Faserrings werden gedehnt und der Faserring buckelt sich über den Rand der Wirbelkörper hinaus vor.
Die Bandscheiben besitzen keine Blutgefäße. Durch ihre ständige Be- und Entlastung werden sie mit Nährstoffen versorgt und sind in der Lage, Stoffwechselabfallprodukte wieder abzugeben (Ernährung durch Diffusion).
39.3.1 Medizinischer Überblick Bandscheibenvorfall
39.3.1.1 Definition
Bei einem Bandscheibenvorfall (auch Bandscheibenprolaps = BSP oder Diskusprolaps genannt) verlagert sich das Gewebe des zentralen Gallertkerns (Nucleus pulposus) oder das Gewebe tritt durch Risse im äußeren Ring (Anulus fibrosus) aus ( ▶ Abb. 39.13).
Bandscheibenprolaps.
Abb. 39.13 Der Nucleus pulposus prolabiert in den Spinalkanal.
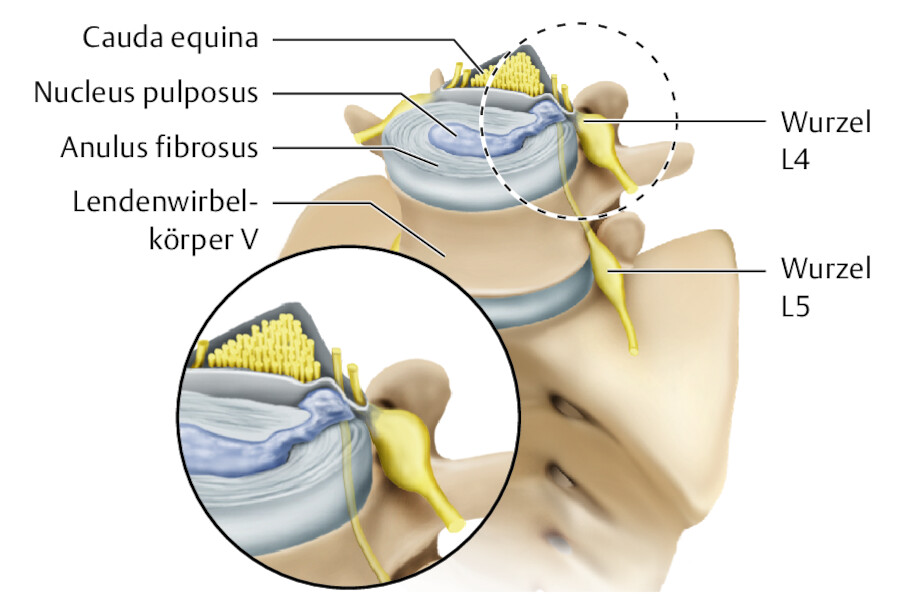
Ein Bandscheibenvorfall tritt am häufigsten auf
-
an der Lendenwirbelsäule (LWS – meistens zwischen L 4/L 5 oder L 5/S 1), nach Schätzungen gibt es 120000 Patienten pro Jahr in Deutschland,
-
an der Halswirbelsäule (HWS – meistens zwischen C 6 und C 7),
-
die Brustwirbelsäule (BWS) ist sehr selten betroffen.
39.3.1.2 Klassifikation
Art und Größe des Vorfalls
-
Protrusion: Der innere Gallertkern wölbt sich vor, ohne den äußeren Faserring zu durchdringen
-
Prolaps (Bandscheibenvorfall): Der innere Gallertkern tritt durch den äußeren Faserring hindurch
-
Sequester: Vorfall mit Absprengungen ohne Verbindung zur Bandscheibe
Lage des Vorfalls Je nach der Austrittsrichtung kann das Bandscheibengewebe auf einen Nerven drücken (komprimieren):
-
medialer Bandscheibenvorfall → Gewebe tritt in Richtung Spinalkanal aus, meist ohne Nervenwurzelkompression
-
lateraler Bandscheibenvorfall → Gewebe tritt in die Zwischenwirbellöcher aus
-
medio-lateraler Bandscheibenvorfall → Gewebe tritt zwischen Zwischenwirbellöchern und Spinalkanal aus und kann auf eine Nervenwurzel drücken
39.3.1.3 Ursachen
Günstige Bedingungen für einen Bandscheibenvorfall sind:
-
vorgeschädigte Bandscheiben: Die Elastizität der Bandscheibe nimmt ab; es entstehen Risse im Anulus fibrosus.
-
mechanische Belastungen: „falsche“, dauerhafte oder einseitige Belastung, z. B. plötzliche Rotationsbewegungen (Drehbewegungen) des Rumpfes beim Aufstehen
-
ungenügend ausgeprägte, verhärtete oder verkrampfte Muskulatur an Rücken und Bauch: Sie kann u. a. durch falsche Haltung, langes Sitzen, zu enge Kleidung, falsches Schuhwerk und psychische Belastungssituationen auftreten.
39.3.1.4 Symptome
Allgemeine Symptome
Allgemeine Symptome eines Bandscheibenvorfalls sind Schmerzen, Fehlhaltungen, Parästhesien (Taubheitsgefühl)
-
im Kopf- und Nackenbereich und in den oberen Extremitäten (bei Bandscheibenvorfällen in der HWS),
-
in der unteren Rückenpartie und den unteren Extremitäten (bei Bandscheibenvorfällen in der LWS),
-
sehr selten im Thoraxbereich (Bandscheibenvorfälle in der BWS).
Schmerzarten Typische Schmerzarten sind:
-
starke, kontinuierliche oder rezidivierende Kreuzschmerzen, da der Vorfall gegen das hintere Längsband drückt: Ist die HWS betroffen, sind es heftige Nackenschmerzen, die in den Kopf und/oder die Arme ausstrahlen.
-
Lumbago („Hexenschuss“): Der Schmerz tritt durch die Muskelverspannung/-verhärtung im Bereich der gesamten LWS auf.
-
Ausstrahlende Schmerzen im Versorgungsgebiet eines Nervs, z. B. des Nervus ischiadicus (Ischialgie): Schmerzen und Parästhesien strahlen in Gesäß und Oberschenkel aus, evtl. bis in den Unterschenkel und den Fuß.
-
Schmerzen, die durch die Schon- oder Zwangshaltung auftreten.
-
Lasègue-Zeichen (gehört zur körperlichen Untersuchung durch den Arzt): Beim passiven Anheben des im Kniegelenk gestreckten Beines werden die Nervenwurzeln zusätzlich angespannt, sodass sich der Schmerz im Gesäß und Oberschenkel charakteristischerweise verstärkt.
Parästhesien, Sensibilitätsstörungen und Lähmungen Diese sind typischerweise mit dem Versorgungsgebiet des eingeengten Nervs verbunden. Es gibt sogenannte Dermatome (von einer Spinalnervenwurzel versorgtes Hautsegment) und Kennmuskeln (Muskeln, deren isolierte Lähmung auf die Schädigung bestimmter Spinalnerven hinweist). Bestimmte pathologische Reflexe sind auch möglich ( ▶ Tab. 39.1 ).
|
Wurzel |
Kennmuskel |
abgeschwächte Funktion |
Reflex |
Sensibilitätsstörung |
|
L 3 |
Schenkel- und Kniestrecker |
Fersenstand |
Patellarsehnen-Reflex |
Vorderseite Oberschenkel bis Innenseite Knie |
|
L 4 |
Schenkel- und Kniestrecker, Fußheber |
Fersenstand, Hebung und Supination des Fußes |
Patellarsehnen-Reflex |
Außenseite Oberschenkel, Vorderseite Unterschenkel, innerer Fußrücken |
|
L 5 |
Fußheber, Großzehenstrecker, Hüftmuskel |
Fersenstand, Großzehenhebung gegen Widerstand |
Tibialis-posterior-Reflex |
Außenseite Ober- und Unterschenkel, Fußrücken bis Großzehe |
|
S 1 |
Waden- und Hüftmuskel |
Zehenstand |
Achillessehnen-Reflex |
Rückseite Ober- und Unterschenkel, äußerer Fußrand |
Schwerste Ausprägungen
Kaudasyndrom Komprimiert der Bandscheibenvorfall die ganze Cauda equina (das Rückenmark endet bei L 2, danach beginnt die Cauda equina), wird vom Kaudasyndrom gesprochen. Symptome sind
-
heftige Schmerzen,
-
Blasen- und Mastdarmstörungen,
-
bei Männern Potenzstörung,
-
Taubheitsgefühl in der Analregion und an der Innenseite der Oberschenkel (Reithosenanästhesie),
-
schlaffe Lähmung beider Beine.
Konussyndrom Tritt die Schädigung bei L 1 oder 2 auf, wird von einem Konussyndrom gesprochen. Anzeichen dieses Syndroms sind
-
Blasen- und Mastdarmstörungen,
-
Sensibilitätsstörungen und
-
selten Lähmungen.
Merke
Bei Blasen- und Mastdarmstörungen in Verbindung mit einer Reithosenanästhesie immer an ein Kaudasyndrom denken (Info an den Arzt). Wegen der Möglichkeit irreversibler Schäden muss beim Kauda- bzw. Konussyndrom sofort operiert werden.
Komplikationen
Medio-laterale Vorfälle Schädigungen, die länger bestehen, können zu dauerhaften Beschwerden, v. a. Paresen (Lähmungen), führen.
Mediale Vorfälle In seltenen Fällen kann der Bandscheibenvorfall so weit auf das Rückenmark drücken, dass die Gefahr einer mehr oder weniger ausgedehnten ▶ Querschnittsymptomatik besteht. Ein nicht oder zu spät operiertes Kaudasyndrom kann eine bleibende Blasenlähmung zur Folge haben.
39.3.1.5 Diagnostik
Zu den diagnostischen Maßnahmen zählen:
-
Anamnese
-
körperliche Untersuchung
-
MRT (Magnetresonanztomografie) oder Kernspintomografie ( ▶ Abb. 39.14)
-
Röntgen: Zum Nachweis eines Bandscheibenvorfalls nicht geeignet, hiermit lassen sich nur knöcherne Strukturen darstellen.
Bandscheibenvorfall.
Abb. 39.14 2 Vorfälle zwischen LWK 4 und 5 sowie zwischen LWK 5 und Sakralwirbelkörper SWK 1.
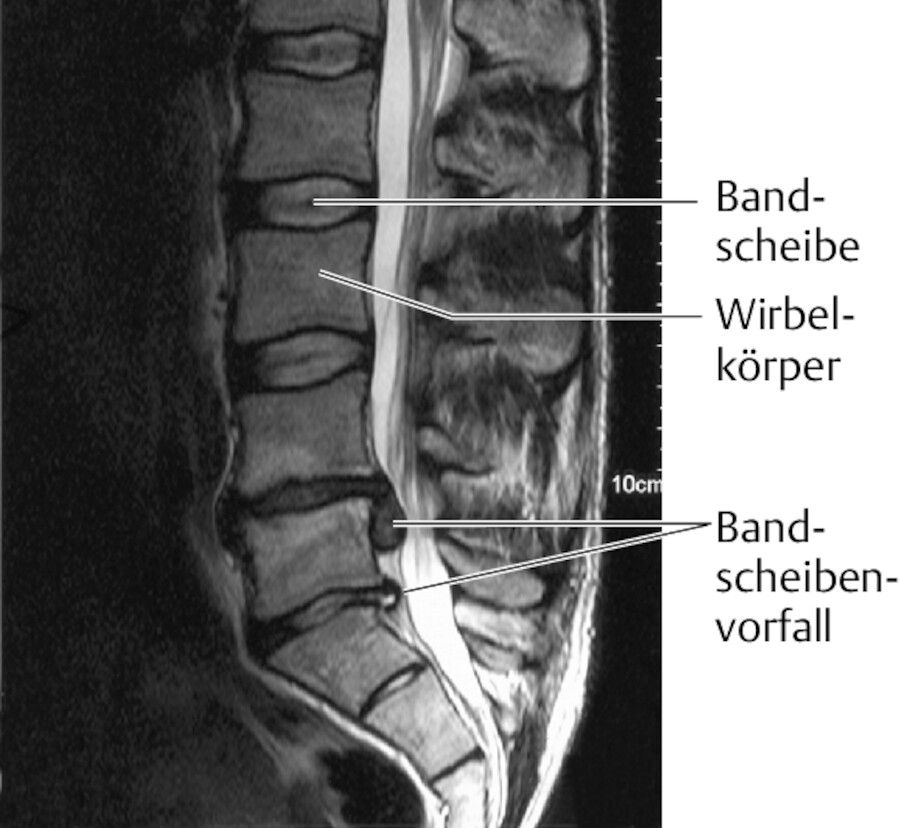
Differenzialdiagnosen
-
Degenerative Wirbelgelenksveränderungen (Arthrosen) verursachen hauptsächlich schmerzhafte Beschwerden. In schweren Fällen können knöcherne Neubildungen auf das Rückenmark drücken (Spinalkanalstenosen).
-
Wirbelgelenksblockaden (Verschiebungen der Wirbelkörper gegeneinander) können muskulären Hartspann verursachen und auch ohne Nervenwurzelkompression schmerzhaft ausstrahlen („Hexenschuss“).
-
osteoporotische Frakturen oder Tumoren an der Wirbelsäule
39.3.1.6 Therapie
Konservative Behandlung
Hat der Patient keine neurologischen Ausfälle, wird er zunächst konservativ behandelt. Dabei werden folgende Ziele verfolgt:
-
Entlastung der Wirbelsäule (Muskulatur, Bandapparat, Bandscheiben)
-
Schmerzbeseitigung
-
Wiederherstellung von Beweglichkeit, Koordination und Kraft des Patienten
Medikamentöse Therapie Hierzu gehören:
-
Schmerzmittel mit entzündungshemmender Wirkung (nichtsteroidale Antiphlogistika, z. B. Diclofenac, Ibuprofen)
-
allgemeine Schmerzmittel (z. B. Paracetamol, Opiate)
-
muskelentspannende Medikamente (z. B. Diazepam)
-
lumbale Wurzelinfiltration: Ein Lokalanästhetikum wird in Kombination mit Kortison an die Nervenaustrittsstelle im Bereich der Zwischenwirbellöcher injiziert (evtl. unter computertomografischer Kontrolle).
Physikalische Therapie Dazu gehören:
-
Bettruhe in der akuten Schmerzphase
-
Entlastungs- oder Stufenlagerung ( ▶ Abb. 39.5)
-
lokale Wärme (Fango, Aconit-Öl- oder Arnika-Wickel)
-
Kälteanwendungen, Massagen, Hydrotherapie
-
Elektrotherapie, z. B. ▶ TENS
-
lokale Salbenanwendung
Die Pflegeperson beobachtet die Bewegungsabläufe des Patienten und macht ggf. auf ungünstige Bewegungen aufmerksam.
Merke
Die Physiotherapie ist von zentraler Bedeutung. Nach der akuten Schmerzphase ist ein systematisches regelmäßiges Aufbau- und Entspannungstraining für Rücken- und Bauchmuskulatur angezeigt.
Der weitere Behandlungsverlauf der konservativen Therapie beinhaltet:
-
langsame Mobilisation unter Anleitung
-
Stufenbettlagerung reduzieren
-
Rücken- und Bauchmuskulatur stärken
-
Bewegungsübungen durchführen
-
Medikamente reduzieren, auf orale Applikation umstellen
-
physikalische Maßnahmen reduzieren oder umstellen
-
Entlassungsmanagement
Alternative Behandlungskonzepte Neben der klassischen konservativen Therapie gibt es alternative Therapieformen, die eine zusätzliche Linderung der Beschwerden bewirken können: Entspannungstechniken, fernöstliche Heilmethoden oder Homöopathie.
Operative Behandlung
Patienten mit einem nachgewiesenen Bandscheibenvorfall müssen operiert werden, wenn
-
ausgeprägte Paresen akut einsetzen (Lähmung, z. B. des Zehenhebers),
-
Schmerzen plötzlich wieder verschwinden und gleichzeitig Lähmungserscheinungen auftreten,
-
Schmerzen anhalten und leichte Ausfallerscheinungen trotz konsequent durchgeführter konservativer Therapie auftreten,
-
ein Konus- bzw. Kaudasyndrom besteht.
Ein Bandscheibenvorfall ohne Beschwerden ist keine Indikation zur OP.
Die Art des Eingriffs ist abhängig von der Lokalisation des Vorfalls, vom Zustand des Anulus fibrosus und von weiteren Befunden (z. B. einer Spinalkanalstenose). Bei ca. 10% der Patienten bringt eine Operation keine Besserung!
Es gibt diverse Operationsansätze:
-
Ziel ist die gezielte Entfernung oder Auflösung der Anteile der Bandscheibe, die den Nerv komprimieren, bei Erhaltung der gesunden Bandscheibe.
-
Heute werden verbreitet „Schlüsselloch-Operationstechniken“ angewandt (z.B. mikrochirurgische Nukleotomie mit Endoskop und Mikroskop).
-
Es gibt diverse Techniken zur Stabilisierung der Wirbelsäule (Bandscheibenprothesen, Knochenspäne oder Knochenzement).
-
Bei kleineren Bandscheibenvorfällen werden minimalinvasive Verfahren (z.B. Verdampfung der Bandscheibe mit einer Laser-Sonde) eingesetzt.
39.3.2 Pflege- und Behandlungsplan
Patienten mit Bandscheibenvorfällen kommen häufig erst dann stationär ins Krankenhaus, wenn konservative Maßnahmen nicht mehr wirkungsvoll sind und nur eine Operation helfen kann.
Fallbeispiel
Herr Bertram ist 44 Jahre alt und steht mitten im Leben. Er ist Familienvater, berufstätig und geht vielen Hobbys nach. Aber seit 3 Jahren quälen ihn immer wieder Kreuzschmerzen und ziehende Schmerzen, die ins rechte Bein ausstrahlen. Zweimal war er in der Vergangenheit für mehrere Wochen krankgeschrieben. Beim ersten Mal wurde ein Bandscheibenvorfall L 4/L 5 diagnostiziert. Herr Bertram entschied sich für die konservativen Therapie. Diese linderte seine Beschwerden. Jedoch kam es immer wieder zu Rückfällen. Nun hat sich Herr Bertram zur Operation entschlossen, weil die Erkrankung sein Leben immer mehr veränderte. Herr Bertram ist leicht übergewichtig, raucht und trägt gern legere Kleidung, weil er durch enge Kleidung eher Rückenschmerzen bekommt. Er hat keine weiteren Erkrankungen und erhofft sich von der OP eine endgültige Heilung seiner Beschwerden.
39.3.2.1 Präoperative Vorbereitung
Dem Patienten werden Informationen zum gesamten Aufenthalt gegeben.
Bewegung Der Patient wird angeleitet beim
-
Umgang mit dem Steckbecken in Seitenlage,
-
rückenschonenden Bewegen im Bett und
-
En-bloc-Aufstehen ( ▶ Abb. 39.15).
En-bloc-Mobilisation.
Abb. 39.15 Das wirbelsäulenschonende Aufstehen sollte der Patient schon präoperativ einüben.
(Foto: M. Niethammer, Thieme)
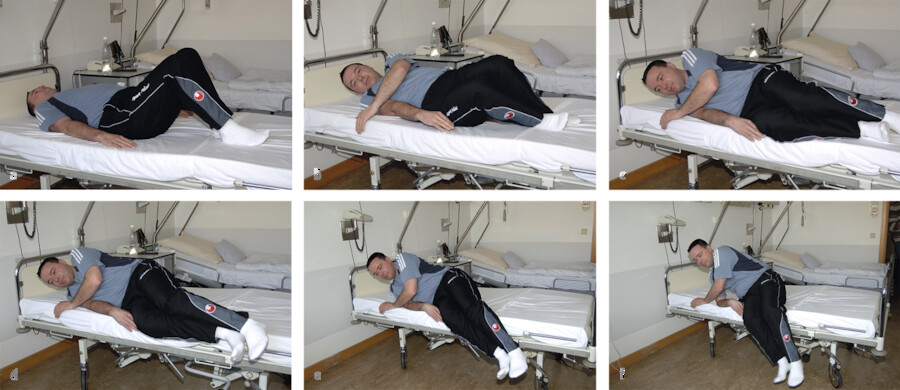
Lagerung Zur Schmerzreduktion und besseren Positionierung können dem Patienten Lagerungskissen angeboten werden. Meist bringt der Patient eigene Kissen mit.
OP-Vorbereitung Die Rasur erfolgt kurz vor der OP und ist abhängig von der Operationstechnik. Viele HWS-Bandscheibenvorfälle werden mikrochirurgisch von vorn operiert. Entsprechende allgemeine Operationsmaßnahmen sind im Abschnitt ▶ „Vorbereitung am Vortag“ beschrieben.
39.3.2.2 Postoperative Versorgung
Operationstag
Es gelten die allgemeinen ▶ postoperativen Maßnahmen, z. B. Prophylaxen, Vitalzeichenkontrolle und Infusionsüberwachung.
Positionierung/Lagerung Je nach Arztanordnung und durchgeführter OP kann der Frischoperierte postoperativ für einige Stunden auf den Rücken gelagert werden, um die Wunde zu komprimieren. Zur Entlastung des Rückens werden die Knie mit Lagerungskissen unterstützt. Gegen Abend kann eine Lageveränderung erfolgen, indem der Patient sich mittels erlernter En-bloc-Technik in die Seitenlage rollt. Die Pflegeperson unterstützt ihn dabei und stützt seinen Rücken und das obenliegende Bein mit einem Kissen ab. Bei zervikalen Vorfällen werden Kopf und Schultern in Zentralstellung auf einem großen Kissen gelagert.
Überwachung Maßnahmen sind:
-
Motorik und Sensibilität überprüfen (HWS: Arme, LWS/BWS: Beine)
-
Lage der Hilfsmittel zur externen Stabilisierung der Wirbelsäule, z. B. Zervikalstütze, kontrollieren
-
Blasen- und Mastdarmfunktion überwachen
-
Verbände und Redons kontrollieren (Nachblutungsgefahr), Redon gut abpolstern (Dekubitusgefahr)
Merke
Die Blasenfunktion ist ein wichtiger postoperativer Parameter (Überwachungsmerkmal) zur Früherkennung von Komplikationen im OP-Gebiet. Unter anderem deswegen erhalten die Patienten prä- oder intraoperativ keinen transurethralen Dauerkatheter.
Pflege in den Folgetagen
Körperpflege Die Grundpflege wird nach Arztanordnung anfangs im Bett in Rücken- bzw. Seitenlage durchgeführt. Je nach Zustand und Ressourcen unterstützt die Pflegeperson den Patienten.
Praxistipp
Prinzipiell sollte der Patient eher stehen als sitzen, d. h. die Grundpflege möglichst stehend am Waschbecken durchführen.
Bewegung Die Mobilisation beginnt i. d. R. am ersten postoperativen Tag (unter Anleitung der Physiotherapeuten) und hängt von der durchgeführten Operation ab. Dabei wird auch hier die En-bloc-Methode favorisiert, die schon präoperativ erlernt wurde (s. ▶ Abb. 39.15). Die Bewegungen sollen beim Aufstehen, Hinlegen und Drehen immer gleichmäßig und in einem Zug erfolgen.
Der Patient sollte sich nicht überfordern und nur kurze Strecken zurücklegen. Er sollte häufiger Ruhepausen im Bett einlegen. Je nach Allgemeinzustand wird die Anforderung gesteigert. Der Patient sollte noch keine Treppen steigen.
Da Liegen und Stehen für die operierte Bandscheibe besser ist als Sitzen, wird dem Patienten empfohlen, auch im Stehen zu essen. Hilfsmittel stehen zur Verfügung.
Prävention und Gesundheitsförderung
Evtl. verwendete Zervikalstützen, die zur Entlastung und Immobilisierung dienen, sollten spätestens nach zwei Wochen abtrainiert werden, weil sich die Muskulatur der HWS sonst daran gewöhnt.
Merke
Der Druck, den die Bandscheiben aushalten müssen, ist sehr unterschiedlich. Je nach Körperhaltung und Tätigkeit lasten auf der Lendenwirbelsäule bei Normalgewichtigen 25 kg in Rückenlage, 85 kg beim Gehen, 100 kg beim Stehen, 140 kg im Sitzen und 175 kg im nach vorne gebeugten Sitzen auf den Bandscheiben der Lendenwirbelsäule.
OP-Wunde Das Sekret in den Redon-Drainagen wird auf Menge und Farbe hin, die Redonflasche auf den Sog hin beobachtet, bei Bedarf werden die Redonflaschen gewechselt. Der behandelnde Arzt zieht die Drainagen üblicherweise nach 24 Stunden.
Merke
Fließt Liquor (Liquor cerebrospinalis = Gehirn-Rückenmark-Flüssigkeit) in die Redon-Drainage, wird der Sog entfernt und die Redonflasche dauerhaft belüftet. Der Arzt muss informiert werden.
Krankenbeobachtung Schmerzen, motorische Schwäche und Taubheitsgefühl werden erfasst.
Ausscheidung Die Darmausscheidung wird medikamentös unterstützt, um ein übermäßiges Pressen zu verhindern.
Physiotherapie Die Physiotherapie spielt eine zentrale Rolle in der postoperativen Behandlung. Angeboten werden
-
Rücken- und Bauchmuskulaturtraining,
-
Rückenschule,
-
Entspannungsgruppen,
-
Bewegungsbad und
-
manuelle Therapie.
39.3.2.3 Entlassungsberatung
Im Anschluss an den Krankenhausaufenthalt wird eine Anschlussheilbehandlung empfohlen, die auch ambulant durchgeführt werden kann. In manchen Fällen hat eine Bandscheibenerkrankung Konsequenzen auf die ausgeübte berufliche Tätigkeit. Der Sozialdienst im Krankenhaus oder eine weiterführende Rehabilitationseinrichtung berät zu den Themen:
-
Veränderungen am Arbeitsplatz
-
Berufsunfähigkeit/Umschulung
-
Erwerbsunfähigkeit
Weitere Beratungsinhalte betreffen die Themenbereiche:
-
Bewegung und Ernährung
-
rückenschonende Maßnahmen im Alltag
-
Selbsthilfe bei Lumbago
Prävention und Gesundheitsförderung
Der Patient wird über Aktivitäten informiert, die er zumindest eine Zeit lang nicht ausüben sollte:
-
in den ersten Tagen: kein Treppensteigen
-
in den ersten Wochen: keine Seitenlage oder erhöhtes Kopfteil
-
mehrere Wochen: kein längeres Sitzen und längeres Stehen
-
bis zu 3 Monate: kein Heben von über 5 – 10 kg Gewicht (ärztliche Empfehlung beachten)
Bewegung und Ernährung
Dem Patienten werden weitere krankengymnastische Übungen empfohlen. Dabei sollte beachtet werden, dass sowohl Bauch- als auch Rückenmuskulatur trainiert werden und die Muskulatur gedehnt und gekräftigt wird. Wichtig ist, dass ein regelmäßiges Training stattfindet. Übergewicht sollte vermieden und wenn vorhanden, reduziert werden.
Rückenschonende Maßnahmen im Alltag
Die Rückenschule ohne rückengerechte Alltagsbewegungen wird keinen Behandlungserfolg erzielen. Deshalb gilt es, die gelernten Übungen auch im Alltag einzusetzen.
Arbeitsplatz Ergonomische und wechselnde Sitzpositionen sollten ermöglicht werden. Zwangshaltungen und länger andauernde Bandscheiben-Belastungen müssen vermieden werden. Abwechslung ist gefragt (z.B. Stehpult, höhenverstellbare Arbeitstische). Optimal wären mehrmals täglich kurze Pausen mit Übungen zur Rückenschule.
Sportarten Empfehlungen können Sie ▶ Tab. 39.2 entnehmen. Generell nicht geeignete Sportarten sind Judo, Skifahren, Ballspiele wie Tennis, Fußball, Handball, Volleyball.
|
Postoperativer Zeitrahmen |
Belastungsformen |
|
1. Tag |
Schonung und Ruhe |
|
2.–14. Tag |
rumpfstabilisierende Übungen aus der Entlastungshaltung, Rückenschwimmen, Aquajogging, Gehen, Training auf dem Fahrradergometer |
|
2.–12. Woche |
rumpfstabilisierende Übungen aus der Entlastungshaltung, Rückenschwimmen, Wandern, Nordic Walking, Fahrradfahren mit „Gesundheitslenker“ |
|
3.–6. Monat |
rumpfstabilisierende Übungen mit leichten Zusatzgewichten, Medizinische Trainingstherapie, Schwimmen, Radfahren, Skilanglauf, Joggen, Tennis, Reiten |
|
nach 6 Monaten |
volle Belastungsfähigkeit, Krafttraining unter Beachtung der Rückenschulregeln |
Hilfsmittel Das rückenschonende Arbeiten und entsprechende Maßnahmen werden ausführlich im Kapitel „ ▶ Unterstützung der Mobilisation“ dargestellt. Dem Patienten stehen weiterhin verschiedene Hilfsmittel zu Verfügung, die ihm das „rückenschonende“ Leben erleichtern können:
-
Sitz-Steh-Hilfen
-
Stehpulte
-
Verlängerungen
-
ausreichend hohe Arbeitstische
Kleidung Wichtig ist es auch, dass der Patient seine Kleidung so anpasst, dass sie der normalen Anatomie entspricht. Auf einengende Jeans und besonders wärmende Kleidung (Leibchen für die LWS) im Rückenbereich sollte verzichtet werden. Durch das ständige Wärmen einzelner Körperregionen wird die Muskulatur zu empfindlich.
Prävention und Gesundheitsförderung
Es empfiehlt sich, gute Schuhe mit elastischer Sohle und gutem Sitz zu tragen, die nicht zu eng sind und keine hohen Absätze haben.
Schuhe sollten nachmittags gekauft werden, da die Füße im Laufe des Tages anschwellen und druckempfindlicher sind.
Matratzenauswahl Der Körper sollte nicht übermäßig einsinken, weil das zu unphysiologischen Schlafpositionen führt. Ebenso sollte verhindert werden, dass der Rücken an einigen Stellen gar nicht auf der Unterlage liegt. Ein Lagerungskissen kann den Rücken an den richtigen Stellen unterstützen.
Selbsthilfe bei Lumbago
Im Falle eines „Hexenschusses“ muss zuerst die Symptomatik eingeschätzt werden:
-
Halten die starken Schmerzen lang an?
-
Habe ich Sensibilitätsstörungen?
-
Habe ich Lähmungserscheinungen?
-
Liegen Störungen der Blasen- und/oder Mastdarmfunktion vor?
Muss der Betroffene eine der 4 Fragen bejahen, sollte er einen Arzt aufsuchen. Ist dies nicht der Fall, wird wie folgt weiter vorgegangen:
-
schonendes langsames Aufstehen (falls der Betroffene am Boden liegt)
-
entspannende Atemtechnik
-
Bettruhe, ggf. als Stufenbettlagerung zur Schmerzlinderung
-
Bedarfsmedikamente nach ärztlicher Anordnung
-
schmerzlindernde Öle lokal auftragen
-
feuchtwarme, mit Arnikalösung getränkte Wickel
-
heißes Wannenbad
-
Kälteanwendungen (feuchtes Handtuch, Cool-Pack) oder Wärmeanwendungen (z. B. Wärmflasche, Heizdecke, durchblutungsfördernde Salben, Leibwickel). Achtung: Gefahr der Verbrennung bei Sensibilitätsstörungen!
39.4 Pflege von Patienten mit Frakturen
39.4.1 Medizinischer Überblick
39.4.1.1 Definition
Eine Fraktur (lat.) ist ein Knochenbruch. Die Bruchstücke (Fragmente) sind durch den Bruchspalt (Frakturlinie) voneinander getrennt.
39.4.1.2 Symptome
Sichere Zeichen Eine Fraktur ist gekennzeichnet durch
-
Fehlstellungen,
-
abnorme Beweglichkeit,
-
hör- und tastbares Knochenreiben (Krepitation) und
-
evtl. sichtbare Knochenteile bei einer offenen Fraktur.
Unsichere Zeichen Häufig werden unsichere Frakturzeichen beobachtet, die aber auch bei anderen Verletzungen vorkommen:
-
Bewegungseinschränkung
-
Schmerzen
-
Schwellung und Hämatome
39.4.1.3 Einteilung der Frakturen
Bricht der Knochen nicht komplett durch, wird von einer unvollständigen Fraktur gesprochen. Dazu gehören:
-
Fissur → es bildet sich ein Riss im Knochen
-
Infraktion → es bildet sich ein Spalt im Knochen
-
kindliche Grünholzfraktur → die Kortikalis bricht nur an einer Seite, die umhüllende elastische Knochenhaut bleibt erhalten.
Die Frakturen lassen sich auf verschiedene Arten einteilen:
-
nach Entstehung der Fraktur
-
nach Hautbeschaffenheit
-
nach Anzahl der Fragmente
-
nach Verlauf der Frakturlinie
Einteilung nach Entstehung
Frakturen entstehen, wenn die Gewalteinwirkung die Belastungsgrenze des Knochens überschreitet. Sie können je nach Art der Gewalteinwirkung als Biegungs-, Dreh-, Schub- oder Scherungsbrüche, Abriss- oder Kompressionsfrakturen bezeichnet werden.
Direkte und indirekte Gewalt Durch eine einmalige direkte Gewalteinwirkung auf den gesunden Knochen, z. B. durch einen Schlag oder Stoß, bricht der Knochen. Um eine indirekte Gewalteinwirkung handelt es sich, wenn die Bruchhöhe nicht dem Ort der Gewalteinwirkung entspricht. Indirekt auftretende Gewalt sind z. B. Stauchung, Scherung, Abriss, Torsion oder Biegung eines Knochens.
Spontanfraktur Eine Fraktur ohne ein vorhergehendes Ereignis wird als Spontanfraktur bezeichnet. Dabei wird unterschieden zwischen Ermüdungsfraktur und pathologischer Fraktur. Ermüdungsfrakturen entstehen nach einer wiederholten längeren Anstrengung bei Dauerbeanspruchung bestimmter Knochenstellen. Pathologische Frakturen entstehen als Folge krankhaft veränderter Knochenstrukturen, z. B. bei ▶ Osteoporose oder ▶ Knochentumoren.
Einteilung nach Hautbeschaffenheit
Ist die Haut über der Bruchstelle unverletzt, wird von einer geschlossenen Fraktur gesprochen. Wurde sie durch das Trauma von außen oder durch den Knochen von innen verletzt, handelt es sich um eine offene Fraktur.
Offene Fraktur Je nach Umfang der Weichteilschäden und Ausmaß der Kontamination werden offene Frakturen in 4 Schweregrade eingeteilt ( ▶ Abb. 39.16). Bei einer offenen Fraktur besteht immer die Gefahr einer Infektion von Knochen und Weichteilen mit den damit verbundenen Komplikationen, sie muss daher frühzeitig operativ versorgt werden.
Einteilung der offenen Frakturen in 4 Schweregrade.
Abb. 39.16
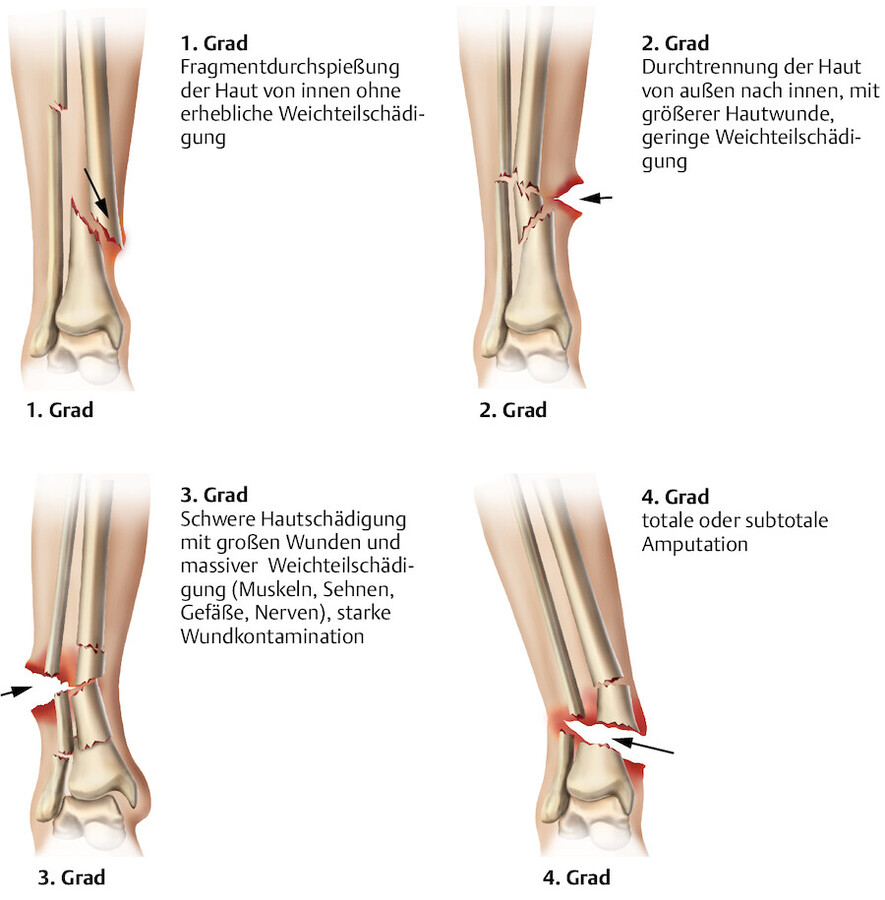
Einteilung nach Anzahl der Fragmente
Unterschieden werden
-
einfache Brüche mit 2 Fragmenten,
-
Mehrfragmentfrakturen mit 3 – 6 Bruchstücken,
-
Trümmerfrakturen mit mehr als 6 Fragmenten und
-
Stückfrakturen, wobei der Knochen an 2 Stellen gebrochen ist (in der Mitte befindet sich ein größeres intaktes Frakturstück).
Einteilung nach Verlauf der Frakturlinie
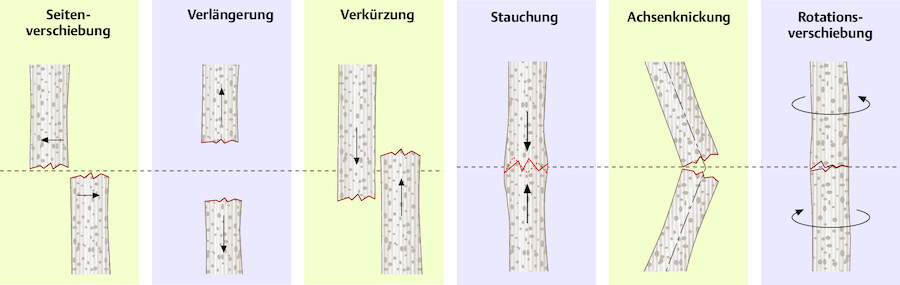
Nach dem Frakturverlauf erfolgt die Einteilung in Quer-, Längs-, Schräg-, Spiral-, T- oder Y-Fraktur. Besteht eine Verschiebung der Bruchstücke gegeneinander, handelt es sich um eine dislozierte Fraktur. Typische Verschiebungen entstehen durch die Art der Gewalteinwirkung und den Muskelzug. Die 6 Dislokationsformen sind in ▶ Abb. 39.17 dargestellt.
Dislokationsformen.
Abb. 39.17 Je nach Art der Gewalteinwirkung und Muskelzug entstehen bei Frakturen typische Dislokationsformen.
39.4.1.4 Diagnostik
-
Röntgenaufnahmen (in mindestens in 2 Ebenen), oft als Verlaufskontrolle.
-
Computertomografie, mittlerweile sind komplexe dreidimensionale Darstellungen möglich
-
Kernspintomografie
-
Ultraschall (z.B. Rippenfrakturen)
Zusätzlich wird in der klinischen Untersuchung immer die Durchblutung, Motorik und Sensibilität im Frakturbereich geprüft, um Begleitverletzungen auszuschließen.
39.4.1.5 Begleitverletzungen
Das umliegende Gewebe kann durch einen Knochenbruch mit verletzt sein. Besonders anfällig sind Nerven und Gefäße. Verletzungen eines Nervs führen im Versorgungsgebiet zu Funktions- und Sensibilitätsstörungen. Betroffen sind häufig
-
N. radialis bei einer Oberarmfraktur oder
-
N. peronaeus am Wadenbeinköpfchen.
Meist entsteht ein Hämatom an der Bruchstelle. Bei Frakturen großer Knochen (z. B. Oberschenkelknochen oder Becken) und ausgedehnter Weichteilbeteiligung ist mit einem hohen Blutverlust zu rechnen. Ein Blutverlust über 1 l führt zum hypovolämischen Schock.
39.4.1.6 Therapie
Nach der Erstversorgung am Unfallort gelten in der Behandlung von Frakturen die 3 R-Grundsätze:
-
Reposition (Einrichten der Fraktur)
-
konservative oder operative Retention (Ruhigstellen)
-
Rehabilitation (Wiederherstellen)
Reposition
Die verschobenen Fragmente werden durch manuellen Zug und Gegenzug von außen eingerichtet. Das Einrichten sollte möglichst sofort und anatomisch korrekt erfolgen. Der Patient wird dafür analgesiert und relaxiert.
Besonders dringlich ist die Reposition bei einer Fraktur mit Weichteil-, Gefäß- oder Nervenbeteiligung. Gelingt eine geschlossene Reposition nicht, muss eine offene Reposition im OP unter Freilegung des Knochens erfolgen.
Konservative Retention
Die eingerichteten Fragmente werden so lange ruhiggestellt, bis der Knochen geheilt ist. Konservative Methoden dazu sind:
-
fixierende Verbände aus Gips oder Kunststoff
-
Schienen aus Gips oder Kunststoff
-
elastische, ▶ ruhigstellende Verbände
-
Extensionen.
Indikationen Konservativ werden folgende Frakturen behandelt:
-
die meisten kindlichen Frakturen
-
alle Frakturen, die auch ohne Operation folgenlos ausheilen (z. B. Rippen- und Beckenbrüche)
-
unkomplizierte, nicht dislozierte Frakturen ohne Gelenkbeteiligung (z. B. Handfrakturen)
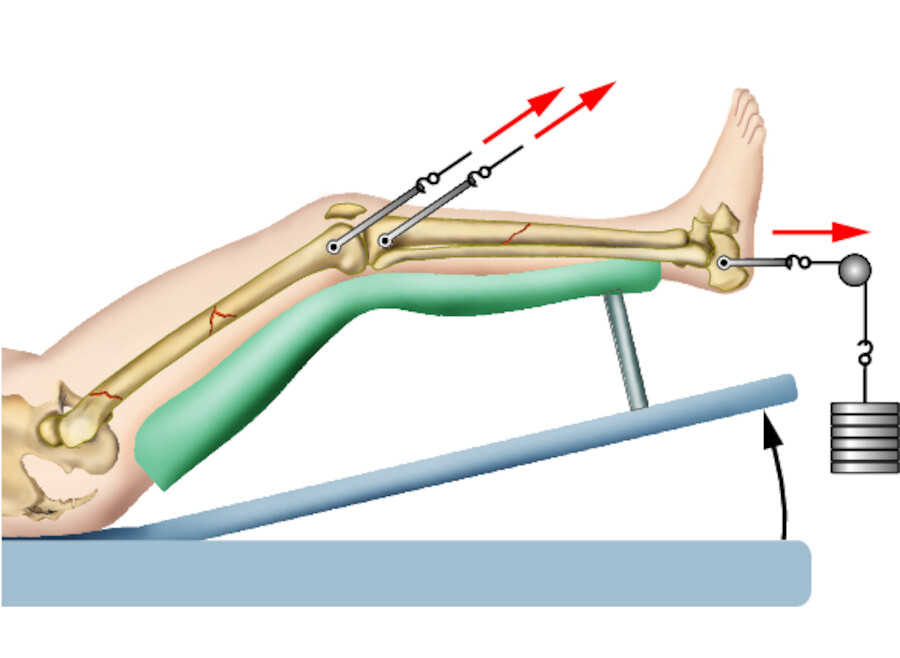
Extension Die „Streckbehandlung“ wird bei Frakturen angewandt, bei denen ein hohes Risiko der Fragmentverschiebung besteht. Durch einen dauerhaften Zug werden die langsame Reposition der Fragmente und die Ruhigstellung in anatomischer Lage erreicht. In Lokalanästhesie wird durch den frakturfernen Knochen ein Metalldraht gebohrt. Daran wird ein Extensionsbügel angebracht. Über einen Seilzug ziehen Gewichte die Fragmente auseinander ( ▶ Abb. 39.18). Da die Extensionsbehandlung mit langer Bettlägerigkeit und Immobilität verbunden ist, wird sie heute nur noch selten und wenn dann über einen kurzen Zeitraum (24–48 Stunden) angewandt, z.B. zur Überbrückung bis zur OP bei Frakturen der unteren Extremitäten, des Beckens und der Halswirbelsäule.
Extensionsbehandlung.
Abb. 39.18 Als Lokalisationsort für Extensionen dienen spongiöse Knochenbereiche mit geringer Weichteildeckung.
Die Vor- und Nachteile einer konservativen bzw. operativen Frakturbehandlung sind in ▶ Tab. 39.3 dargestellt.
|
Gipsbehandlung |
Extension |
Osteosynthese |
|
Reposition |
||
|
nicht exakt möglich |
nicht exakt möglich |
anatomisch korrekte Reposition |
|
Ruhigstellung |
||
|
absolute Ruhigstellung nicht möglich |
absolute Ruhigstellung nicht möglich |
absolute Ruhigstellung |
|
Mobilisation |
||
|
mithilfe von Gehstützen früh möglich |
keine Mobilisation möglich, Patient ist lange bettlägerig |
Frühmobilisation an Gehstützen oder Vollbelastung früh möglich |
|
Infektionsrisiko |
||
|
keins, da Fraktur geschlossen bleibt |
gering, nur im Bereich der Nageldurchtrittsstelle |
Infektion des gesamten Knochens möglich |
|
Weichteilkontrolle |
||
|
nicht möglich |
gut möglich |
gut möglich (besonders wichtig bei offenen Frakturen) |
|
Thromboserisiko |
||
|
bei Gips an den unteren Extremitäten erheblich |
aufgrund der Bettlägerigkeit erheblich |
bei Frühmobilisation gering |
|
spezielle Vorteile |
||
|
meist ambulante Therapie möglich |
keine Sekundärverletzung durch Muskelzug |
|
|
spezielle Nachteile |
||
|
|
|
Operative Retention
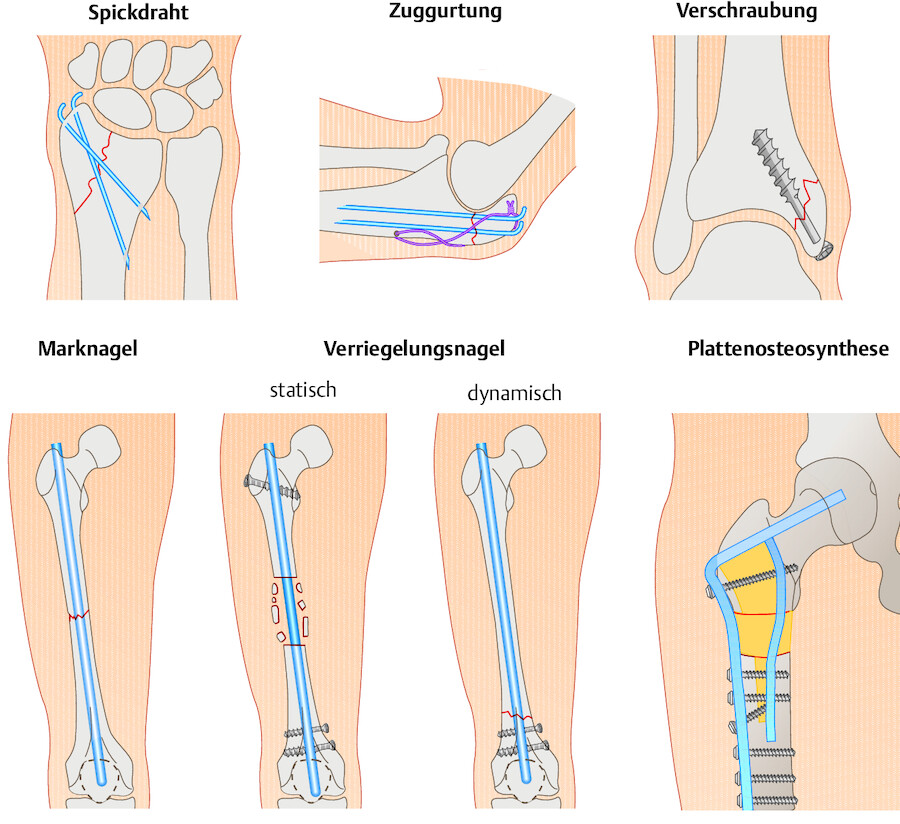
Zur operativen Frakturbehandlung stehen verschiedene Osteosyntheseverfahren zur Verfügung ( ▶ Abb. 39.19).
Verschiedene Osteosyntheseverfahren.
Abb. 39.19
Indikationen Operativ werden Frakturen versorgt, die sonst nicht knöchern oder langsamer und mit schlechterem funktionellem Ergebnis ausheilen würden, z. B.:
-
offene Frakturen
-
Frakturen, bei denen ein Gelenk beteiligt ist
-
Frakturen, die sich nicht geschlossen reponieren lassen
-
Frakturen mit Nerven- und Gefäßverletzungen
Definition
Osteosynthesen bezeichnen ein operatives Verfahren zur Stabilisierung der Fraktur mit verschiedenen Implantaten für die Dauer der Bruchbehandlung.
Die feste Verbindung der Bruchteile für die gesamte Dauer des Heilungsprozesses ermöglicht eine frühfunktionelle und schmerzfreie Übungsbehandlung.
Mit Schrauben, Drähten, Nägeln oder Platten wird die Fraktur versorgt. Je nach Stabilität wird unterschieden zwischen lagerungs-, übungs- und belastungsstabilen Fixierungssystemen.
Lagerungsstabile Osteosynthesen
Sie dürfen nicht bewegt oder belastet werden (z. B. Spickdrahtosteosynthesen bei Frakturen an Hand und Fuß). Lagerungsstabile Osteosynthesen benötigen deshalb immer eine zusätzliche Ruhigstellung in einer Gipsschiene.
Übungsstabile Osteosynthesen
Die meisten Osteosynthesen sind übungsstabil, d. h., die operierte Extremität darf frei bewegt, aber nicht belastet werden. Hierzu zählen die Zuggurtung bei Frakturen an Ellenbogen oder Kniescheibe, Schrauben- oder Plattenosteosynthesen ( ▶ Abb. 39.19).
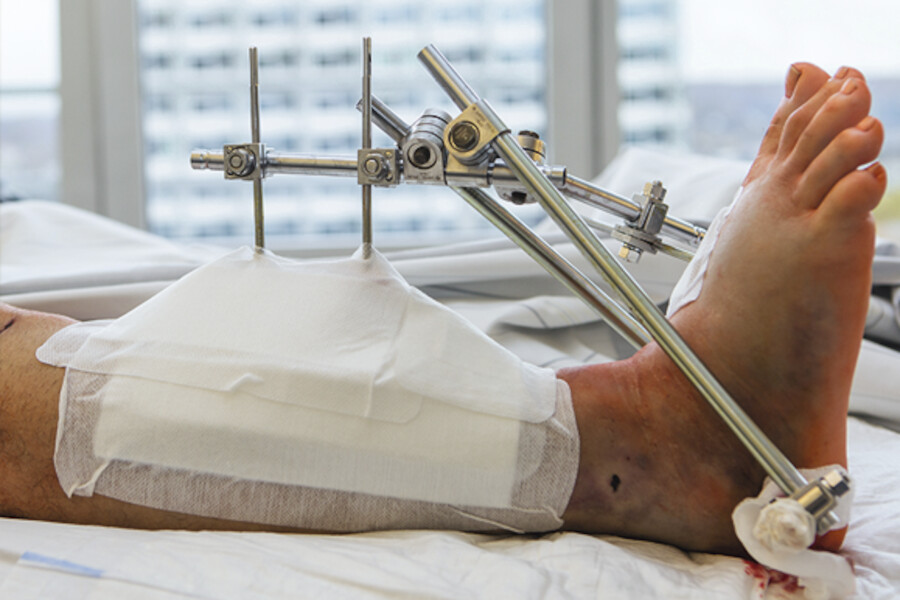
Fixateur externe Eine besondere Form der übungsstabilen osteosynthetischen Behandlung bildet der Fixateur externe ( ▶ Abb. 39.20). Er nimmt die nötige Stabilisierung der Fragmente von außen vor. Der Fixateur externe stabilisiert die Bruchfragmente durch Nägel oder Schrauben, die frakturfern eingebracht werden. Sie sind über ein Gestänge (Rahmenfixation) miteinander verbunden, um die Fraktur in der gewünschten Position zu halten. Angewandt wird der Fixateur externe hauptsächlich bei offenen oder infizierten Frakturen mit Weichteildefekten, instabilen Beckenfrakturen sowie als vorübergehende Fixation bei Polytraumen. Die Vorteile des Fixateur externe sind die relativ kurze Operationsdauer und die geringe intraoperative Weichteilverletzung.
Fixateur externe.
Abb. 39.20 Er wird zur Ruhigstellung einer Extremität eingesetzt.
(Foto: K. Oborny, Thieme)
Belastungsstabile Osteosynthesen
Zu den belastungsstabilen Osteosynthesen gehören der Marknagel (bei Frakturen der unteren Extremität) oder die Verbundosteosynthese (bei Knochendefekten durch pathologische Frakturen). Der Patient darf den betroffenen Körperteil gleich nach der Operation voll- bzw. teilbelasten.
Endoprothesen Die Implantation eines künstlichen Gelenks aus Metall wird als Endoprothese bezeichnet. Sie wird v. a. bei Schenkelhalsfrakturen, aber auch bei Gelenkdegenerationen an Hüfte oder Knie eingesetzt. Endoprothesen sind bis auf wenige Ausnahmen belastungsstabil.
Spongiosaplastiken Knochentransplantationen in Form von Spongiosaplastiken dienen zur Defektauffüllung bei Trümmerfrakturen. Spongiosa wird aus dem Beckenkamm entnommen. Die Stabilität wird durch eine zusätzliche Osteosynthese durch einen Fixateur externe oder eine Platte erreicht.
Die Entscheidung über das Verfahren hängt von der Art der Fraktur und den Begleiterkrankungen ab. Das Material wird i. d. R. (außer bei Endoprothesen) nach Abschluss der Frakturheilung (nach 3 Wochen bis zu 2 Jahren) in einer zweiten Operation entfernt.
Rehabilitation
Dem Patienten werden geeignete und auf ihn abgestimmte krankengymnastische Übungen verordnet, die
-
den nicht betroffenen Körperteil mit einbeziehen,
-
Funktionsverluste während der Ruhigstellung vermeiden,
-
helfen, die volle Beweglichkeit und Funktion nach abgeschlossener Frakturheilung wiederzuerlangen.
39.4.1.7 Frakturheilung
Für die ungestörte Frakturheilung sind folgende Bedingungen zu erfüllen:
-
inniger Kontakt der Fragmente
-
ununterbrochene Ruhigstellung
-
ausreichende Durchblutung
-
Infektionsfreiheit
Unterschieden werden primäre und sekundäre Frakturheilung.
Primäre Frakturheilung Unter idealen Bedingungen, die zumeist bei osteosynthetischer Versorgung gegeben sind, wird der Bruchspalt durch direkt einsprossende Zellen des Knochens (Osteoblasten) überbrückt und verzahnt. Es entsteht voll belastbares Knochengewebe ohne Kallusbildung.
Sekundäre Frakturheilung Ist eine ununterbrochene Ruhigstellung nicht gewährleistet, wie es bei der konservativen Behandlung häufig der Fall ist, verläuft die Heilung über verschiedene Umbauprozesse der Zellen in Knochengewebe. Die anfangs noch weiche Kallusbildung lagert Kalk ein und wird hart und belastbar. Der Verlauf der Frakturheilung lässt sich gut im Röntgenbild beurteilen. Sind nicht alle der Voraussetzungen für die Heilung des Knochens gegeben, kann es zu vielfältigen Komplikationen kommen ( ▶ Tab. 39.4 ).
|
Komplikation |
Ursachen |
|
Osteomyelitis |
|
|
Pseudarthrose |
|
|
ischämische Kontrakturen:
|
|
|
Frakturkrankheit (Sudeck-Syndrom) |
|
|
Fettembolie |
|
39.4.2 Pflege- und Behandlungsplan
Für den Patienten entstehen Probleme bei einer Fraktur in erster Linie durch Schmerzen und Bewegungseinschränkung. Ein Krankenhausaufenthalt kommt für einen Verunglückten immer unvorbereitet. Lässt der Zustand des Patienten es zu, wird er im Rahmen eines Aufnahmegesprächs über alle anstehenden Maßnahmen und den voraussichtlichen Ablauf informiert.
Die Aufgaben der Pflege variieren, je nachdem ob die Fraktur operativ oder konservativ versorgt wird.
39.4.2.1 Pflege bei osteosynthetischer Frakturbehandlung
Fallbeispiel
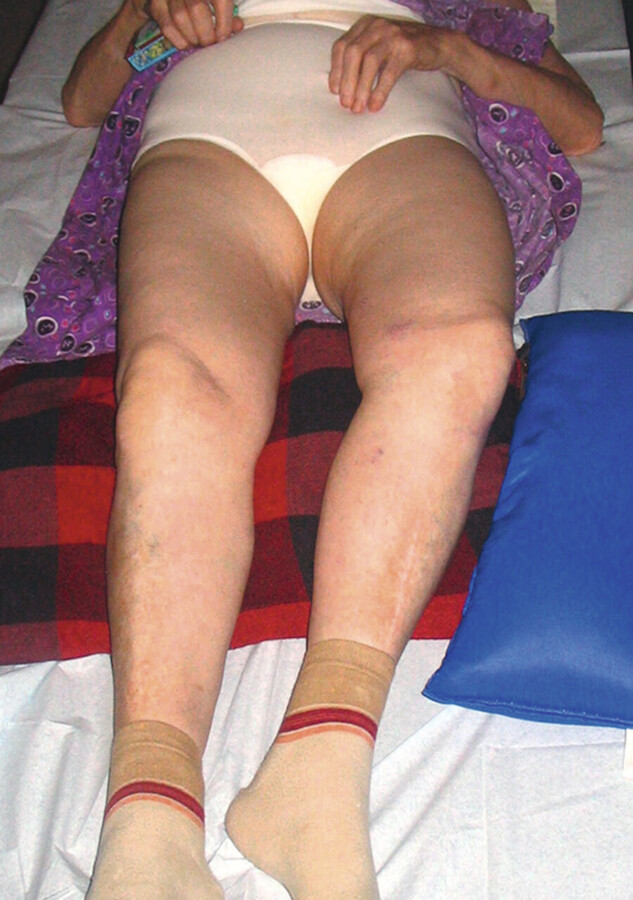
Frau Keller, 80 Jahre alt, lebt allein, führt ihren Haushalt selbst und ist stolz auf ihre Selbstständigkeit. Nur für schwere Einkäufe bittet sie ihren Enkel um Hilfe. Heute ist sie mit dem Bus unterwegs, um einen Besuch zu machen. Beim Einsteigen rutscht sie auf regennasser Straße aus und stürzt auf den Gehweg. Die anderen Fahrgäste versuchen ihr aufzuhelfen, aber Frau Keller hat zu große Schmerzen in der linken Hüfte. Sie kann das Bein nicht mehr bewegen, es liegt stark nach außen verdreht. Der vom Busfahrer gerufene Rettungswagen bringt sie ins Krankenhaus. Der Arzt stellt eine mediale Oberschenkelhalsfraktur ( ▶ Abb. 39.21) fest und empfiehlt zur Behandlung eine Totalendoprothese der Hüfte.
Typische Beinfehlstellung bei einer Schenkelhalsfraktur.
Abb. 39.21 Der Winkel zwischen Hals und Schaft des Oberschenkelknochens beträgt normalerweise 125 – 130°. Das betroffene Bein ist verkürzt und nach außen gedreht.
Operationsvorbereitung
Grundsätzlich gelten auch bei einer akut auftretenden Operationsindikation die ▶ allgemeinen Operationsvorbereitungen. Wenn die Operation sofort durchgeführt werden muss, kann keine Nahrungskarenz und Darmentleerung mehr stattfinden. In jedem Fall sollte dem Patienten die Möglichkeit gegeben werden, seine Blase zu entleeren. Meist wird routinemäßig ein Blasenkatheter gelegt.
Wenn mit einem großen Blutverlust gerechnet werden muss, sollten ausreichend Blutkonserven bereitgestellt werden. Bei geplanten Operationen (z. B. bei einer Hüft-Endoprothese) kann der Patient unter bestimmten Bedingungen präoperativ Eigenblut spenden, was ihm intra- oder postoperativ wieder verabreicht werden kann.
Postoperative Versorgung
Die allgemeinen pflegerischen Aufgaben in der postoperativen Phase können im Kapitel ▶ „Postoperative Phase“ nachgelesen werden. Zu den besonderen pflegerischen Schwerpunkten gehören
-
Lagerung/Positionierung,
-
Mobilisation,
-
Schmerzbehandlung,
-
Wund- und Drainagenversorgung und
-
Versorgung nach den ATL.
Lagerung/Positionierung
Ziel ist eine bequeme, schmerzreduzierende und funktionelle Positionierung der operierten Extremität. Um postoperative Schwellungen durch einen venösen Rückstau zu vermeiden, wird das betroffene Körperteil leicht hochgelagert.
Es gelten die Anordnungen des Operateurs über Art und Dauer der Schienenlagerung. In der Regel wird die betroffene Extremität für 4 – 7 Tage auf einer Lagerungsschiene oder einem Kissen ruhiggestellt. Die Lage der Schiene und der Sitz der Extremität in der Schiene (und ggf. die Polsterung) sind regelmäßig zu kontrollieren. Regelmäßig werden Durchblutung, Sensibilität und Beweglichkeit der Finger bzw. Zehen der betroffenen Extremität durch die Pflegeperson kontrolliert. Neben der Spitzfußprophylaxe können weitere Prophylaxen durchgeführt werden.
Praxistipp
Leiten Sie den Patienten nach Einschätzung seiner Fähigkeiten und seines Kooperationswillens an, die korrekte Lage auf der Schiene selbst zu kontrollieren.
Positionierung der oberen Extremitäten Zur Ruhigstellung (z. B. nach einer Humerusfraktur) wird der Arm nach vorn auf ein oder mehrere Kissen gelagert. Der Oberarm wird um ca. 60° von der Mittellinie weggeführt (abduziert), das Ellenbogengelenk in ca. 90° Mittelstellung gebeugt.
Positionierung der unteren Extremitäten Vor allem bei Schenkelhalsfrakturen ist auf die Luxationsprophylaxe zu achten. Das Bein wird flach in einer Schiene oder auf ein Kissen positioniert, dabei liegt der Fuß gerade in der Schiene. Zur Spitzfußprophylaxe sollte der Fuß am Ende der Schiene anliegen. Um einen Dekubitus zu vermeiden, ist auf Weich- oder Hohllagerung der Ferse zu achten. Zur Unterstützung und um eine Überstreckung des Kniegelenks zu vermeiden, wird ein kleines, flaches Kissen in die Kniekehle gelegt. Beim Aufsetzen des Oberkörpers sollte die Hüfte nur leicht gebeugt werden. Zwischen den Beinen befindet sich ein weiteres oder ein spezielles Keilkissen, um unerwünschte Bewegungen eines Körperteils zur Mittellinie (Adduktion) zu vermeiden. Eine Abduktion > 20 – 30° über die Mittellinie sollte verhindert werden.
Praxistipp
Stellen Sie Nachttisch, Getränke, Telefon und Klingelanlage in erreichbare Nähe, damit sich der Patient beim Drehen und Beugen des Oberkörpers nicht in eine luxationsbegünstigende Lage begibt.
Mobilisation
Da die meisten Osteosynthesen mindestens eine Übungsstabilität erlauben, wird eine frühzeitige Mobilisation angestrebt. Die Entscheidung über die Übungs- oder Belastungsstabilität findet immer erst nach der postoperativen Röntgenkontrolle und durch den Arzt statt. Vorher darf keine Mobilisation oder Bewegung vorgenommen werden.
Mobilisation bei Frakturen der oberen Extremitäten Die Mobilisation kann i. d. R. noch am OP-Tag stattfinden. Je nach Kreislaufsituation ist das Stehen vor dem Bett oder ein kurzes Aufstehen (z. B. zur Toilette) mit Unterstützung und in Begleitung einer Pflegeperson möglich.
Mobilisation bei Frakturen der unteren Extremitäten Die erste Mobilisation kann i. d. R. am ersten postoperativen Tag stattfinden. Sie orientiert sich aber am Zustand des Patienten und geschieht optimalerweise in enger Zusammenarbeit mit den Physiotherapeuten. Wie das Positionieren erfordert auch die Mobilisation bei Frakturen an den Beinen, besonders bei Endoprothesen, einige Aufmerksamkeit. Bei bestimmten Bewegungen besteht Luxationsgefahr, deshalb gelten folgende Regeln:
-
Drehen und Aufstehen über die operierte Seite
-
Überkreuzen der Beine beim Aufstehen und Sitzen vermeiden
-
optimale Sitzposition in 90°-Hüftbeugung durch Sitzerhöhung
-
tiefe Sitzposition vermeiden
In der ersten postoperativen Zeit benötigt der Patient Hilfe bei der Lageveränderung im Bett. Die Pflegeperson hält und stabilisiert das operierte Bein. Der Patient wird dazu angehalten, die gesunden Extremitäten regelmäßig zu bewegen, evtl. unter Anleitung der Physiotherapeuten. Diese stellen auch geeignete Hilfsmittel wie Unterarmgehstützen, Rollstuhl, Gehhilfe oder Rollator zur Verfügung und üben das Gehen. Nach ärztlicher Anordnung und Einweisung durch den Physiotherapeuten ist die Motorschiene zur passiven Bewegung des Kniegelenks eine geeignete Mobilisationsform. Bevor sie in ein anderes Bett gelegt wird, ist sie z. B. mit 70 % Alkohol zur Desinfektion abzuwischen.
Die Übungen erfolgen i. d. R. 2-mal täglich. Der Beugungsgrad wird der Schmerzsituation des Patienten angepasst und täglich gesteigert.
Schmerzbehandlung
In den ersten postoperativen Tagen nach einer Osteosynthese leidet der Patient unter starken Schmerzen. Je nach Anordnung des Arztes erhält er ▶ Schmerzmittel oral, als Injektion oder Infusion bzw. kontinuierlich über eine PCA-Schmerzpumpe.
Definition
PCA: engl. patient-controlled analgesia, d. h. patientenkontrollierte Analgesie: Der Patient fordert Schmerzmittel in kleinen Dosen entsprechend seinem Bedarf. Die Schmerzpumpe ist vom Arzt programmiert, sodass keine Überdosierung möglich ist.
Besonders wichtig ist, dass der Patient zu Beginn der Mobilisationsmaßnahmen schmerzfrei ist, um aktiv an den Bewegungsübungen teilnehmen zu können Eine rechtzeitige und ausreichende Schmerzmittelgabe verhindert unnötige Schmerzsituationen. Der Patient wird darüber informiert, dass er keinesfalls Schmerzen „aushalten“ muss.
Wund- und Drainagenversorgung
Um Blutungen frühzeitig zu erkennen, werden Wunde und Drainagen in engen zeitlichen Abständen von der Pflegeperson überwacht. Sie achtet auch darauf, dass der Verband korrekt sitzt, nicht einschnürt oder Falten wirft. Jeder Verbandwechsel erfolgt unter aseptischen Bedingungen ebenfalls nach Anordnung des Arztes.
Je nach OP-Art liegen 1 – 3 Wunddrainagen. Von der Pflegeperson werden Fördermenge und Sog kontrolliert, abhängig davon werden die Drainagen am 2.– 3. postoperativen Tag nach Anordnung des Arztes entfernt. Alle Beobachtungen werden sorgfältig dokumentiert.
Versorgung nach den ATL
Die unterstützende Pflege ist abhängig vom Ausmaß der Beeinträchtigung in der Bewegung, von Schmerzen, weiteren Verletzungen oder Begleiterkrankungen und den Ressourcen des Patienten. ▶ Die ATL werden ausführlich in Buchteil 2 beschrieben.
Patienten mit Frakturen der oberen Extremitäten benötigen Hilfestellungen bei der Zubereitung der Mahlzeiten, z. B. Brötchen aufschneiden, Flaschen und Portionsverpackungen öffnen.
Praxistipp
Beim Anziehen sollte erst der operierte Körperteil angezogen werden, beim Ausziehen erst das gesunde Körperteil.
Patienten mit Frakturen der unteren Extremität müssen u. U. ein Steckbecken oder eine Urinflasche benutzen. Bei Patienten mit Hüftendoprothesen oder Femurschaftfrakturen muss das Steckbecken von der nichtoperierten Seite aus unter das Becken platziert werden. Eine Hilfe zum schmerzärmeren Unterstecken oder Entfernen des Steckbeckens kann eine Erhöhung des Trochanter major auf der gegenüberliegenden Seite sein.
Entlassungsvorbereitung
Vor der Entlassung wird der Patient mit den noch erforderlichen Hilfsmitteln wie Unterarmgehstützen, Toilettensitzerhöhung ( ▶ Abb. 39.22) oder Rollstuhl und Toilettenstuhl versorgt. Die häusliche Situation muss in Gesprächen mit dem Patienten und seinen Angehörigen erfasst werden. Bestehen längerfristige Einschränkungen in der selbstständigen Versorgung, können vom Sozialdienst entsprechende Veränderungen in der Wohnung eingeleitet und ein ambulanter Pflegedienst engagiert werden.
Toilettensitzerhöhung.
Abb. 39.22 Die Sitzerhöhung erleichtert dem Patienten das Aufstehen und Hinsetzen auf die Toilette und verhindert eine zu starke Beugung des Hüftgelenks über 90°.
(Foto: K. Gampper, Thieme)

Fallbeispiel
Frau Keller wurde schon am Tag nach der Operation mobilisiert. Die Schmerzen waren mithilfe der Medikamente gut auszuhalten. Jeden Tag übte sie mit der Physiotherapeutin das Gehen an Unterarmgehstützen und nach wenigen Tagen konnte sie in Begleitung auf dem Krankenhausflur spazieren gehen. Die Sozialarbeiterin kümmerte sich um eine ambulante Rehabilitationsmaßnahme. Versorgt mit allen Hilfsmitteln und der Unterstützung ihrer Familie, kann sich Frau Keller weiterhin gut selbstständig versorgen.
Bei einer endoprothetischen Versorgung schließt sich häufig eine Anschlussheilbehandlung (AHB) an. Das wesentliche Ziel ist die Verbesserung der Beweglichkeit, um die weitgehende Selbstständigkeit des Patienten zu erreichen und ihn je nach Alter evtl. für das Arbeitsleben zu rehabilitieren.
Im Krankenhaus begonnene Maßnahmen wie Narbenpflege, Krankengymnastik oder Lymphdrainagen sollten weitergeführt werden, um den Erfolg des Osteosyntheseverfahrens sicherzustellen.
39.4.2.2 Pflege bei Fixateur externe
Vor allem ein Fixateur externe an der unteren Extremität schränkt die Beweglichkeit stark ein. Deshalb sind Thrombose-, Dekubitus-, Pneumonie- und Obstipationsprophylaxe wichtige pflegerische Aufgaben (s. dort). Weitere pflegerische Aufgaben sind die postoperative Überwachung und die Entlassungsvorbereitung.
Postoperative Überwachung
Zum Ausschluss von Nervenverletzungen werden regelmäßig Durchblutungs-, Sensibilitäts- und Beweglichkeitskontrollen der fixierten Extremität durchgeführt.
Veränderungen der Hautfarbe (livide bis blass) weisen auf eine schwellungsbedingte Gefäßkompression oder -verletzung hin. Der behandelnde Arzt wird informiert, wenn die Ein- bzw. Austrittsstelle der Nägel blutet. Der Patient wird darauf hingewiesen, dass er jede Veränderung im Wundbereich (z. B. Taubheitsgefühl, Kribbeln oder Schmerzen) mitteilen soll. Den korrekten Sitz und die Stabilität des Fixateurs kontrolliert der Arzt.
Lagerung
Die betroffene Extremität wird in einer Schaumstoffschiene hochgelagert, um den Ödemabfluss zu unterstützen. Das Wadenbeinköpfchen muss besonders gut gepolstert werden, da dort die Gefahr der lagerungsbedingten Schädigung des Nervus peronaeus besteht.
Gelkühlkissen können zur Schmerzlinderung und als abschwellende Maßnahme eingesetzt werden. Die Kühldauer sollte 15 Min. nicht überschreiten, um Kälteschäden zu vermeiden.
Merke
Legen Sie Kühlelemente nie ohne Schutzhülle auf die Haut, sonst kann es zu Kälteschäden kommen!
Wundversorgung
Für die Wundversorgung gelten die ▶ aseptischen Regeln des Verbandwechsels. Die tägliche Inspektion der Eintrittsstellen der Schrauben und Nägel lassen eine der häufigsten Komplikationen rechtzeitig erkennen. Die sog. Pintrack-Infektion (Pin = Stift, Track = Weg) kann zur Lockerung und damit zur Instabilität führen. Bei fortschreitender Infektion droht die Bohrlochosteomyelitis.
Offene Wundbehandlung Bei der offenen (verbandlosen) Versorgung werden Eintrittsstellen und Wunde mit geeignetem Wundantiseptikum (z. B. Lavanid) desinfiziert. Die weiteren äußeren Metallteile können mit einem alkoholischen Hautantiseptikum abgesprüht werden. Bei sauberen und trockenen Wundverhältnissen ist es möglich, die Extremität mit lauwarmer, steriler Ringerlösung zu spülen und den Wundbereich mit sterilen Kompressen zu trocknen.
Geschlossene Wundbehandlung Die Eintrittsstellen werden nach der Desinfektion mit Schlitzkompressen abgedeckt und mit einer Binde fixiert.
Entlassungsvorbereitung
Zum Schutz vor Verletzungen können spezielle Plastikkappen auf die Schraubenenden gesteckt werden. Dem Patienten kann zusätzlich gezeigt werden, wie er bei alltäglichen Verrichtungen (z. B. beim An- und Auskleiden, bei der Körperpflege und im Schlaf) Verletzungen vermeiden kann. Er wird darüber informiert, dass sich die Metallteile bei starker Sonneneinstrahlung erwärmen. Bei Beschwerden sollte der Patient umgehend den Arzt aufsuchen.
Nach dem Entfernen der Pins werden die Wundlöcher steril verbunden. Später reicht ein Pflaster aus.
39.4.2.3 Pflege bei Extensionsbehandlung
Die Extensionsbehandlung ist mit langer Bettlägerigkeit und Immobilität verbunden. Der Umfang der pflegerischen Unterstützung ist individuell festzulegen und sollte dem Patienten ein gewisses Maß an Selbstständigkeit ermöglichen.
Pflegerische Hilfe benötigt der Patient bei der Körperpflege und beim ▶ An- und Auskleiden, bei der ▶ Nahrungsaufnahme und bei den ▶ Ausscheidungen.
Fallbeispiel
Erfahrungsbericht von Herrn Giesicke, 54 Jahre: Vor 2 Tagen habe ich den Fixateur bekommen. Ich brauche total viel Hilfe, weil ich nicht aufstehen kann: beim Waschen, sogar beim Toilettengang. Ich bin völlig unbeweglich in diesem Gestell. Einmal ist jemand aus Versehen an das Gestänge gekommen und die Gewichte pendelten hin und her – oje, war das schmerzhaft! Alle geben sich große Mühe, es mir bequem zu machen: Die Pflegenden hier auf der Station, meine Familie und meine Freunde kommen mich regelmäßig besuchen. Vormittags kommt die Physiotherapeutin. Aber die Tage sind sehr lang, es gibt wenig Abwechslung. Ich kann doch nicht immer nur lesen! Mir fehlt meine Arbeit im Garten. In der Nacht kann ich nicht gut schlafen, weil ich eigentlich auf dem Bauch schlafe.
Lagerung
Für den Aufbau einer Extension werden Betten benötigt, bei denen das Fußende hochgestellt werden kann, damit das Körpergewicht des Patienten als Gegenzug wirkt. Das frakturierte Bein wird auf eine Lagerungsschiene positioniert. Weitere Kissen oder Polster dienen dem unverletzten Bein als Halt. Die Pflegeperson achtet darauf, dass die verletzte Extremität achsengerecht positioniert ist.
Das Fibulaköpfchen muss zur Verhinderung einer Peronaeuslähmung druckfrei gelagert sein. Die Fersen werden hohl gelagert, eine Spitzfußprophylaxe ist durchzuführen ( ▶ Abb. 39.23).
Spitzfußprophylaxe.
Abb. 39.23 Zur Spitzfußprophylaxe wird der Fuß mit einem Schlauchverband versehen. Der Fuß wird anschließend mithilfe des Extensionsgestänges in 90°-Stellung fixiert.

Bettwäschewechsel Das Wechseln der Bettwäsche bei Extension der unteren Extremität erfordert 2 – 3 Pflegepersonen. Beim Anheben des Patienten hat eine Pflegeperson darauf zu achten, dass der Patient und die Lagerungsschiene gleichzeitig angehoben werden.
Extensionsgestänge
Über variable Extensionsgestänge, die am Fußende des Bettes befestigt sind, wird ein Seilzug über Rollen mit Gewichten belastet (s. ▶ Abb. 39.23). Das Zuggewicht wird vom behandelnden Arzt angegeben und beträgt ca. 10 – 15 % des Körpergewichts des Patienten.
Überprüfung des Extensionsaufbaus Die Gewichte müssen frei hängen. Die Zugschnüre dürfen nicht durch die Bettdecke belastet werden. Eine am Extensionsgestänge angebrachte Horizontalstange kann die Bettdecke halten.
Beförderung Bei der Beförderung des Patienten (z. B. zur regelmäßigen Röntgenuntersuchung) muss das Gewicht gehalten werden, damit es nicht gegen das Bettende schlägt. Abschließend wird jeweils die Position des Seilzugs und der Extensionsgewichte kontrolliert.
Komplikationen vermeiden
Lange Bettlägerigkeit verursacht Sekundärerkrankungen wie ▶ Dekubitus, ▶ Thrombose, ▶ Kontrakturen und ▶ Obstipation. Die Pflegeperson leitet pflegerische Maßnahmen nach individueller Risikoeinschätzung ein. Physiotherapie und medikamentöse Thromboseprophylaxe gehören zur begleitenden Behandlung. Die ausführliche Information des Patienten über die Pflegemaßnahmen fördert die aktive Mitarbeit.
Pflegerische Überwachung
Die Pflegeperson kontrolliert in regelmäßigen Abständen Durchblutung, Sensibilität und Beweglichkeit der Zehen bzw. Finger. Sie verabreicht die angeordneten Schmerzmittel und überprüft deren Wirksamkeit. Weiterhin kontrolliert die Pflegeperson die Haut und die Durchtrittsstellen der Extensionsnägel. Die Durchtrittsstellen werden auf Entzündungszeichen beobachtet. Das kann bei der täglichen Wundversorgung geschehen.
Die Haut wird auf Spannungsblasen inspiziert. Sie können aufgrund von Schwellungen oder drohenden Perforationen der Haut durch Bruchfragmente auftreten.
39.4.2.4 Ruhigstellende Stützverbände
Fallbeispiel
Leon ist 11 Jahre alt und kann richtig gut Inliner fahren. Natürlich fährt er immer mit Helm. Nur die lästigen Schoner für Knie und Handgelenke lässt er manchmal zu Hause, wenn seine Eltern es nicht merken. Heute hat er sich eine rasante Strecke ausgesucht. Immer wieder fährt er den steilen Berg hinunter. Doch auf einmal verliert er das Gleichgewicht und gerät ins Straucheln. Um den Sturz abzufangen, stützt er sich mit beiden Händen ab. Danach tut der rechte Unterarm ziemlich weh, er kann ihn kaum bewegen.
Ein ruhigstellender Stützverband wird angelegt
-
zur Fixierung nicht dislozierter, stabiler Extremitätenfrakturen,
-
bei Fissuren (= unvollständige Fraktur in Form eines Haarrisses),
-
nach geschlossener Reposition und
-
nach osteosynthetischen Eingriffen, Luxationen und Entzündungen.
Der Stützverband, der aus Gips oder Kunststoff besteht, stellt sowohl die Fraktur als auch das benachbarte Gelenk ruhig. Die Extremität wird in Funktionsstellung fixiert, um die negativen Folgen im Falle einer Versteifung gering zu halten und eine Gebrauchsfähigkeit im Verband zu ermöglichen. Die Behandlung dauert bis zum knöchernen Ausbau der Fraktur. Zur Auswahl stehen Gipsstützverbände, synthetische Stützverbände (Cast) und Orthesen.
Die Tabelle im Abschnitt „Pflegerische Methoden“ gibt Auskunft über die wichtigsten Vor- und Nachteile der Gips- oder synthetischen Verbände ( ▶ Tab. 39.3 ).
Gipsstützverbände Der ruhigstellende Gipsverband besteht aus pulverisiertem Gipsmaterial (Kalziumsulfat). Es wird auf Mullbinden gebracht und mit einem wasserlöslichen Kleber fixiert. Das beim Brennen abgegebene Wasser wird beim späteren Tauchen ins Wasser wieder aufgenommen und bewirkt die Verfestigung des Materials.
Synthetischer Stützverband Bei den heute gebräuchlicheren synthetischen Stützverbänden werden Trägermaterialien wie Polyester, Polypropylen oder Fiberglas (heute eher selten) verwendet. Die aus selbsthärtendem Harz bestehende Beschichtung ist bei allen Bandagen gleich. In der Handhabung ergeben sich einige Besonderheiten.
Praxistipp
Wegen der Verklebungs- und Allergiegefahr ist immer mit Einmalhandschuhen zu arbeiten. Die Kleidung ist zu schützen. Die raue Oberfläche des Verbandes kann mit einem dünnen Nylonstrumpf oder Schlauchmull abgedeckt werden.
Aufbau eines Stützverbandes
Der ruhigstellende Stützverband aus Gips oder Kunststoff wird in verschiedenen Arbeitsschritten aufgebaut.
Hautschutzmaßnahmen
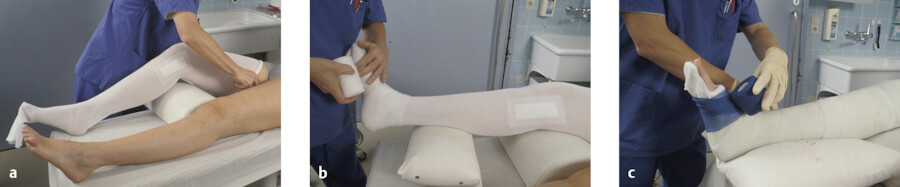
Nach Inspektion der Haut werden bestehende Wunden desinfiziert und mit einer sterilen Auflage versorgt. Die Wunden müssen regelmäßig beurteilt werden, weshalb in diesem Fall eine Gipsschiene von Vorteil sein kann. An der zu fixierenden Extremität wird ein Schlauchverband (z. B. Tg-Verband, Stülpa, ▶ Abb. 39.24 a) angebracht. Der faltenfreie Unterzug aus Schlauchmull ist hautfreundlich und gewährleistet den Feuchtigkeits- und Wärmeaustausch. Er verhindert
Anlegen eines Stützverbandes.
Abb. 39.24 Der ruhigstellende Stützverband aus Gips oder Kunststoff wird in mehreren Arbeitsschritten aufgebaut.
(Foto: T. Stephan, Thieme)
-
das Festkleben von Körperhaaren mit dem Stützverband,
-
den Juckreiz unter dem Verband,
-
das Verrutschen der Polsterwatte,
-
den Kontakt mit der Polsterwatte (Dermatitisgefahr).
An beiden Enden sollte der Schlauchmull ca. 5 cm länger als der Gips sein, um durch späteres Umschlagen ein Randpolster bilden zu können.
Polsterung
Gezielte Polsterung Zum Schutz vor Druck- und Scheuerschäden im Bereich oberflächlich verlaufender Nervenbahnen oder von Knochenvorsprüngen ohne ausreichende Weichteildeckung wird die gezielte Polsterung durchgeführt. Sie besteht aus speziell anmodellierten Polsterstücken aus Filz oder Schaumgummi.
Zirkuläre Polsterung Sie besteht aus Verbandwatte (zunehmend aus synthetischem Material) und wird von distal nach proximal gewickelt, sodass sich die einzelnen Polstertouren zur Hälfte überlappen ( ▶ Abb. 39.24 b). Um ein Polster am Rand des Stützverbandes zu erhalten, wird die Verbandwatte um 5 – 10 cm verlängert und abschließend umgeschlagen. An besonders druckgefährdeten Stellen wie Ferse oder Ellenbogen werden zusätzliche Polsterstücke aufgelegt.
Krepppapier/Schaumstoffbinden Eine Lage Krepppapier für Gipsverbände bzw. Schaumstoffbinden bei synthetischen Stützverbänden fixiert und komprimiert die Polsterung zusätzlich. Sie sind wasserabweisend imprägniert und schützen die Polsterwatte vor Feuchtigkeit.
Gipsbinden und Gipslonguetten
Gipsbinden sind gerollt und eignen sich für die zirkuläre Anlage eines Stützverbandes ( ▶ Abb. 39.24 c). Gipslonguetten sind gelegt bzw. gefaltet. Sie werden für Gipskonstruktionen verwendet, wenn Biege- und Druckkräften entgegengewirkt werden muss, wie das bei Extremitätenfrakturen der Fall ist. Die synthetischen Stützverbände stehen ebenfalls als Binde oder Longuette zur Verfügung, wodurch der fixierende Effekt mit weniger Gewicht erreicht werden kann.
Arbeitsregeln
1. Zügiges Arbeiten Die schnelle Abbindezeit von etwa 5 Min. erfordert eine strukturierte Ablauforganisation. Alle erforderlichen Materialien müssen vorab sorgfältig bereitgelegt werden.
2. Sauberes Tauchwasser Die Tauchwassertemperatur beeinflusst die Abbindezeit und damit die Verarbeitungszeit des Gipses. In der Regel beträgt die Wassertemperatur 20 – 25 °C. Zu warmes Tauchwasser (ca. 35 °C) kann zu Wärmeschäden an der Haut führen. Das Tauchwasser ist regelmäßig zu wechseln, damit die Abbindezeit durch Gipsreste nicht verkürzt wird. Die Technik des Tauchvorgangs ist abhängig davon, ob Binden oder Longuetten verarbeitet werden.
3. Richtiges Anlegen Die Gipsbinde wird flach und ohne Zug auf das entsprechende Körperteil abgerollt und mit der flachen Hand anmodelliert, wobei die Falten geglättet werden. Mit der letzten Gipsbinde wird die Unterpolsterung umgeschlagen. Dadurch entsteht ein Randpolster, das oben und unten die scharfen Randkanten verdeckt.
Für eine Gipsschiene wird die glatt gezogene Longuette auf die gepolsterte Körperstelle gelegt. Eine nasse Mullbinde fixiert die Schiene zunächst. Vor dem Abhärten sind die Randkanten vom Körper weg abzurunden. Die Mullbinde wird nach dem Aushärten durch eine elastische Binde ersetzt.
4. Vollständiges Austrocknen Nach 5 – 10 Min. ist der Gips abgebunden und damit nicht mehr verformbar. So lange muss die Extremität ruhiggehalten werden. Die vollständige Austrocknung dauert je nach Dicke des Gipses 24 – 36 Std. In dieser Zeit darf der Gips nicht belastet werden.
Anlegen eines Stützverbandes
Die Pflegeperson übernimmt folgende Aufgaben.
Vorbereitung und Lagerung
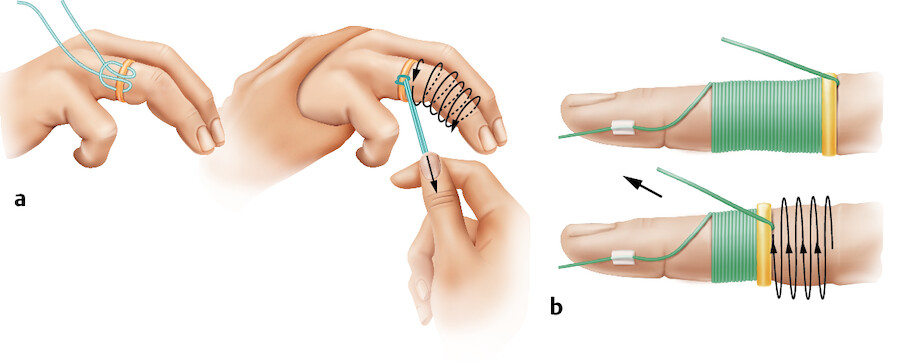
Der Patient wird durch den Arzt über Art und Dauer der Ruhigstellung informiert. Er trifft auch die Entscheidung über eine eventuelle Schmerzmittelgabe oder Kurznarkose. Die Pflegeperson hilft dem Patienten beim Ausziehen der Kleidung. Soll ein Stützverband an einer der oberen Extremität angelegt werden, müssen Nagellack und Fingerringe entfernt werden, um die Endglieder auf Schwellung und mangelnde Durchblutung beobachten zu können ( ▶ Abb. 39.25).
Ablösen eines Fingerrings bei Schwellung.
Abb. 39.25 Fingerringe an geschwollenen Fingern können mit Seife gleitfähig gemacht werden. Hilft dies nicht, wird der Ring mit einem Ringschneider durchtrennt.
Der Patient wird in eine geeignete Position gebracht. Neben der richtigen Positionierung des Körperteils dient eine gute Lagerung auch zur Entspannung. Eine angespannte Muskulatur würde den Gips zu weit werden lassen und die gewünschte Ruhigstellung nicht erreichen. Die Fixation endet i. d. R. 2 Querfinger breit vor Ellenbeuge, Achselhöhle, Leiste und Kniekehle, um die Bewegungsfreiheit des folgenden Gelenkes nicht einzuschränken.
Spalten des Gipses und Nachbereitung
Ein Stützverband, der nach einer frischen Fraktur oder nach einer Operation angelegt wurde, muss nach dem Aushärten (einschließlich aller Polsterungs-Schichten) gespalten werden. Das bedeutet, dass bei dem noch frischen Gips ein Streifen herausgeschnitten wird. Gespalten wird der Gips, um bei einer möglichen Weichteilschwellung Durchblutungsstörungen und Nervenschädigungen zu verhindern.
Als abschwellende Maßnahme sollte die betroffene Extremität frühzeitig, möglichst über Herzhöhe, hochgelagert werden. Das kann durch Hochstellen der Bettenden, Schienenlagerung, Keile oder Kissen ermöglicht werden. Auch trockene Kälte wirkt abschwellend.
Während des Aushärtens sollte der Gipsverband flächig und gleichmäßig aufliegen. Damit die Feuchtigkeit verdunsten kann, werden Gipsverbände nicht zugedeckt und die Einmalunterlage als Bettschutz wird häufig gewechselt. Bei sehr großen Gipsverbänden ist der Patient vor Auskühlung zu schützen.
Merke
Heben Sie den frischen Gips nur mit den flachen Händen. Vermeiden Sie Fingerabdrücke auf dem Gips, sie führen zu Druck auf dem darunterliegenden Gewebe.
Beobachten des Patienten
Während und nach der Gipsanlage werden Durchblutung, Sensibilität und Beweglichkeit der Zehen und Finger regelmäßig überprüft. Abweichungen vom Aufnahmebefund grenzen ab, was Unfall- und was Folgen der Gipsanlage sind.
Der Patient sollte wissen, dass er jede Auffälligkeit wie Schmerzen, Gefühllosigkeit, Kribbeln oder ein Spannungsgefühl sofort weitergeben soll. Bei Schmerzen ist zu klären, ob es sich um einen Wund-, Fraktur- oder Druckschmerz durch einen zu engen Gips handelt.
Ein zu lockerer Gips gewährleistet nicht ausreichend die Ruhigstellung. Deshalb muss u. U. nach dem Abschwellen ein neuer Gips angelegt werden.
Nicht jede Versorgung mit einem ruhigstellenden Stützverband verlangt eine stationäre Aufnahme. Geht der Patient nach dem Austrocknen des Gipsverbandes nach Hause, werden der Umgang mit dem Gips und evtl. auftretende Beschwerden bzw. Komplikationen mit dem Betroffenen besprochen. Ein Merkblatt wie in ▶ Abb. 39.26 bietet sowohl ambulanten als auch stationär verbleibenden Patienten Informationen und Hinweise über den Umgang mit ihrem frischen Stützverband.
Patienteninformation zum Umgang mit ihrem Erstgips.
Abb. 39.26

Fallbeispiel
Leon ist noch am Abend mit seinen Eltern in die chirurgische Ambulanz gefahren. Das Röntgenbild zeigte eine stabile nicht verschobene Radiusfraktur. Der Arzt meint, das sei die häufigste Fraktur nach einem Sturz. Leon bekommt einen Unterarmgips für 4 Wochen. Die Gesundheits- und Krankenpflegerin aus der Ambulanz erklärt ihm und seinen Eltern genau, worauf sie achten müssen. Am nächsten Tag sollen sie zur Gipskontrolle kommen. Ein paar Tage braucht er wohl noch ein bisschen Hilfe, z. B. beim An- und Ausziehen. Nur Klavier spielen und Sport treiben kann er ein paar Wochen lang nicht.
Komplikationen
Verschiedene Komplikationen können bei der Behandlung mit ruhigstellenden Verbänden auftreten:
-
Venenthrombose
-
Druckschäden
-
Durchblutungsstörungen
-
Kontrakturen
Druckschäden Sie können besonders im Bereich von Knochenvorsprüngen und oberflächlich verlaufenden Nervenbahnen entstehen und haben einen Ausfall der jeweiligen motorischen bzw. sensiblen Funktion zur Folge. Verhindert werden Druckschäden durch eine ausreichende Polsterung beim Anlegen des Stützverbandes. Weitere Ursachen für Druckschäden im Gipsverband können Fingerabdrücke durch unsachgemäßes Halten und Falten im Gips sein.
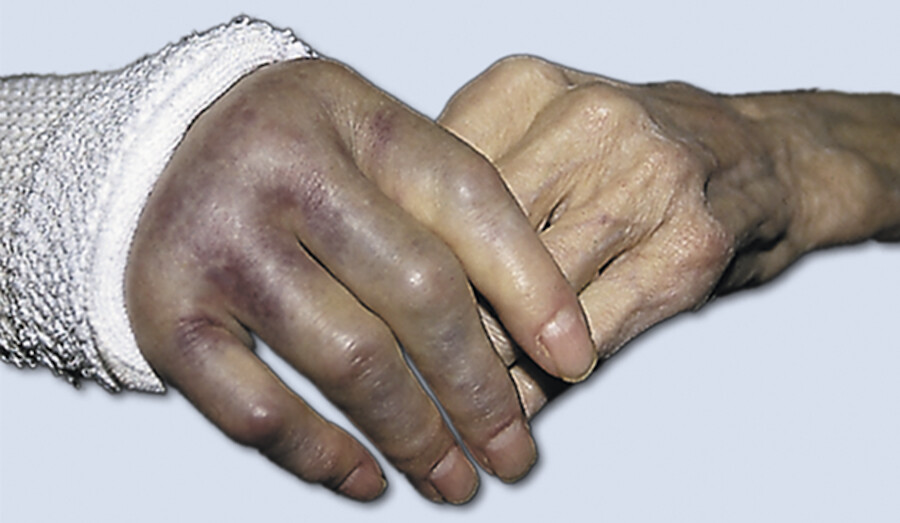
Durchblutungsstörungen Sie treten auf, wenn eine Schwellung nach der Fraktur besteht oder der Stützverband zu eng gewickelt wurde ( ▶ Abb. 39.27). Deshalb müssen zirkulär angelegte Gipse immer bis zum letzten Faden der Polsterung aufgeschnitten werden. Rundgipse werden erst nach Abschwellen der Extremität angelegt.
Fingerschwellung bei 80-jähriger Patientin bei zu engem Gipsverband.
Abb. 39.27
Kontrakturen Sie können durch die längerdauernde Ruhigstellung entstehen. Die Kapselstrukturen verkleben und die Gelenke versteifen. Deshalb sollten nur Gelenke immobilisiert werden, die unbedingt ruhiggestellt werden müssen. Benachbarte Gelenke, aber auch alle anderen nicht betroffenen Gelenke sind durch geeignete Übungen zu bewegen.
Entfernen des Stützverbandes
Röntgenkontrollen geben Auskunft über den Heilungsprozess der Fraktur. Zirkuläre Gipsverbände werden mit der oszillierenden Gipsfräse entfernt. Das Sägeblatt trennt mit den nur wenige Millimeter betragenden Schwingungen den Gips auf. Der stabilere Kunststoffverband muss von zwei Seiten zur Schale geschnitten werden, um die Extremität herauszuheben.
Praxistipp
Machen Sie den Patienten auf das Geräusch und die evtl. Wärmeentwicklung aufmerksam.
Bei unsachgemäßer oder ungeübter Anwendung kann es durch den Reibungswiderstand am Fräsenblatt und am Gips zu Wärmeschäden der Haut kommen. Um dem vorzubeugen, wird der Patient zur entspannten Haltung aufgefordert, damit sich bei entspannter Muskulatur ausreichend Platz zwischen Haut und Stützverband befindet. Die Schnittstelle sollte nicht über Knochen liegen. Die Fräse wird mit beiden Händen gehalten, eine Hand stützt die Säge sicher ab, damit die Säge nicht unkontrolliert tiefer fräst.
Nach dem Aufsägen wird der Gips mit dem Gipsspreizer oder dem Rabenschnabel aufgebrochen. Restliche Polsterschichten werden mit der Verbandschere aufgetrennt, so kann der Stützverband vollständig entfernt werden.
39.4.2.5 Ruhigstellende elastische Verbände
Ruhigstellende elastische Verbände werden v. a. bei Frakturen des Schultergelenks angelegt. Die angelegten Verbände werden während der Behandlung nicht abgenommen, deshalb müssen gefährdete Hautstellen (z. B. Achsel oder die Brust bei Frauen) geschützt werden. Haut darf nicht auf Haut liegen, ein Schutz aus Mullkompressen, evtl. mit Polsterwatte, ist erforderlich.
Rucksackverband Dieser Verband kommt bei Klavikulafrakturen zur Anwendung. Er besteht aus mit Watte gepolstertem Schlauchverband, der wie Rucksackriemen angelegt wird und die Schultern nach hinten zieht ( ▶ Abb. 39.28).
Gilchchrist Verband.
Abb. 39.28

Desaultverband Dieser Verband stellt das Schultergelenk und den Oberarm ruhig. Er besteht aus schulterbreitem Schlauchmull und wird mit Pflaster fixiert oder es wird ein Fertigverband mit Klettverschlüssen angelegt. Der betroffene Arm ruht in gebeugter Stellung vor dem Körper ( ▶ Abb. 39.29).
Desaultverband.
Abb. 39.29

Gilchristverband Dieser Verband wird bei Oberarmschaftfrakturen oder Verletzungen im Bereich des Schultergürtels angewandt. Ein Schlauchverband von 3 – 4-facher Armlänge oder ein Fertigverband mit Klettverschlüssen fixiert den betroffenen Arm in gebeugter Stellung vor dem Oberkörper ( ▶ Abb. 39.30).
Rucksackverband.
Abb. 39.30
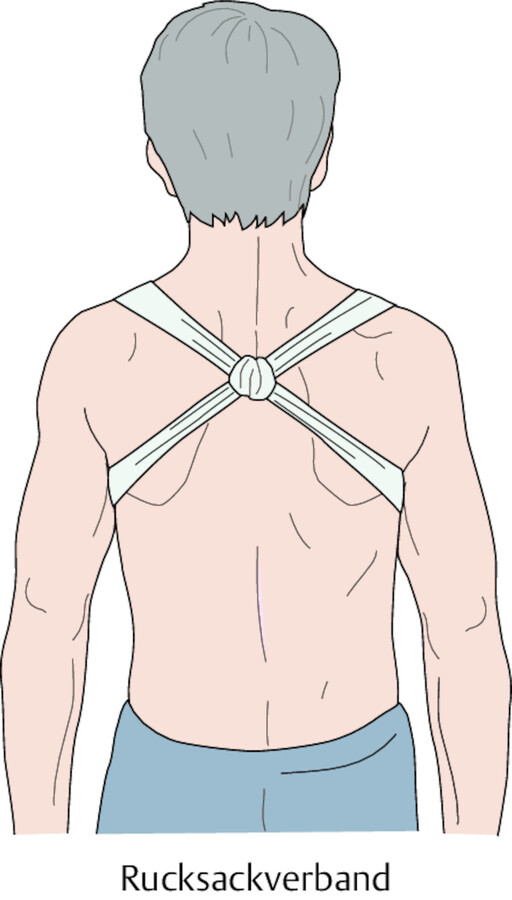
Dachziegelverband Diese Verbände werden z. B. bei Zehenfrakturen durch das schichtweise Übereinanderkleben von Pflasterstreifen angelegt.
Unterstützung bei den ATL
Die Ruhigstellung durch den Stützverband schränkt den Patienten in seiner Bewegungsfreiheit und damit auch seine Selbstständigkeit ein. Die Pflegenden passen ihre Unterstützung dem individuellen Bedarf des Patienten an.
Körperpflege Entsprechend der fixierten Körperpartie benötigt der Patient Hilfe bei der Körperpflege. Ein Gips ist unbedingt trocken zu halten, damit er keinen Schaden nimmt. Kunststoffstützverbände sind nicht empfindlich beim Kontakt mit Wasser. Spezielle Plastikbeutel, die den Verband wasserdicht verschließen, ermöglichen dem Patienten zu duschen.
Kleiden Zweckmäßige Kleidung, z. B. mit seitlichen Reißverschlüssen oder leichten Änderungen, und anfängliche Hilfestellung durch die Pflegeperson ermöglichen dem Patienten bald mehr Selbstständigkeit.
Lagerung und Mobilisation Kissen und Schienen unterstützen im Bett den Stützverband. Die erste Mobilisation nach vollständigem Aushärten des Gipses findet unter pflegerischer Begleitung und Unterstützung statt. Der korrekte Umgang mit Hilfsmitteln, wie Unterarmgehstützen oder Gehwagen, wird dem Patienten erklärt. Ein übergroßer Strumpf wärmt den ruhiggestellten Fuß und sorgt für eine ausreichende Durchblutung. Bei Rumpfgipsen benötigt der Patient Hilfe beim Anlegen des Gipskorsetts (2 Gipsschalen werden mit Klettverschlüssen fixiert). Hat er das Korsett an, ist der Patient mobil.
Essen und Trinken Bei Frakturen der oberen Extremität kann es nötig sein, den Patienten bei der Zubereitung der Mahlzeiten zu unterstützen, z. B. Fleisch schneiden oder Brötchen schmieren.
39.5 Pflege von Patienten mit Amputationen
39.5.1 Medizinischer Überblick
39.5.1.1 Definition
Unter einer Amputation wird die vollständige Entfernung eines Körperteils verstanden. Sie erfolgt als therapeutische Maßnahme (geplante Amputation) oder nach schweren gewaltsamen Einwirkungen als traumatische Amputation.
Geplante Amputation
Bei manchen Erkrankungen ist es trotz therapeutischer Bemühungen nicht möglich, das erkrankte Körperteil zu erhalten. In diesem Fall muss eine Amputation durchgeführt werden. Solche Erkrankungen können sein:
-
Durchblutungsstörungen bei Arteriosklerose oder Diabetes mellitus
-
maligne Tumoren
-
Infektionen
-
angeborene Missbildungen (selten)
Die Amputationshöhe wird so gewählt, dass eine gute Restfunktion erhalten bleibt und eine optimale Prothesenversorgung möglich wird. Um Komplikationen vorzubeugen, wird die Narbe außerhalb der späteren Belastungszone platziert und ausreichend mit Weichteilen gedeckt.
Traumatische Amputation
Durch schwere Unfälle wird ein Körperteil vollständig vom Gesamtkörper abgetrennt. In manchen Fällen ist es möglich, das abgetrennte Körperteil (Amputat) wieder anzunähen (zu replantieren). Voraussetzungen dafür sind z. B.
-
glatte Amputationsränder (keine ausgedehnten Weichteilzerstörungen),
-
saubere Wundverhältnisse,
-
eine gesunde Durchblutungssituation und
-
schnelles Handeln und korrekter Umgang mit dem Amputat.
Merke
Grundsätzlich kann niemals am Unfallort entschieden werden, ob eine Replantation möglich ist oder nicht. Das Amputat muss gesucht werden. Es ist nach dem Auffinden so zu behandeln, als werde es replantiert werden.
Verhalten am Unfallort Die betroffene Extremität darf zur Blutstillung nicht abgebunden werden. Sie wird mit einem (möglichst) sterilen Verband komprimiert und hochgelagert.
Versorgung des Amputats Das Amputat wird steril in Kompressen verpackt und dann in eine saubere Plastiktüte gelegt. Diese wiederum wird in eine zweite Tüte gelegt, die mit einem Wasser-Eis-Gemisch gefüllt ist ( ▶ Abb. 39.31). Durch die Kühlung verlängert sich die Haltbarkeit des Amputats.
Amputatversorgung.
Abb. 39.31 Der abgetrennte Körperteil wird in eine sterile Kompresse gewickelt und gekühlt.
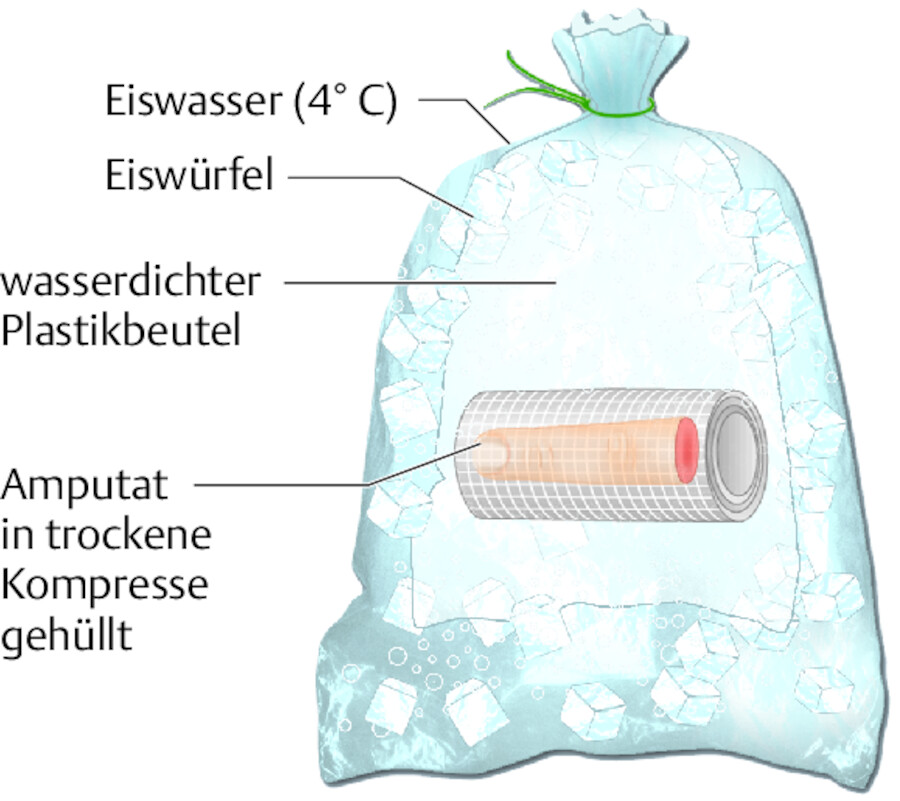
Merke
Auf keinen Fall sollte der abgetrennte Körperteil direkt mit Wasser oder Eis in Berührung kommen, damit weitere Schäden vermieden werden. Das verpackte Amputat wird so schnell wie möglich in das Krankenhaus gebracht.
Gelingt die Replantation nicht, ist das Ziel aller Bemühungen ein sauberer prothesengängiger Amputationsstumpf ohne Wundinfektion.
39.5.1.2 Komplikationen
Nach einer Amputation können folgende Komplikationen auftreten:
-
Nachblutungen
-
Kontrakturen
-
Stumpfödeme
-
Hauterkrankungen im Stumpfbereich (bakteriell oder pilzbedingt, z. B. Kontaktdermatitis, Follikulitis und Furunkel
-
Hauttumoren und Prothesenrandknoten
Viele Patienten leiden nach einer Amputation an Stumpfschmerzen und Phantombeschwerden.
Stumpfschmerz
Ein Stumpfschmerz kann direkt nach der Operation oder erst nach einer beschwerdefreien Zeit auftreten. Hält er länger als drei Monate an, wird vom chronischen Stumpfschmerz gesprochen. Der Stumpfschmerz kann folgende Ursachen haben:
-
mechanische Faktoren (z. B. schlecht angepasste Prothese)
-
vaskuläre Faktoren (z. B. Durchblutungsstörungen)
-
entzündliche Faktoren (z. B. Hautentzündungen und Osteomyelitis)
-
andere Erkrankungen (z. B. Hauttumore oder Neurome)
Stumpfschmerzen treten meist als Dauerschmerz auf, manchmal werden sie von Patienten als „attackenartig“ beschrieben. Häufig besteht eine Druckschmerzhaftigkeit des Stumpfes und im Narbenbereich eine Hyperästhesie (Überempfindlichkeit).
Phantombeschwerden
Es wird unterschieden zwischen Phantomschmerz und Phantomgefühl. Beim Phantomschmerz werden Schmerzen in dem nicht mehr vorhandenen Körperteil empfunden. Im Unterschied dazu wird das Phantomgefühl vom Patienten als Wahrnehmung beschrieben, bei der er das verlorene Körperteil oder Teile davon in seiner Bewegung erlebt oder in einer bestimmten Position spürt. Phantombeschwerden treten meist innerhalb weniger Tage bis Wochen nach der Amputation auf.
Phantomschmerzen Sie treten oft attackenartig auf. Sie können Stunden bis Tage anhalten und werden als sehr quälend empfunden. Ursachen können sein:
-
Störungen der schmerzleitenden Systeme in Rückenmark und Gehirn
-
Reizungen der Nervenenden
Prävention und Gesundheitsförderung
Die wirksamste Therapie gegen Phantomschmerzen ist die lückenlose Schmerztherapie in der prä- und postoperativen Phase!
39.5.1.3 Schmerztherapie nach Amputationen
Beim Stumpfschmerz sollte zunächst eine kausale Behandlung erfolgen. Bestehen die Schmerzen weiter, können ebenso wie bei Phantomschmerzen verschiedene Medikamentengruppen verabreicht werden, z. B.:
-
Schmerzmittel
-
Antikonvulsiva
-
Muskelrelaxanzien
-
schmerzdistanzierende Antidepressiva
-
Calcitonin
▶ Calcitonin ist ein natürliches Hormon der Schilddrüse und wirkt auf den Knochenstoffwechsel und auf die Schmerzschwelle. Die genaue Art der Wirkung auf den Phantomschmerz ist bisher unklar. Je früher die Therapie mit Calcitonin beginnt, desto besser sind die Ergebnisse.
Weitere Maßnahmen sind:
-
therapeutische Lokalanästhesie
-
Nervenblockaden, auch als kontinuierliche Periduralblockade mit Katheter
-
Bio-Feedback, Spiegeltherapie
-
lokale Kältebehandlungen oder Wechselbäder
-
Bei langwierigen Phantomschmerzen sollten die Betroffenen psychologisch bzw. psychotherapeutisch mitbehandelt werden.
39.5.2 Pflege- und Behandlungsplan
Für alle Patienten ist eine Amputation ein einschneidender Eingriff, der das zukünftige Leben verändert. Patienten, deren Amputation als zeitlich geplanter Eingriff erfolgt, können sich vorab mit der Situation auseinandersetzen. In manchen Fällen erhoffen sie sich sogar eine Verbesserung der Lebensumstände durch die Amputation der erkrankten Gliedmaßen.
Fallbeispiel
Herr Scheffler ist seit 30 Jahren insulinpflichtiger Diabetiker. Als Folge davon leidet er unter Durchblutungsstörungen und Polyneuropathien. Aus einer oberflächlichen Schnittverletzung entwickelte sich über Wochen eine ausgedehnte infizierte Wunde am linken Kleinzeh und am lateralen Fußrand. Lange hat Herr Scheffler die Wunde selbst behandelt und erst spät seinem Hausarzt gezeigt. Dieser überweist den Patienten zur weiteren Behandlung ins Krankenhaus. Die Wundversorgung erfolgt regelmäßig, die Blutzuckereinstellung wird optimiert. Es zeigen sich keinerlei Heilungstendenzen. Nach längerem stationären Aufenthalt und anschließender ambulanter Weiterbehandlung ist jetzt eine Vorfußamputation geplant.
Patienten nach einem Unfall stehen der Situation völlig unvorbereitet gegenüber. Sie brauchen Zeit und Unterstützung durch das therapeutische Team.
Fallbeispiel
Mark Herbert, 24 Jahre alt, hatte vor einem Jahr einen schweren Motorradunfall. Er verlor bei hoher Geschwindigkeit die Kontrolle über das Motorrad und geriet ins Schleudern. Die schweren Verletzungen machten eine Unterschenkelamputation nötig. Nach dreiwöchigem Krankenhausaufenthalt und anschließender Reha wurde er nach Hause entlassen. In allen Lebensbereichen fand eine Veränderung statt. Doch Mark H. hat mit der Unterstützung seiner Familie die Situation akzeptiert und nimmt die Herausforderungen an. Er bewegt sich sicher mit seiner Prothese und kann mit speziellen Prothesen wieder joggen.
39.5.2.1 Operationsvorbereitung
Die allgemeinen Operationsvorbereitungen können im Abschnitt ▶ „Präoperative Phase“ nachgelesen werden.
Aufnahmegespräch Hier können Informationen zum Verlauf der Behandlung und zur Prothesenversorgung gegeben werden. Vorab können auch schon Kontakte zu sozialen Diensten geknüpft werden, wenn es um die Klärung von Fragen in beruflicher oder finanzieller Hinsicht geht. Auch Gespräche mit einem Patienten in einer vergleichbaren Situation können ermutigen und motivieren.
Präoperatives Training Patienten mit Beinamputation können schon vor der Operation den Umgang mit Unterarmgehstützen erlernen. Dazu wird ihnen ein präoperatives Training angeboten. Der gezielte Aufbau von Muskelgruppen erleichtert die vermehrte Beanspruchung und vermeidet Muskelkater.
Merke
Alle vorbereitenden Maßnahmen müssen die besondere psychische Situation des Patienten berücksichtigen.
39.5.2.2 Postoperative Maßnahmen
Theoretische Grundlagen und pflegerische Aufgaben der allgemeinen Nachversorgung können im Abschnitt ▶ „postoperativen Phase“ nachgelesen werden. Zur Gewährleistung eines komplikationslosen Genesungsverlaufs stehen folgende Punkte im Vordergrund:
-
Überwachung auf Nachblutungen
-
Lagerung des amputierten Stumpfs
-
Unterstützung bei den ATL und Mobilisation
-
Wundbehandlung
-
Wickeln des Stumpfs
-
besondere Stumpfhygiene
-
Schmerzbehandlung
-
Prothesenversorgung
Überwachung auf Nachblutungen
Die Durchtrennung aller Blutgefäße im betroffenen Bereich bedingt eine hohe Nachblutungsgefahr. Der Verband und die Drainagen sind gezielt zu kontrollieren. Wegen der Gefahr der Verstopfung der Saugdrainagen ist die Sogkontrolle besonders wichtig.
Notfallmaßnahme Damit bei einer spontanen Nachblutung schnell reagiert werden kann, sollte in Patientennähe ein Abbindeschlauch deponiert sein. Alle an der Behandlung Beteiligten müssen wissen, wo sich dieser befindet und wie er angewendet wird.
Stumpfgips Wurde zur Verhinderung eines postoperativen Ödems intraoperativ ein Stumpfgips angelegt, ist die Überwachung des Wundgebiets erschwert. Nachblutungen können nicht frühzeitig erkannt werden. Deshalb muss bei übermäßigen Schmerzen, ansteigenden Temperaturen oder wenn Wundsekret durch den Verband dringt, der Arzt informiert werden, der die weiteren Maßnahmen anordnet. Der Gips wird nach 12 – 14 Tagen entfernt.
Lagerung des Stumpfs
Die spezielle Lagerung des Amputationsstumpfs hat 2 Schwerpunkte.
Entlasten des Wundgebietes
Intraoperativ werden Blut- und Lymphgefäße durchtrennt, sodass postoperativ die Weichteile anschwellen können. Um diesem Wundödem vorzubeugen, wird das Stumpfende in den ersten 24 Stunden auf ein kleines Kissen und hochgelagert. Bei ausgedehnten Schwellungen wird der Stumpf noch länger stundenweise auf 30° hochgelagert.
Merke
Bei Patienten mit gestörter Durchblutung (AVK) wird das Stumpfende horizontal oder tiefer gelagert und nicht hoch.
Vermeiden von Kontrakturen
Kontrakturen entstehen vorwiegend im benachbarten Gelenk. Sie behindern die schon eingeschränkte Beweglichkeit und die prothetische Versorgung. Beugekontrakturen in der Hüfte (nach Oberschenkelamputationen) und im Knie (nach Unterschenkelamputationen) erschweren das Aufrichten des Oberkörpers und die Gewichtsübernahme auf die Prothese. Deshalb wird der betroffene Körperteil gestreckt gelagert.
Lagerung bei Oberschenkelamputation Im Liegen wird das Hüftgelenk in Nullstellung, der Stumpf flach und gestreckt gelagert. Die korrekte Lagerung des Stumpfs wird im Rollstuhl durch entsprechende Hilfsmittel gewährleist. Der Patient sollte nur kurzzeitig am Bettrand sitzen. Zur Streckung des Stumpfs ist es möglich, dass der Patient zeitweise auf dem Bauch liegt.
Lagerung bei Unterschenkelamputation Eine zusätzliche Streckung des Unterschenkelstumpfs kann erreicht werden, wenn der Stumpf mit einem Sandsäckchen beschwert wird.
Lagerung bei Fingeramputationen Der Fingerstumpf wird geschient und befindet sich damit kontinuierlich in der Streckstellung.
Unterstützung bei den ATL und der Mobilisation
Eine frühzeitige Mobilisation am 1. oder 2. postoperativen Tag verringert das Dekubitusrisiko sowie die Gefahr einer Thrombose oder Pneumonie und stabilisiert den Kreislauf. Es kann sinnvoll sein, die Mobilisation mit anderen pflegerischen Maßnahmen zu verbinden, je nach Zustand des Patienten.
Ein Patient mit einer Amputation der oberen Extremitäten benötigt Hilfe bei der Körperpflege und beim Essen. Ein Patient mit einer Amputation der unteren Extremitäten benötigt Hilfe bei der Veränderung seiner Körperlage. Von zwei Pflegepersonen wird der Patient für kurze Zeit aufgerichtet und vor das Bett gestellt. Ausmaß und Dauer der Mobilisation hängen von mehreren Faktoren ab, z. B.:
-
Einschränkung des Patienten
-
Schmerzsituation
-
körperlichen Verfassung
Praxistipp
Eine Dauerversorgung mit einem Rollstuhl wird nicht angestrebt. Die Unbeweglichkeit und Bewegungseinschränkung im Hüft- und Kniegelenk würde dadurch gefördert und ein späteres Gehen evtl. unmöglich gemacht.
Physiotherapie Die Beeinträchtigung von Körperschema und Gleichgewicht ist erheblich und sollte schon frühzeitig mit einer täglichen speziellen Bewegungsschule durch Physiotherapeuten behandelt werden. Mobilisation und physiotherapeutische Behandlung werden nach Absprache im therapeutischen Team erweitert und intensiviert.
Ergotherapie Verluste von oberen Extremitäten verlangen eine Hilfsmittelberatung durch Ergotherapeuten, um die Greif- und Haltefunktion des verlorenen Körperteils auszugleichen.
Wundbehandlung
Das Pflegeziel ist eine ungestörte Wundheilung mit einer reizlosen weichen Narbe. Eine Wundheilungsstörung hätte die Verzögerung der Rehabilitation und Versorgung mit einer Prothese zur Folge.
Verbandwechsel Den Zeitpunkt des ersten Verbandwechsels bestimmt der Arzt. Er erfolgt unter den bekannten aseptischen Bedingungen. Der Patient sieht beim ersten Verbandwechsel auch das erste Mal seinen Amputationsstumpf. Das kann für ihn sehr belastend sein. Hier benötigt er die einfühlsame Unterstützung durch die Pflegeperson.
Grenzzonenamputation Eine Besonderheit stellt die sog. Grenzzonenamputation bei ▶ pAVK dar. Die Amputation im Zehen- oder Fußbereich erfolgt als Gangränabtragung im Übergang zwischen noch durchblutetem und gangränösem Gewebe. Die Wunde wird nicht durch eine Naht verschlossen, sondern heilt sekundär durch Granulation ( ▶ Abb. 39.32). Art und Häufigkeit des Verbandwechsels bestimmt der behandelnde Arzt.
Zwei Wochen nach einer Grenzzonenamputation granuliert die Wunde.
Abb. 39.32

Wickeln des Stumpfs
Um den venösen und lymphatischen Rückstrom zu unterstützen und den Stumpf prothesengerecht, d. h. konisch zu formen, wird der Stumpf gewickelt. Die Gestaltung und Intensität beim Wickeln bestimmt der Arzt.
Um Abschnürungen zu vermeiden, wird mit Kurzzugbinden in Achtertouren gewickelt. Begonnen wird an der Stumpfspitze, weiter wird mit abnehmendem Druck zum Körper hin gewickelt. Der diagonale Zug bestimmt die Formung des Stumpfes. Zur besseren Fixierung und um das Verrutschen zu vermeiden, wird das nächsthöhere Gelenk mit eingebunden ( ▶ Abb. 39.33). An Stellen mit geringer Weichteildeckung oder Knochenvorsprüngen sollten Stumpfkissen aus Schaumgummi oder Rollenwatte eingewickelt werden.
Wickeln des Stumpfs.
Abb. 39.33 Um den venösen und lymphatischen Rückstrom zu unterstützen und den Stumpf prothesengerecht konisch zu formen, wird er elastisch gewickelt.
(Fotos: K. Oborny, Thieme)
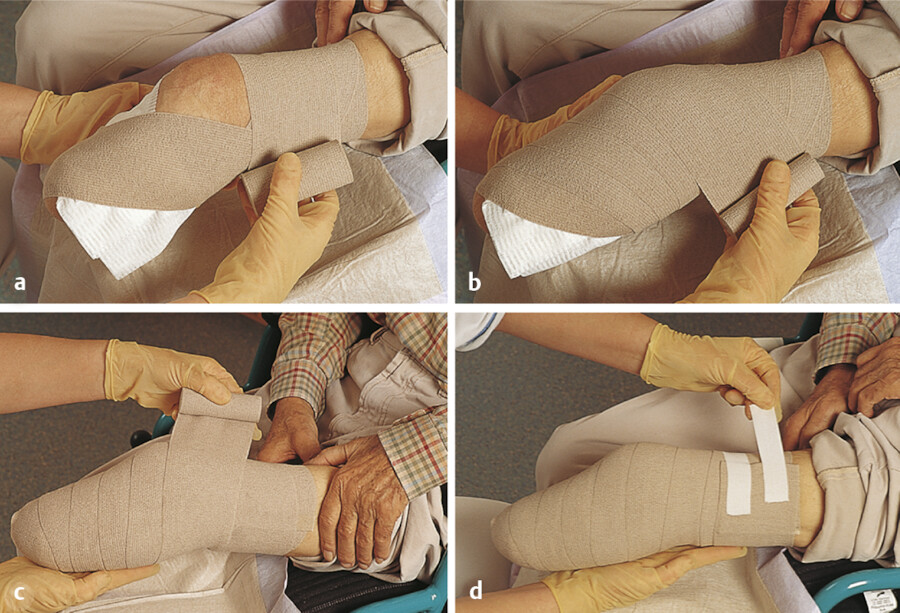
Praxistipp
Die Binde darf nicht zu straff angelegt werden, um einem druckbedingten Schwund der Stumpfmuskulatur vorzubeugen. Beim Wickeln des Oberschenkelstumpfes muss darauf geachtet werden, dass der Stumpf in Streckstellung gewickelt wird. Deshalb ist es empfehlenswert, den Stumpf im Stehen zu wickeln.
Der Stumpf wird so lange gewickelt, bis er vollständig abgeschwollen ist. Wenn der Patient das Wickeln erlernt hat, kann er dessen Durchführung selbst übernehmen. Es stehen auch individuell angepasste Kompressionsstrümpfe zur Verfügung.
Stumpfhygiene
Beim täglichen Wickeln muss der Stumpf sorgfältig von der Pflegeperson inspiziert werden. Sie achtet dabei auf die Stumpfhaut, die Hautdurchblutung und die Narbe.
Veränderungen im Narbenbereich, Druckstellen oder Hautreizungen können zu einer verzögerten Prothesenanpassung und zu einer Immobilität des Patienten führen und sollten verhindert werden.
Zur sorgfältigen Hautpflege gehört das tägliche kurze Waschen mit warmem Wasser und einer milden Seife. Die Haut darf nicht aufgeweicht werden. Nach der Waschung muss der Stumpf sehr sorgfältig abgetrocknet werden. Neigt ein Patient zu starker Schweißabsonderung, kann der Stumpf durch Abwaschungen oder Stumpfbäder mit Salbeitee behandelt werden.
Praxistipp
Ein Handspiegel hilft dem Patienten, seinen Stumpf besser zu sehen. Nach einer behutsamen Anleitung kann er selbstständig die Haut am Stumpf auf Veränderungen beobachten.
Abhärtungsmaßnahmen Nach abgeschlossener Wundheilung kann mit Abhärtungsmaßnahmen begonnen werden, damit die Stumpfhaut weniger empfindlich gegen mechanische Reize und die Druckbelastungen durch die Prothese ist. Der Patient wird über die Bedeutung dieser Maßnahmen aufgeklärt und frühzeitig in die Durchführung einbezogen:
-
nach dem Waschen kräftig abfrottieren
-
die Stumpfhaut nach dem Waschen weich bürsten
-
Luft und Licht an den Stumpf lassen
-
durchblutungsfördernde kaltwarme Wechselbäder
-
Narbenpflege mit pH-neutraler Salbe
-
Stumpfbewegungen in Materialien wie Sand, Erbsen oder spezieller Knetmasse
Schmerzbehandlung
Nach der Amputation kommt es in den ersten postoperativen Tagen zu den üblichen Wundschmerzen, die durch den großen Eingriff und die Traumatisierung des Gewebes bedingt sind. Maßnahmen zur Analgesie werden nach ärztlicher Anweisung durchgeführt. Das Schmerzmittel muss rechtzeitig verabreicht werden, um dem Patienten unnötige Schmerzen zu ersparen. Eine ▶ systematische Schmerzerfassung und eine gute Beobachtungsgabe werden dabei von den Pflegepersonen erwartet. Auch im Hinblick auf den ▶ Phantomschmerz ist der frühzeitige Therapiebeginn entscheidend für den Erfolg.
Prothesenversorgung
Definition
Prothesen sind ein Ersatz für das amputierte Körperteil und dienen neben dem optischen Ausgleich der Wiederherstellung der Steh-, Geh- und Greiffähigkeit.
Hand-, Arm- und Beinprothesen sind meist mit Gelenkvorrichtungen und der Möglichkeit zur Bewegung ausgestattet.
Prothesenarten
Nach der abgeschlossenen Wundheilung wird der Patient mit einer Übungsprothese versorgt und kann erste Geh- oder Greifübungen ausführen. Die individuelle Versorgung mit einer Prothese wird der Amputationsart sowie den Bedürfnissen und Möglichkeiten des Patienten angepasst ( ▶ Abb. 39.34). Über die Art des Prothesenaufbaus entscheiden z. B. das Alter und die Beweglichkeit.
Eine Prothese wird individuell an den Patienten angepasst.
Abb. 39.34
(Foto: K. Oborny, Thieme)
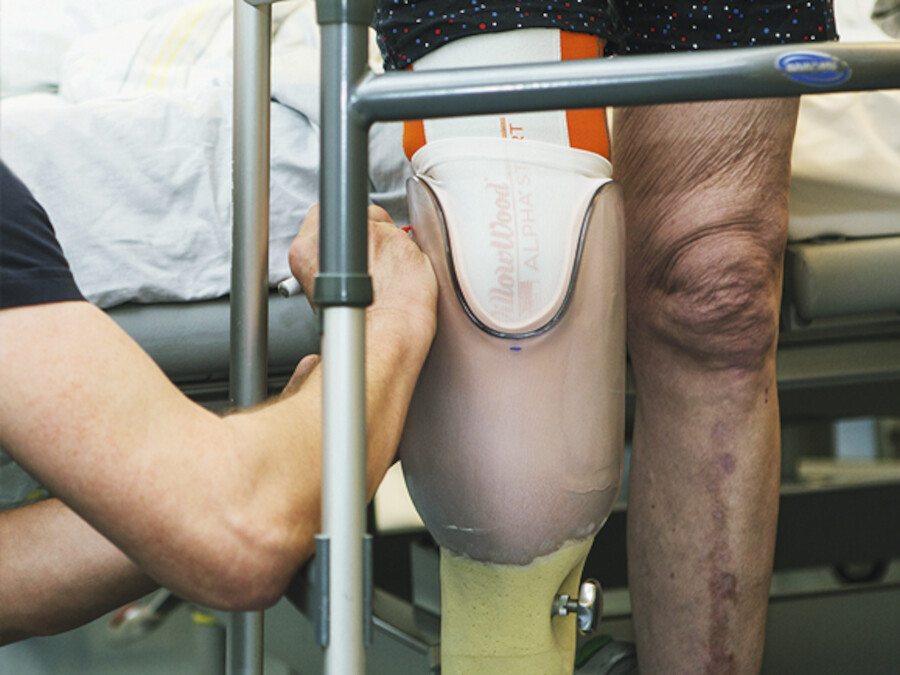
Oberschenkelprothesen Um ein möglichst normales Gangbild zu erreichen, sind die Prothesen mit Kniegelenken und Prothesenfuß versehen.
Armprothesen Hier gibt es so genannte Schmuckprothesen, die in Form und Farbe gut angepasst sind, aber keine Funktion übernehmen können. Eigenkraftprothesen übertragen die Bewegungen des Schultergürtels auf die Mechanik der Prothese. Myoelektrische Fremdkraftprothesen erfordern eine hohe Kooperation des Betroffenen. Willkürliche Muskelkontraktionen, verstärkt durch einen batteriebetriebenen Motor, ermöglichen z. B. das Öffnen und Schließen der Prothesenhand.
Prothesenanpassung
6 – 12 Monate nach der Amputation hat der Stumpf seine endgültige Form. Dann kann vom Orthopädiemechaniker eine individuelle Dauerprothese angepasst werden.
Merke
Jede Art der Prothesenversorgung erfordert unbedingt eine Schulung und Begleitung des Prothesenträgers durch Physio- oder Ergotherapeuten, um die Möglichkeiten, aber auch die Grenzen der Prothese aufzuzeigen.
39.5.2.3 Entlassungsberatung
Wenn die Wundheilung abgeschlossen und der Patient mit einer Übungs- oder Testprothese versorgt ist, wird er in einer ambulanten oder teilstationären Rehabilitationseinrichtung auf die Belastungen und Anforderungen seines Alltags vorbereitet.
Rehabilitationsmaßnahmen Der Umfang und die Möglichkeiten der Maßnahmen zur Rehabilitation orientieren sich am Alter und am Ausmaß der Einschränkungen. Besondere Trainingsprogramme verbessern die Greiffunktion bzw. die Steh- und Gehfähigkeit, leiten an zum Stufensteigen, Gehen auf unebenem Gelände und Überwinden von Hindernissen. Vor allem jüngeren Menschen wird Anleitung zur sportlichen Betätigung mit Prothese gegeben. Sie bieten die Möglichkeit, sich positiv mit der Situation auseinanderzusetzen und sich zu beweisen.
Berufliche Tätigkeit Ist eine Weiterbeschäftigung im Beruf nicht möglich, müssen Maßnahmen der Berufsfindung und eine Umschulung eingeleitet werden. Sie erfolgen in Abstimmung mit der Bundesagentur für Arbeit oder bei Berufsunfällen mit den Berufsgenossenschaften und Berufsförderungswerken.
39.6 Pflege von Patienten mit Osteosarkom
39.6.1 Medizinischer Überblick
39.6.1.1 Definition
Osteosarkome sind die häufigsten primären bösartigen Knochentumoren, deren Zellen direkt Knochen oder Osteoid bilden. Das Osteosarkom wächst aggressiv und schädigt Knochen und Gelenke. Es metastasiert hämatogen (über den Blutweg) und vorwiegend in die Lunge. Zum Zeitpunkt der Diagnosestellung sind bei 20 % der Patienten schon Metastasen nachweisbar.
Das Ewing-Sarkom (benannt nach dem US-amerikanischen Pathologen J. Ewing) geht vom Knochenmark aus und gehört ebenfalls zu den malignen Knochentumoren. Es tritt seltener auf als das Osteosarkom.
Primäre Knochentumoren Bösartige primäre Knochentumoren machen etwa 1 % aller bösartigen Tumore aus. Am häufigsten erkranken Kinder und Jugendliche zwischen dem 10. und 20. Lebensjahr, Jungen doppelt so häufig wie Mädchen. Knochentumore entstehen vorwiegend in der Längenwachstumszone der Röhrenknochen, bevorzugt in der Kniegegend ( ▶ Abb. 39.35).
Osteosarkome treten am häufigsten im Kniegelenk auf.
Abb. 39.35
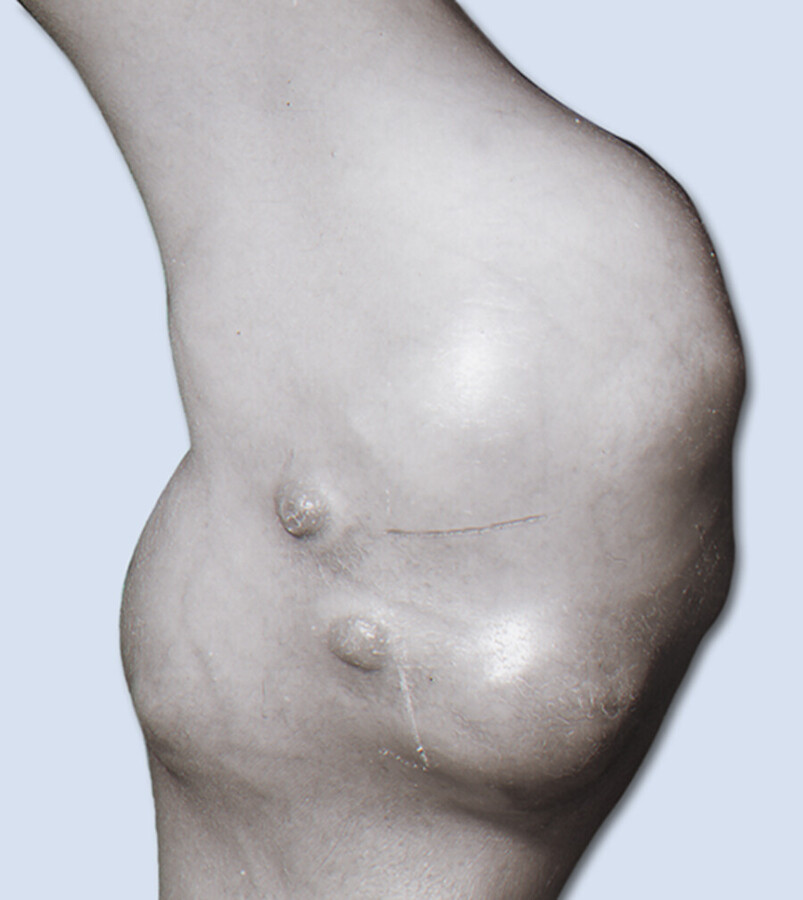
Sekundäre Knochentumoren Als sekundär auftretende Knochentumoren werden die Metastasen eines Primärtumors anderer Organe bezeichnet. Diese Tochtergeschwülste entstehen durch die Absiedelung von Zellen verschiedener anderer Krebsarten, z. B. bei ▶ Lungen-, Schilddrüsen- oder ▶ Brustkrebs.
39.6.1.2 Symptome
Die Patienten klagen schon im frühen Stadium über Schmerzen und Schwellungen im betroffenen Bereich, häufig in Ruhe oder in der Nacht. Die Haut über der Schwellung ist oft pergamentartig verdünnt. Es kann zur Spontanfraktur des Knochens kommen. Weitere allgemeine Symptome sind lokale Entzündungszeichen (Rötung, Schwellung, Überwärmung), Lymphknotenschwellung.
Die Patienten machen keinen „kranken Eindruck“ wie bei anderen Krebserkrankungen, Allgemeinsymptome wie ungewollte Gewichtsabnahme, Leistungsknick, Blässe oder Nachtschweiß treten häufig erst in fortgeschrittenen Stadien auf.
39.6.1.3 Diagnostik
Merke
Die endgültige Diagnose eines malignen Knochentumors erfolgt immer auf der Grundlage der histologischen Untersuchung einer Gewebeprobe.
Folgende Untersuchungen werden durchgeführt, um die Größe und Ausdehnung des Tumors zu bestimmen und Metastasen zu suchen:
-
Röntgenbild
-
Kernspintomografie
-
Computertomografie
-
bei sekundären Knochentumoren Skelettszintigrafie zur Suche nach weiteren Knochenmetastasen
-
vor einem geplanten operativen Eingriff evtl. eine Angiografie oder eine Ultraschalluntersuchung
Labor Es gibt keinen spezifischen Laborparameter, die alkalische Phosphatase kann erhöht sein und gilt als prognostisches Kriterium und als Verlaufsparameter.
39.6.1.4 Therapie
Knochentumore erfordern häufig eine Kombinationstherapie, die sich zusammensetzt aus
-
Chemotherapie und
-
operativer Therapie.
Die chemotherapeutische Behandlung wird sowohl neoadjuvant (vor einer Operation zur Reduzierung der Tumormasse) als auch adjuvant (nach der Operation) je nach Art und Stadium des Sarkoms in standardisierten Verfahren durchgeführt. Seit einigen Jahren werden postoperativ außerdem Immunmodulatoren (z.B. Mifamurtid) zur Verhinderung von Metastasen gegeben.
Der Erhalt der Extremität oder des Gelenks ist wesentliches Therapieziel. Ist es durch die präoperative Chemotherapie gelungen, den Primärtumor zu verkleinern, kann eine operative Resektion im Gesunden erfolgen. Dabei werden die betroffenen ▶ Extremitäten mit Endoprothesen stabilisiert. Kann eine Resektion des Tumorgewebes im Gesunden nicht realisiert werden, d. h. steht eine Amputation bevor, muss der Patient bereits während der vorbereitenden Chemotherapie ▶ auf eine Amputation vorbereitet werden. Auch einzelne Metastasen (z. B. in der Lunge) werden chirurgisch entfernt.
39.6.1.5 Prognose
Die Prognose hängt von verschiedenen Faktoren ab, z. B.:
-
Bösartigkeit des Tumorgewebes (Grading)
-
Lokalisation des Tumors
-
Metastasierung
39.6.2 Pflege- und Behandlungsplan
Das Osteosarkom tritt vorwiegend bei relativ jungen Menschen auf. Da die Krankheit oft lange Zeit unerkannt bleibt und zu Beginn keine Beschwerden verursacht, trifft die Diagnose „Knochenkrebs“ die Patienten völlig unerwartet. Sie stellt für den Patienten eine existenzielle Bedrohung dar.
Fallbeispiel
Kai ist 15 Jahre alt und geht in die 9. Klasse. Er ist ein sportlicher Typ und spielt Handball im Verein. Er trainiert zweimal in der Woche, am Wochenende finden die Spiele statt. Mit seinen Freunden geht er ab und zu zum Bowlen. Deshalb denkt sich Kai nichts weiter, als er eine leicht schmerzhafte Schwellung am Oberschenkel feststellt. Als die scheinbare Zerrung nach zwei Wochen noch nicht zurückgegangen ist, sucht er mit seiner Mutter den Hausarzt auf. Dieser untersucht ihn gründlich und schickt ihn sicherheitshalber zum Röntgen ins Krankenhaus. Dort spricht der Arzt erstmals von einem Knochentumor, von Chemotherapie und Operation. Erst nach der Biopsie wird Kai und seinen Eltern der genaue Behandlungsplan erläutert.
Die Schwerpunkte der Pflege ergeben sich aus der individuellen Situation des Patienten. Es gelten die Pflegemaßnahmen, wie sie im Kapitel ▶ „Prinzipien der Pflege und Therapie onkologischer Patienten“ beschrieben sind.
39.6.2.1 Vorbereitung auf die therapeutischen Maßnahmen
Wenn der Patient stationär aufgenommen wird, befindet er sich meist noch in der Auseinandersetzung mit der Diagnose.
Die Pflegeperson gibt dem Patienten im ersten Gespräch Informationen über den allgemeinen Stationsablauf und das weitere Vorgehen bezüglich geplanter Diagnostik und Therapie. Damit kann dem Patienten die Eingewöhnung erleichtert werden. Es gilt außerdem, eine offene und vertrauensvolle Situation zu schaffen, um weitere Gespräche zu ermöglichen, in denen die Sorgen und Probleme erfasst werden können. Dabei sollten auch die Angehörigen des Patienten mit einbezogen werden. Spezielle Pflegeziele werden formuliert. Ein Ziel ist es, Kontakte zu verschiedenen sozialen Diensten zu vermitteln, damit berufliche, familiäre und finanzielle Fragen beantwortet werden können.
39.6.2.2 Begleitung während der Therapien
Sowohl die Chemo- als auch die Strahlentherapie werden als belastend und kräftezehrend empfunden und sind von Nebenwirkungen begleitet. Die ausführliche Aufklärung vor Therapiebeginn ist daher unerlässlich.
Für die Pflege gilt es, den Patienten aufmerksam zu beobachten und ihn im Bedarfsfall zu unterstützen. Geeignete Pflegemaßnahmen und Prophylaxen werden in den Pflegeplan aufgenommen. Je nach Therapiephase können der Zustand des Patienten und damit die Pflegebedürftigkeit sehr schwanken. Deshalb ist der Pflegebedarf täglich einzuschätzen und der Pflegeplan anzupassen, wobei die Selbstständigkeit des Patienten gefördert werden muss.
Ausführlich wird die Begleitung bei Chemo- und Strahlentherapie im Kapitel ▶ „Prinzipien der Pflege und Therapie onkologischer Patienten“ beschrieben.
39.6.2.3 Pflege nach einer Operation
Allgemeine pflegerische Aufgaben in der perioperativen Phase können im Kapitel ▶ „Perioperative Pflege“ nachgelesen werden; zur Pflege von Patienten nach Amputationen siehe Kapitel ▶ „Pflege von Patienten mit Amputationen“.
Prävention und Gesundheitsförderung
Die regelmäßige Nachsorge hat einen hohen Stellenwert, um bei den zumeist jungen Patienten einen Rückfall bzw. eine Metastasierung möglichst früh zu erkennen.
39.7 Lern- und Leseservice
39.7.1 Literatur
39.7.1.1 Osteoporose
[1957] Deutsche Rheuma-Liga. Osteoporose Merkblätter. Bonn: Deutsche Rheuma-Liga Bundesverband e.V.; 2008
[1958] Greten H. Innere Medizin. 13. Aufl. Stuttgart: Thieme; 2010
[1959] Schwegler J, Lucius R. Der Mensch. Anatomie und Physiologie, 6. Auf. Stuttgart: Thieme; 2016
39.7.1.2 Rheumatische und degenerative Erkrankungen
[1960] Deutsche Rheuma-Liga: Positionen der Deutschen Rheuma-Liga zu den Anforderungen an die Pflegeversicherung. Bonn: Deutsche Rheuma-Liga Bundesverband e.V.; 2007
[1961] Niethard FU, Pfeil J. Duale Reihe: Orthopädie, 7. Aufl. Stuttgart: Thieme; 2014
39.7.1.3 Erkrankungen der Bandscheiben
[1962] Bäker BA, Reisky P. Die verrückte Bandscheibe. 2. Aufl. München: Ehrenwirth; 2001
[1963] Bonse M. Neurologie und Neurologische Krankenpflege. 8. Aufl. Stuttgart: Kohlhammer; 2010
[1964] Gravius S et al. Die lumbale Bandscheibenprothese. Dtsch Ärztebl 2007; 38
[1965] Krämer J, Wilcke A, Krämer R. Wirbelsäule und Sport. Empfehlungen von Sportarten aus orthopädischer und sportwissenschaftlicher Sicht. Köln: Deutscher Ärzte-Verlag; 2005
[1966] Paetz B, Benzinger-König B. Chirurgie für Pflegeberufe. 22. Aufl. Stuttgart: Thieme; 2014
[1967] Sitzmann F, Hrsg. Pflegehandbuch Herdecke. 3. Aufl. Berlin: Springer; 1998
[1968] Schirmer M. Degenerative Halswirbelsäulenerkrankungen mit unterschiedlichen Schmerzsymptomen. Notfall & Hausarztmedizin 2006; 30
[1969] Schirmer M. Segment LW4/5 als physiologischer Schwachpunkt des Menschen. Notfall & Hausarztmedizin 2004; 30
39.7.1.4 Frakturen
[1970] Imhoff A, Linke R, Baumgartner R. Checkliste Orthopädie. 2. Aufl. Stuttgart: Thieme; 2010
[1971] Kirschnick O. Pflegetechniken von A–Z. 4. Aufl. Stuttgart: Thieme; 2010
[1972] Paetz B, Benzinger-König B. Chirurgie für Pflegeberufe. 22. Aufl. Stuttgart: Thieme; 2014
39.7.1.5 Amputationen
[1973] Kickinger W. Beinamputationen. Facultas; 2005
[1974] Kirschnik O. Pflegetechniken von A-Z. 4. Aufl. Stuttgart: Thieme; 2010
[1975] Striebel HW. Therapie chronischer Schmerzen. 4. Aufl. Stuttgart: Schattauer; 2005
39.7.1.6 Osteosarkom
[1976] Pschyrembel. Klinisches Wörterbuch. 266. Aufl. Berlin: de Gruyter; 2014
[1977] Greten H. Innere Medizin. 13. Aufl. Stuttgart: Thieme; 2010
39.7.2 Kontakt- und Internetadressen
[1978] Aktion Gesunder Rücken e.V. (AGR), Postfach 103, 27443 Selsingen, Tel.: 04761/92 63 580. Im Internet: http://www.agr-ev.de; Stand: 18.12.2016
[1979] Bundesverband der deutschen Rückenschulen (BdR) e.V., Bleekstr. 22, 30559 Hannover, Tel.: 0511/350 27 30. Im Internet: http://www.bdr-ev.de; Stand: 18.12.2016
[1980] Bundesselbsthilfeverband Osteoporose e.V., Kirchfeldstr. 149, 40215 Düsseldorf, Tel.: 0211/30 13 14. Im Internet: https://www.osteoporose-deutschland.de/; Stand: 10.03.2017
[1981] Deutsche Rheuma-Liga Bundesverband e.V., Maximilianstr. 14, 53111 Bonn, Tel.: 0228/766 060, Fax: 0228/766 020. Im Internet: https://www.rheuma-liga.de/startseite/; Stand: 10.03.2017
[1982] Deutsche Schmerzliga e.V., Postfach 74 01 23, 60570 Frankfurt, Tel.: Adenauerallee 18, 61 440 Oberursel, Tel.: 069/13 82 80 22, Im Internet: http://www.schmerzliga.de; Stand: 18.12.2016
[1983] Kuratorium Knochengesundheit, Leipziger Str., 74889 Sinsheim, Tel.: 07261/92170. Im Internet: http://www.osteoporose.org/; Stand: 10.03.2017
[1984] Nakos – Nationale Kontakt- und Informationsstelle zur Anregung und Unterstützung von Selbsthilfegruppen: www.nakos.de; Stand: 18.12.2016
[1985] http://www.bfo-aktuell.de; Stand: 18.12.2016
[1986] http://flexikon.doccheck.com/de/osteoporose; Stand: 18.12.2016
[1987] http://www.orthopaede.com; Stand: 18.12.2016
[1988] http://www.osteoporose.org; Stand: 18.12.2016
[1989] http://www.osteoporose-deutschland.de; Stand: 18.12.2016
[1990] http://www.rheuma-liga.de; Stand: 18.12.2016
[1991] http://www.schmerz-therapie-deutschland.de; Stand: 18.12.2016