
40 Pflege von Patienten mit Erkrankungen der Augen, des Hals-Nasen-Ohrenbereiches oder der Haut
Anatomie und Physiologie im Fokus
(nach Schwegler u. Lucius 2016)
Das Auge im Überblick
Das Auge ist zusammen mit dem Ohr die eigentliche Schnittstelle zwischen dem Selbst und seiner Umwelt. Mehr als 90 % aller Informationseinheiten erreichen das Gehirn durch einen dieser Kanäle. Wie ein Kugelgelenk kann sich das Auge in allen 3 Raumachsen bewegen: nach außen und innen, nach oben und unten, Drehung nach innen und nach außen.
Augapfel
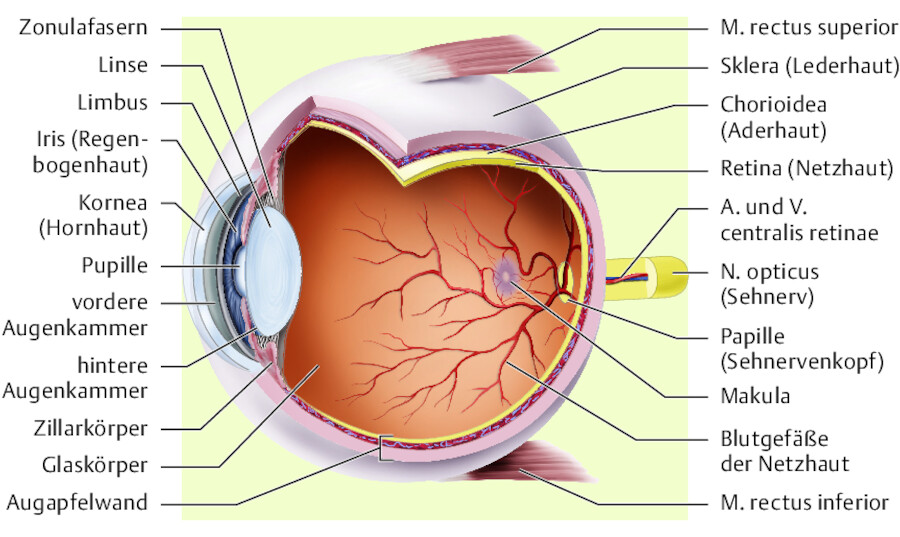
Er besteht aus 3 Schichten: derber äußerer Lederhaut, gut durchbluteter Aderhaut und lichtempfindlicher Netzhaut ( ▶ Abb. 40.1). Da Lederhaut und Aderhaut lichtundurchlässig sind, gelangt das Licht durch die Pupille ins Innere des Auges. Ihre Größe wird von der Iris bestimmt und vom vegetativen Nervensystem gesteuert. Die transparente Bindehaut kleidet die Innenseite der Lider aus und bedeckt einen Teil des Augapfels. Die Hornhaut ist der einzige Teil des Körpers, an dem straffes Bindegewebe vollständig durchsichtig wird.
Augapfel.
Abb. 40.1 Die Bulbuswand wird von außen nach innen aus Lederhaut, Aderhaut und Netzhaut gebildet. Der durchsichtige Glaskörper füllt den ⅔ des Augapfelvolumens ausmachenden Glaskörperraum aus.
Linse
Unmittelbar hinter der Iris befindet sich die Linse. Sie besitzt wie die Hornhaut keine Blutgefäße. Die Linse besteht aus einem Kern und Rinde, die von einer Kapsel umschlossen werden.
Glaskörper
Den größten Teil des Augeninnenraums nimmt der Glaskörper ein. Eine feine Membran grenzt diese gallertige Masse von der Hinterkammer ab. Der Glaskörper ist normalerweise völlig klar und besteht zu über 98 % aus Wasser.
Netzhaut
Sie besteht aus verschiedenen Nervenzellschichten mit lichtempfindlichen Sensoren (Zapfen und Stäbchen). Am hinteren Pol der Netzhaut befinden sich der Austritt des Sehnervs und der gelbe Fleck (Macula lutea) mit der Fovea, der Stelle des schärfsten Sehens. In der Fovea stehen die Zapfen am dichtesten. An der Austrittsstelle des Sehnervs treten die arteriellen Gefäße ins Auge ein und verzweigen sich bäumchenartig.
40.1 Pflege von Patienten mit Augenerkrankungen
40.1.1 Medizinischer Überblick
40.1.1.1 Definition
Augenerkrankungen sind angeborene oder erworbene Anomalien, Entzündungen, degenerative oder dystrophische Veränderungen
-
der Lider,
-
des vorderen Augenabschnitts (Konjunktiva, Kornea, Sklera, Augenvorderkammer, Kammerwinkel, Iris, Augenlinse, Zonulafasern, Ziliarkörper),
-
des Augenhinterabschnitts (Sklera, Choroidea, Retina, Glaskörper, Papille),
-
des Sehnerven,
-
der Sehbahn einschließlich des Chiasma opticum (Sehnervenkreuzung) und der Sehrinde und
-
der Orbita.
Stellvertretend für die Vielzahl von Augenerkrankungen werden das Offenwinkelglaukom und die Netzhautablösung näher vorgestellt.
Offenwinkelglaukom
Fallbeispiel
Die 45-jährige Angela Meyerbrink hat sich bei ihrer Augenärztin einen Termin für eine Kontrolluntersuchung geben lassen: „Beschwerden habe ich eigentlich keine, aber abends, wenn ich müde bin, kann ich nicht mehr richtig lesen. Brauche ich vielleicht eine Lesebrille?“ Nach ihrer Untersuchung fasst Frau Dr. Elke Schröder zusammen: „Ja, Frau Meyerbrink, sie benötigen tatsächlich ihre erste Lesebrille, das ist ganz normal. Auch sonst sind Ihre Augen bisher gesund, aber ich habe auch Ihren Augeninnendruck gemessen und der ist mit 24 mmHg etwas zu hoch und muss beobachtet werden.“
Definition
Das Offenwinkelglaukom ist eine schmerzfreie Sehnervenerkrankung mit zunehmender Zerstörung der Nervenfaserschicht, Aushöhlung des Sehnervenkopfes (Papillenexkavation) und Gesichtsfelddefekten. Ein wesentlicher Risikofaktor ist eine Erhöhung des Augeninnendrucks.
Glaukome können angeboren oder erworben sein, z. B. durch eine Augenerkrankung sekundär entstehen.
Prävention und Gesundheitsförderung
An einem Offenwinkelglaukom sind in Deutschland ca. 950 000 Menschen erkrankt. Unbehandelt kann es zur Erblindung führen. Da das Offenwinkelglaukom nicht schmerzhaft ist und der Patient meistens noch sehr lange Zeit gut sieht, obwohl bereits schon bleibende Augenschäden vorliegen, können nur Vorsorgeuntersuchungen eine Gefährdung aufdecken. Als eine der wichtigsten Präventionsmaßnahmen in der Augenheilkunde sollte deshalb bei allen Männern und Frauen, die älter sind als 40 Jahre, der Sehnervenkopf (die Papille) am Augenhintergrund beurteilt und der Augeninnendruck gemessen werden.
Netzhautablösung
Fallbeispiel
Alex und seine Frau sitzen beim Frühstück und lesen die Zeitung. Kristina schüttelt den Kopf. „Was ist denn los?“, fragt Alex. „Ach, ich sehe dauernd so schwarze Punkte. Die stören ganz schön! Und weißt du noch, als ich dir letztens von diesen Lichtblitzen erzählt habe? Nun bin ich schon so kurzsichtig und seh’ fast nix ohne Brille und jetzt auch noch das! Ich muss unbedingt mal wieder zum Augenarzt.“
Definition
Die Netzhautablösung (Amotio retinae, Ablatio retinae) stellt eine Trennung von Netzhaut und retinalem Pigmentepithel dar.
Ursachen können sein:
-
Riss in der Netzhaut (rhegmatogene Netzhautablösung)
-
Membranen unter, auf und über der Netzhaut oder im Glaskörperraum (traktions-(zug-)bedingte Netzhautablösung), z. B. bei ▶ Diabetes mellitus
-
Exsudationen bei Aderhautmelanomen oder Metastasen (exsudative Netzhautablösung)
Mit speziellen Netzhautoperationen (Plombe, Cerclage, Vitrektomie) kann die Netzhaut heute meistens wieder angelegt werden. Unbehandelt führt eine Netzhautablösung häufig zur Erblindung.
Arzneimittel im Fokus
Arzneimittel in der Augenheilkunde
Augenerkrankungen werden sehr häufig mit Augentropfen, -salben und -gelen behandelt oder die Wirkstoffe unter die Bindehaut (subkonjunktival) oder in den Glaskörper (intravitreal) gespritzt. Nur in Ausnahmefällen werden systemische Medikamente verabreicht. Verschiedene Medikamentengruppen finden Anwendung.
Miotika
Dies sind pupillenverengende Medikamente, die zu einer Miosis (Verengung der Pupille) führen. Sie werden prä- und postoperativ eingesetzt und in der Glaukomtherapie (z. B. Pilocarpin).
Mydriatika und Zykloplegika
Dies sind Medikamente, die pupillenerweiternd wirken (Mydriasis = weite Pupille). Zykloplegika (z. B. Atropin) lähmen außerdem vorübergehend die Fähigkeit des Auges zur Akkommodation, d. h. unter Zunahme der Brechkraft nahe gelegene Objekte auf der Netzhaut scharf abzubilden. Sie werden z. B. zur Untersuchung des Augenhintergrunds und prä- und postoperativ appliziert.
Antiglaukomatosa
Sie wirken vorwiegend lokal und werden zur Senkung des Augeninnendrucks instilliert.
Künstliche Tränen
Dies sind Tränenersatzmittel zur symptomatischen Behandlung eines trockenen Auges oder bei unzureichendem Lidschluss, z. B. bei ▶ beatmeten Patienten.
Antibiotika und Virustatika
Sie werden zur Behandlung bakterieller Entzündungen und Virustatika zur Therapie durch Viren hervorgerufener Erkrankungen verordnet. Sie werden als Augentropfen oder -salben und seltener intravenös oder in Tablettenform verabreicht.
Antiallergika
Zur Therapie allergischer Augenerkrankungen der Lider und der Bindehaut stehen zahlreiche Antiallergika als Augentropfen oder -salben zur Verfügung. Einige Patienten entwickeln aber auch Allergien gegen die in den Antiallergika enthaltenen Konservierungsmittel. Häufig können ihre Symptome mit in Einmaldosis-Ophthiolen enthaltenen konservierungsmittelfreien, antiallergischen Augentropfen beseitigt werden.
Entzündungshemmende Medikamente
Stark entzündungshemmende Medikamente sind nichtsteroidale Antiphlogistika und Steroide. Sie werden z. B. bei schweren Entzündungen des Augeninneren verabreicht. Antiseptisch und desinfizierend wirkende Augentropfen und -salben wirken keimabtötend sowie entzündungs- und sekretionshemmend. Sie werden bei unspezifischen entzündlichen Erkrankungen des Auges appliziert.
Antimykotika
Sie werden selten verabreicht. Antimykotika beeinflussen das Pilzwachstum.
Immunsuppressiva und Zytostatika
Immunsuppressiva unterdrücken oder schwächen die Immunantwort. Zytostatika schädigen noch zusätzlich bösartig entartete Zellen. Sie werden nur angewandt, wenn das Sehvermögen in Gefahr ist, z. B. bei einer schweren Uveitis (Entzündung der mittleren Augenhaut).
VEGF-Hemmer
Diese Medikamente (VEGF = vascular-endothelial-growth-factor) enthalten Wirkstoffe, die das Wachstum von Gefäßen im Auge hemmen. Sie werden am häufigsten bei einer besonderen Form der altersabhängigen Makuladegeneration (feuchte AMD) und der diabetischen Retinopathie in den Glaskörper gespritzt und können eine Erblindung verhindern oder hinauszögern.
Lokalanästhetika
Sie werden z. B. bei der Augeninnendruckmessung und vor einer Hornhautfremdkörperentfernung instilliert.
40.1.2 Pflege- und Behandlungsplan
40.1.2.1 Augenpflege
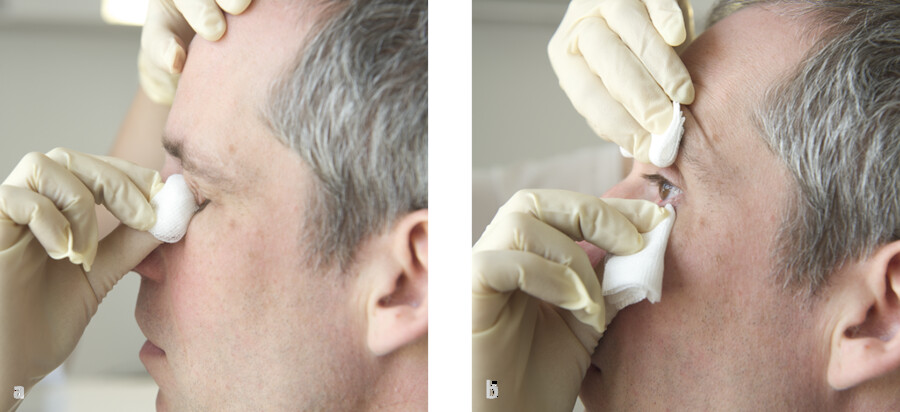
Die Augenpflege stellt eine spezielle Reinigungsform des Auges dar, bei deren Durchführung Salben- und Tropfenreste von Ober- und Unterlidhaut des Auges entfernt werden ( ▶ Abb. 40.2). Sie erfolgt mindestens einmal täglich, z. B. vor der ärztlichen Visite. Besteht eine starke Wundsekretbildung, kann es notwendig werden, die Augenpflege öfter durchzuführen. Patienten empfinden die Augenpflege häufig als sehr angenehm.
Augenpflege.
Abb. 40.2 a Reinigung von Ober- und Unterlid bei geschlossenem Auge, b Reinigung des Unterlids bei geöffnetem Auge.
(Foto: W. Krüper, Thieme)
Merke
Die gewissenhafte Augenpflege unter aseptischen Bedingungen stellt das Kernstück der Augenbehandlung dar. Der postoperative Verlauf ist auch von der Augenpflege abhängig.
Material
Zur Vorbereitung werden auf einem Tablett gerichtet:
-
Händedesinfektionsmittel
-
Einmalhandschuhe bei septischen Augen
-
sterile Pflaumentupfer (z. B. 5er-Packung) und sterile Kompressen
-
sterile 0,9 %ige Kochsalzlösung oder Ringer-Lösung mit Überlaufkanüle (keine kalten Flüssigkeiten verwenden)
-
Nierenschale (Pappschalen nur als Abwurfschalen)
Durchführung
Zunächst wird der Patient über Zweck und Vorgehensweise informiert. Anschließend wird er gebeten, eine sitzende oder liegende Position einzunehmen. Nach der Händedesinfektion nach Hygieneplan und gegebenenfalls nach dem Überstreifen der Einmalhandschuhe werden die sterilen Pflaumentupfer über der Nierenschale mit der sterilen 0,9 %igen Kochsalzlösung befeuchtet und die Augen gereinigt.
Die Reinigung der Ober- und Unterlidhaut des geschlossenen Auges erfolgt mit der unberührten Seite des Tupfers, ohne Druck auszuüben, vom inneren zum äußeren Lidwinkel durch bogenförmige Tupferführung, zunächst entlang des Unterlids, anschließend mit neuem Tupfer entlang des Oberlids. Dabei darf nicht gerieben werden.
Es wird auch die Tupferführung von außen nach innen gelehrt – die hier beschriebene Vorgehensweise wird von uns aus praktischen und hygienischen Gründen bevorzugt.
Bei stark verklebten Augenlidern ist es sinnvoll, den feuchten Tupfer für kurze Zeit auf dem Auge zu belassen, um die Verklebung aufzuweichen. Die gebrauchten, kontaminierten Tupfer werden in die bereitgestellte Nierenschale abgeworfen. Eine intensivere Reinigung des Unterlids ist möglich, wenn der Patient die Augen während des Waschvorgangs öffnet und nach oben schaut. Eine Wiederholung des Auswaschvorgangs erfordert jeweils die Verwendung frischer Tupfer. Abschließend können die Augenlider mit einer Kompresse trocken getupft werden.
40.1.2.2 Instillation von Augenmedikamenten
Die für einen bestimmten Patienten vom Arzt verordneten Augenmedikamente und sterilisierte Zellstofftupfer werden in einer Dose, die mit dem Namen des Patienten versehen ist, gerichtet und auf sein Zimmer gebracht (Ausnahme: Kinder). Applikationen aus diesen Tropfflaschen bzw. Tuben erhält nur dieser Patient.
Merke
Bei der Applikation von Augenmedikamenten gilt die 6-R-Regel: richtiger Patient, richtiges Auge, richtiges Medikament zum richtigen Zeitpunkt, richtige Applikationsform und richtige Dokumentation.
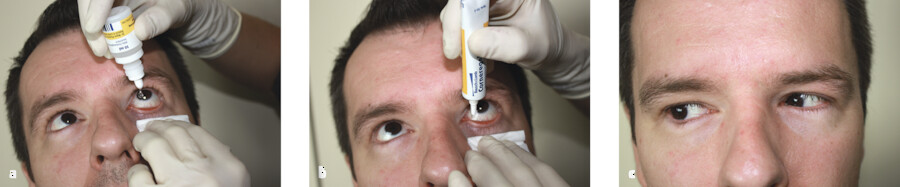
Das Verfallsdatum der Augenmedikamente muss regelmäßig kontrolliert werden, damit Wirksamkeit und Keimfreiheit gewährleistet werden können. Bei Verfärbungen und Ausflockungen wird das Medikament verworfen oder zur Ursachenklärung an die Apotheke zurückgegeben. Nach dem Öffnen der Originalverpackung sind die meisten Augenmedikamente nur sehr begrenzt haltbar, weshalb sie mit dem Öffnungsdatum versehen werden ( ▶ Abb. 40.3).
Augenmedikamente.
Abb. 40.3 a Verschiedene Augentropfen in Flaschenform und als Einmaldosis, b neue Tropfen- oder Salbenpackungen werden mit dem Anbruchdatum versehen.

Material
Neben den verordneten Medikamenten werden folgende Gegenstände benötigt:
-
Händedesinfektionsmittel
-
Einmalhandschuhe bei septischen Augen
-
sterilisierte Zellstofftupfer (3,5 × 5 cm)
-
Abwurfschale
Durchführung
Nach der Händedesinfektion und dem Überstreifen der Einmalhandschuhe wird der Patient gebeten, den Kopf in den Nacken zu legen und nach oben zu sehen. Kontaktlinsen müssen bis auf wenige ausdrücklich vom Arzt festgelegte Ausnahmen vor der Gabe von Augenmedikamenten entfernt werden. Sie können sich sonst verfärben.
Das Unterlid wird mithilfe eines Tupfers nahe dem Wimpernrand leicht nach unten gezogen, sodass der untere Bindehautsack zu sehen ist. Die Pflegende stützt die Hand, die das Tropffläschchen oder die Salbentube hält, an der Stirn des Patienten ab, um Verletzungen durch unkontrollierte Bewegungen des Patienten zu vermeiden ( ▶ Abb. 40.4).
Instillation von Augentropfen und Augensalben.
Abb. 40.4 a Einträufeln von Augentropfen, b Einbringen von Augensalbe. c Der Patient wird gebeten, nach rechts, links und unten zu blicken.
(Foto: K. Gampper, Thieme)
Augentropfen Die Augentropfen werden aus dem senkrecht gehaltenen Fläschchen in den unteren Bindehautsack geträufelt. Die Tropfflasche bzw. die Salbentube darf weder Wimpern, Lidränder, Bindehaut noch Hornhaut berühren, da eine Kontamination mit Keimen oder Augenverletzungen die Folge sein könnte.
Praxistipp
Werden mehrere Augentropfen hintereinander verabreicht, instillieren Sie diejenigen zuletzt, die der Patient als unangenehm empfindet – z. B. weil sie ein „Brennen“ verursachen. Andernfalls könnte ein Lidkrampf die weitere Applikation beeinträchtigen.
Augensalbe Zur Applikation der Augensalbe wird ein etwa 0,5 cm langer Salbenstrang direkt aus der Tube in den unteren Bindehautsack gegeben. Nach der Instillation wird der Patient gebeten, bei noch zurückgezogenem Unterlid nach unten zu sehen. Dadurch verteilt sich die Salbe in der unteren Umschlagsfalte und wird nicht aus dem Auge herausgepresst. Nach der Applikation wird die Salbentube sofort geschlossen, damit die Spitze nur mit der Kappeninnenseite in Kontakt kommt.
Merke
Sind sowohl Augentropfen als auch Augensalben zum selben Zeitpunkt verordnet worden, werden Augentropfen zuerst gegeben, da sie nach der Salbenapplikation nicht mehr so gut vom Auge aufgenommen werden können.
Überschüssige Tropfen oder Salbe werden vorsichtig mit einem sterilisierten Zellstofftupfer abgewischt. Die gebrauchten und kontaminierten Tupfer werden in die Nierenschale abgeworfen. Abschließend sollte der Patient noch darüber informiert werden, dass das Nachwischen mit Fingern oder Taschentüchern zur Keimverschleppung führen kann, und deshalb unterlassen werden sollte.
40.1.2.3 Augenspülung
Eine Augenspülung erfolgt meistens notfallmäßig bei Verätzungen des Auges mit Laugen oder Säuren. Am Unfallort ist es wichtig, so rasch wie möglich mit sauberem Leitungswasser oder Mineralwasser zu spülen und die Spülung nicht zu unterbrechen. In der Klinik kann der Vorgang ohne Zeitverzögerungen optimiert werden.
Material
Für die Augenspülung werden folgende Gegenstände benötigt:
-
wasserdichte Unterlage
-
Plastikschürzen für Patienten und Pflegende
-
Auffangschale
-
Lokalanästhetikum
-
Lidsperrer, Lidhaken
-
sterile Tupfer
-
Spritze oder Spülkontaktlinse
-
Ringer-Lösung oder physiologische Kochsalzlösung mit Infusionsbesteck in 500-ml-Spritzbeutel oder sterilem Glas
Je nach Anordnung werden Phosphatpuffer-Lösungen (z. B. Isogutt, Tim-oculav) oder bei Farb-, Teer- oder Schmaucheinsprengungen, z. B. Bepanthen-Augensalbe, gerichtet.
Durchführung
Der Patient wird über die geplante Maßnahme informiert und gebeten, eine sitzende oder liegende Position einzunehmen. Nach der Händedesinfektion wird die Spüllösung in ein sauberes Gefäß gefüllt (Glas oder Spritze). Alternativ können auch ein Spritzbeutel oder eine Infusionsflasche mit Infusionsbesteck zur Spülung verwendet werden. Bei starken Schmerzen und Lidspasmus (Blepharospasmus) ist die Spülung evtl. erst nach der Applikation lokalanästhesierender Augentropfen möglich.
Eine assistierende Pflegende hält die Lider auseinander, wenn der Arzt keinen Lidsperrer einsetzt. Das vorhandene Fremdkörpermaterial kann vorsichtig mit sterilen Tupfern entfernt werden. Die Spülung kann beginnen, wenn der Patient den Kopf zur Seite geneigt hat und die Auffangschale unter dem Kinn positioniert ist. Mit Kompressen wird danebenlaufende Flüssigkeit aufgefangen. Abschließend wird das gespülte Auge vorsichtig trocken getupft.
40.1.2.4 Augenverbände
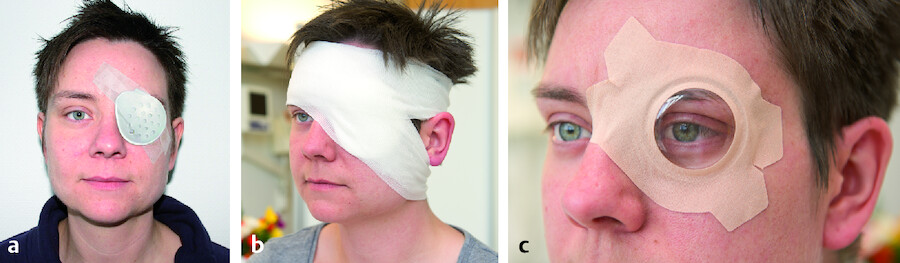
Das Anlegen von Augenverbänden dient der Fixierung von Wundauflagen und der Ruhigstellung der Augen. Die Verbandform ( ▶ Abb. 40.5) bedarf immer einer ärztlichen Anordnung.
Augenverbände.
Abb. 40.5 a Lochkapselverband, b Rollverband, c Uhrglasverband.
(Foto: W. Krüper, Thieme)
Material
Benötigt werden
-
hautfreundliches Pflaster,
-
Verbandschere,
-
sterile Augenkompressen und
-
je nach Verbandart 1 – 2 elastische Binden, Lochpolster, Lochkapsel oder Uhrglas.
Durchführung
Augenverbände gibt es als Lochkapselverband, geschlossenen Augenverband, Uhrglasverband, Druckverband oder Rollverband.
Lochkapselverband Beim Lochkapselverband wird eine sterilisierte, mit Löchern versehene und gewölbte Plastikkapsel auf ein sterilisiertes Lochpolster aufgelegt und mit einem hautfreundlichen Pflasterstreifen fixiert. Die Spitze der Kapsel liegt dabei oben nasal und die runde Seite unten temporal auf der Gesichtshaut auf. Der Patient mit funktioneller Einäugigkeit erhält eine durchsichtige, sterilisierte Lochkapsel.
Der Lochkapselverband schützt vor Infektionen und mechanischen Einwirkungen wie Zugluft und Stößen. Durch die Löcher ermöglicht er dem Patienten eine Orientierung im Raum. Ein Lochkapselverband wird z. B. nach einer Kataraktoperation angelegt.
Geschlossener Augenverband Der geschlossene Augenverband besteht aus einer undurchsichtigen und sterilen, ovalen Augenkompresse, die von oben nasal nach unten temporal schräg aufgelegt und mit hautschonenden Pflasterstreifen fixiert wird. Der Verband stellt das Auge ruhig und schützt vor Infektionen. Angelegt wird er z. B. nach Netzhautoperationen.
Beim Anlegen ist darauf zu achten, dass eine in der Augenkompresse vorhandene Naht nach außen gerichtet ist. Die Pflasterstreifen sollen so straff angelegt werden, dass einerseits die Lidspalte unter dem Verband geschlossen bleibt, andererseits aber Kaumuskelbewegungen und Mimik den Verband nicht ablösen.
Uhrglasverband Als Uhrglasverband wird ein durchsichtiges, uhrglasförmiges Plexiglas bezeichnet, das gebrauchsfertig von breiten Heftpflasterstreifen eingefasst ist. Das Pflaster dichtet das Auge nach außen ab. Die Innenseite des uhrglasförmigen Plexiglases beschlägt nach kurzer Zeit mit Wassertropfen, so entsteht eine feuchte Kammer.
Der Uhrglasverband schützt die Hornhaut vor dem Austrocknen. Er wird deshalb bei Patienten mit fehlendem oder unvollständigem Lidschluss verwendet (z. B. bei Patienten mit Beatmungstherapie, Fazialisparese mit unvollständigem oder unmöglichem Lidschluss = Lagophthalmus).
Druckverband Beim Druckverband wird zunächst eine zusammengefaltete sterile Augenkompresse und/oder ein Pflaumentupfer (je nach ärztlicher Anordnung) auf das geschlossene Auge aufgelegt und anschließend mit einem geschlossenen Verband fest auf der Haut fixiert. Der Druckverband wird z. B. angewandt, um Nachblutungen und Schwellungen der Lider nach einer ▶ Enukleation zu vermeiden.
Rollverband Der Rollverband stärkt den Druckverband durch das zirkuläre Anlegen einer elastischen kohäsiven Fixierbinde um den Kopf. Er wird i. d. R. nur am ersten postoperativen Tag nach einer ▶ Entfernung des Augapfels (Enukleation) angelegt. Der Rollverband verhindert ein Verrutschen des Druckverbandes. Durch die verstärkte Kompression wird die Gefahr einer Nachblutung reduziert.
Merke
Beim Druck- und Rollverband muss das abgedeckte Lid geschlossen bleiben.
Entfernung
Der Augenverband wird entfernt, indem das Pflaster langsam abgezogen wird. Um die empfindliche Gesichtshaut zu schützen, hält die Pflegende mit ihrer freien Hand die Haut am Pflasterrand unter leichter Gegenspannung.
40.2 Pflege von Patienten mit Sehbehinderungen oder Blindheit
40.2.1 Medizinischer Überblick
Fallbeispiel
Ich sitze auf der Parkbank und lausche mit geschlossenen Augen dem Vogelgezwitscher. Das gleichmäßige Brummen des Autoverkehrs ertönt im Hintergrund. Vor mir höre ich ein gleichmäßiges Scharren. Dann klackt es ein paar Mal und wieder ist das Scharren zu hören. Ich öffne die Augen. An mir geht ein etwa 30-jähriger Mann vorbei. Er bewegt einen langen weißen Stock auf dem Boden hin und her. Am Ende des Parkweges ertastet er vorsichtig die unterste Stufe einer kleinen Treppe und geht dann zügig hinauf. Oben bleibt er an einer Fußgängerampel stehen. Ich erinnere mich, dass diese Ampel langsam tickt, solange sie rot ist, und schneller, wenn sie grün ist.
40.2.1.1 Definition
Als blind im Sinne des Gesetzes gelten Personen,
-
bei denen angeboren oder erworben das Sehvermögen völlig fehlt oder
-
deren Sehschärfe entweder auf dem besseren Auge nicht mehr als 1/50 beträgt oder deren dauerhafte Störungen des Sehvermögens einer Herabsetzung der Sehschärfe auf 1/50 entsprechen (z. B. bei ausgeprägter Gesichtsfeldeinschränkung).
Eine Amaurose (vollständige Erblindung) liegt vor, wenn der Patient kein Licht mehr wahrnimmt und die Pupillen nicht mehr auf direkten Lichteinfall reagieren.
40.2.1.2 Ursachen
Die häufigste Ursache für Erblindungen im Sinne des Gesetzes ist die altersabhängige Makuladegeneration (AMD). Die AMD ist eine Erkrankung der zentralen Netzhaut, von der nur 1 – 3 % der 60-Jährigen, aber 30 – 40 % der 80-Jährigen zumindest in geringem Ausmaß betroffen sind. Weitere Ursachen sind z. B. das Glaukom und die ▶ Retinopathia diabetica.
Sehbehinderungen
Es gibt verschiedene Arten von Sehbehinderungen, z. B. Fehlsichtigkeit, Farbsinnstörungen, Nachtblindheit, Gesichtsfelddefekte, Doppelbilder und Augenzittern.
Fehlsichtigkeit Zu den verschiedenen Formen der Fehlsichtigkeit (Ametropie) gehören z. B.:
-
Myopie: Die Kurzsichtigkeit wird mit Minusgläsern in der Brille oder Kontaktlinsen ausgeglichen.
-
Hyperopie: Die Übersichtig- bzw. Weitsichtigkeit wird auch mit Kontaktlinsen oder einer Brille ausgeglichen. Diese enthält sog. Plusgläser.
-
Astigmatismus: Die Stabsichtigkeit („Hornhautverkrümmung“) wird mit Zylindergläsern in der Brille ausgeglichen.
Farbsinnstörungen Ist der Farbsinn normal, werden alle Farben des Farbraums, die sich aus den Primärfarben Rot, Grün und Blau zusammensetzen, richtig erkannt (Trichromasie). Abweichungen sind:
-
Anomale Trichromasie: Hierbei können farbschwache Menschen Rot und Grün nicht richtig unterscheiden.
-
Deuteranomalie: Etwa 5 % der männlichen Bevölkerung leiden an einer sog. Grünschwäche.
-
Dichromasie: Eine angeborene oder erworbene Rot-, Grün- oder Blaublindheit liegt vor, wenn die jeweilige Farbe überhaupt nicht gesehen werden kann.
-
Komplette Achromatopsie: Bei dieser angeborenen, selten auftretenden Störung werden nur Helligkeitsunterschiede wahrgenommen.
Nachtblindheit Eine Nachtblindheit (Nyktalopie) tritt als Folge einer Schädigung der Netzhautstäbchen auf (z. B. bei Retinitis pigmentosa). Die Stäbchen sind vorwiegend für das Sehen bei Dämmerung und Dunkelheit verantwortlich.
Gesichtsfelddefekte Gesichtsfelddefekte (Skotome) beeinträchtigen das Sehvermögen erheblich. Bei einem ▶ Zentralskotom , z. B. einer Sehnervenentzündung bei Multipler Sklerose, werden fixierte Objekte im Gesichtsfeldzentrum nur unscharf gesehen. Bei einer konzentrischen Einschränkung (sog. Röhrengesichtsfeld), wie sie z. B. bei Retinitis pigmentosa oder Glaukom im Endstadium auftreten kann, fällt das Gesichtsfeld in der Peripherie aus. Die Orientierung im Raum wird dadurch erheblich erschwert ( ▶ Abb. 40.6).
Gesichtsfeldeinschränkungen.
Abb. 40.6 a Beim Zentralskotom kann der Patient fixierte Objekte nicht mehr scharf sehen, sondern nur noch den Randbereich des Gesichtsfeldes wahrnehmen. Bei der peripheren Gesichtsfeldeinschränkung kann gegenüber der Sichtweise eines Normalsichtigen (b) nur noch der zentral fixierte Gegenstand wahrgenommen werden (c).
(Fotos: K. Oborny, Thieme)

Doppelbilder Doppelbilder (Diplopie) entstehen durch Lähmungen einzelner oder mehrerer Augenmuskeln. Sie stellen eine erhebliche Beeinträchtigung des Patienten dar. Häufig muss vorübergehend ein Auge abgeklebt werden.
Augenzittern Unter Augenzittern (Nystagmus) wird eine rhythmische Oszillation der Augen verstanden. Das Augenzittern kann physiologisch (optokinetischer Nystagmus), angeboren oder erworben (z. B. bei Hirnstammerkrankungen oder Sehverlust) sein.
40.2.2 Pflege- und Behandlungsplan
Während ein früh oder bereits lange erblindeter Mensch gelernt hat, seine anderen Sinne wie Gehör, Tast-, Geruchs- und Geschmackssinn vermehrt einzusetzen und sich in vertrauter oder fremder Umgebung rasch zurechtzufinden, ist der neu Betroffene sehr unsicher.
40.2.2.1 Zu Hilfsangeboten und Hilfsmitteln beraten
Die Pflegende berät den Sehbehinderten oder Blinden und dessen Angehörige z. B. zu Betroffenenverbänden wie dem DBSV und zu weiteren spezifischen Angeboten.
DBSV Beim Deutschen Blinden- und Sehbehindertenverband e. V. (www.dbsv.org) erhalten blinde Menschen Informationen, weitere Telefonnummern und Adressen. Anrufer werden beim Wählen einer zentralen Telefonnummer (01 805/666 456) automatisch mit dem zuständigen Landesverein ihrer Region verbunden.
Hilfsmittel Für Blinde gibt es eine ganze Reihe von praktischen Hilfsmitteln, z. B. ( ▶ Abb. 40.7):
-
Braille-Schrift, bei der Punktmuster-Codes für Buchstaben, Zahlen und Zeichen so in Papier gepresst sind, dass sie als Erhöhung mit den Fingerspitzen abgegriffen werden können
Hilfsmittel für blinde Menschen.
Abb. 40.7
Abb. 40.7a Taktiles Brettspiel
(Foto: slexp88/adobe.stock.com)

Abb. 40.7b Buch in Braille-Schrift
(Foto: Shawn Hempel/adobe.stock.com)

Abb. 40.7c weißer Langstock zur Orientierung
(Foto: New Africa/adobe.stock.com)

-
Lang- bzw. Blindenstöcke mit speziellem Blindenstocktraining
-
Wasserball oder Fußball mit Klingelball
-
Blindenhörbüchereien
-
spezielle Personalcomputer (PC) mit Spezialdrucker, die Texte einscannen und in Braille-Schrift umsetzen
40.2.2.2 Bei den ATL unterstützen
Der Patient und seine Angehörigen werden in den wichtigsten Räumen der Station und im Patientenzimmer herumgeführt. Falls die Nummer des Patientenzimmers nicht ertastet werden kann, wird zur Wiedererkennung ein Gegenstand angebracht, der ertastbar ist. Dem Patienten sollte die Möglichkeit gegeben werden, sich mit den Gegenständen des Zimmers und der Pflegestation bekannt zu machen. Die Rufanlage muss für den Sehbehinderten ohne Probleme erreich- und ertastbar sein.
Praxistipp
Beschreiben Sie Hindernisse oder Besonderheiten ganz konkret. Wählen Sie z. B. statt: „Im Zimmer steht auch ein Tisch“ eine genauere Aussage wie „Direkt rechts neben Ihnen steht ein Tisch mit einer Blumenvase in der Mitte“.
Beim Anziehen unterstützen Falls der blinde Patient mit seinen Kleidungsstücken nicht vertraut ist, kann die Pflegende Art und Farbe der Kleidung beschreiben. Sie assistiert ihm dann bei der Zusammenstellung und bei der Tagesfrisur.
Beim Essen unterstützen Die Pflegende beschreibt genau alle Speisen, die der Patient erhält. Wenn der Patient es wünscht, kann die Pflegende auch die Hand des Patienten an das Besteck und den Teller heranführen oder ihm das Essen mundgerecht portionieren (z. B. Fleisch in kleine Stücke schneiden). Für die Pflege von Sehbehinderten hat sich die Anschaffung bunter, schwerer Gläser bewährt, die besser zu erkennen sind und deshalb nicht so leicht umfallen. Sie sollten nur bis zur Hälfte gefüllt werden.
Praxistipp
Beschreiben Sie die Speisen im Uhrzeigersinn: „Bei 3 Uhr finden Sie das Gemüse, die Kartoffeln bei 7 Uhr und bei 11 Uhr das Fleisch. Die Salatschale mit dem Gurkensalat steht auf dem Tablett links oben, das Dessertschälchen mit dem Vanillepudding rechts oben.“
Beim Bewegen unterstützen Der Patient erhält jeweils eine aktuelle Beschreibung des geplanten Weges und wird über vorkommende Hindernisse informiert. Die Pflegende unterstützt den Sehbehinderten, indem sie ihn führt. Dazu hakt er sich bei der Pflegenden ein. Wenn ein Mensch erst kurze Zeit blind ist, wird er besondere Schwierigkeiten haben Treppen zu steigen. Ein bereits längere Zeit Erblindeter benötigt meist nur Hilfe bei der ersten Stufe und kann den Rest selbstständig bewältigen.
Praxistipp
Möchte sich der Patient setzen, führen Sie seine Hand an die Stuhllehne heran, sodass er sich die Sitzfläche selbst ertasten kann.
40.3 Pflege von Patienten mit Enukleation und Augenprothese
40.3.1 Medizinischer Überblick
40.3.1.1 Definition
Eine Enukleation (lat. enucleare = entkernen) ist die operative Entfernung eines Körperteiles aus einer Kapsel, z. B. die Entfernung des Augapfels aus den umgebenden Geweben.
Augenprothesen sind Schalen aus Glas oder Kunststoff. Sie werden anstelle des Augapfels als Platzhalter und/oder aus kosmetischen Gründen in die vordere Orbita zwischen Augenlidern und Bindehautauskleidung der Enukleationshöhle eingesetzt.
40.3.1.2 Ursachen
Eine Enukleation und die anschließende Versorgung mit einer Augenprothese wird am häufigsten durchgeführt bei
-
bestimmten Augentumoren,
-
schwersten Augenverletzungen und
-
nichttherapierbarem schmerzhaft geschrumpftem Auge (Phthisis bulbi).
40.3.1.3 Verlauf
Am 5. postoperativen Tag, nachdem die Schwellung rückläufig ist, wird dem Patienten meist eine vorläufige Augenprothese angepasst. Diese vorläufige Glasprothese wird einem Glasprothesensatz entnommen und entspricht in Form und Farbe annähernd dem anderen Auge. Der Patient wird dann mit der vorläufigen Augenprothese entlassen. Später wird eine individuell angefertigte Augenprothese aus Glas von einem Augenkünstler angefertigt. Sie ist dem anderen Auge so ähnlich, dass ein ungeübter Beobachter das sog. „Glasauge“ oft gar nicht registriert. Die Glasprothese muss etwa alle ein bis zwei Jahre ausgetauscht werden, da die Tränenflüssigkeit die Oberfläche mit der Zeit aufraut.
40.3.2 Pflege- und Behandlungsplan
40.3.2.1 Postoperative Nachsorge
Im Operationssaal wird dem Patienten eine Lochprothese oder ein Keramikbrikett in die Enukleationshöhle eingesetzt, bevor die OP-Wunde mit einem Druckverband versorgt wird. Pflegende übernehmen die Wundversorgung und die Anleitung zur Handhabung der Augenprothese.
Wundversorgung
Die Lochprothese bzw. das Keramikbrikett bleiben zunächst als Platzhalter in der Enukleationshöhle. Der Platzhalter wird während der ersten postoperativen Tage einmal täglich bei der ärztlichen Visite herausgenommen und gereinigt. Nach der Inspektion der Wundhöhle und vor dem Wiedereinsetzen der Augenprothese wird nach ärztlicher Anordnung eine antibiotische Augensalbe appliziert. Danach wird erneut ein ▶ Druck- oder Rollverband angelegt. Nachdem die Schwellung rückläufig ist, wird dem Patienten eine vorläufige Augenprothese angepasst.
40.3.2.2 Zur Handhabung einer Augenprothese anleiten
Die Einweisung in die Handhabung der Augenprothese erfordert von der Pflegenden Einfühlungsvermögen, Geduld und eine ruhige Ausstrahlung. Sie sollte dafür bewusst einen längeren Zeitraum im Stationsablauf einplanen. Der Patient wird informiert, dass die Augenprothese auch nach dem stationären Aufenthalt einmal täglich herausgenommen und gereinigt werden soll.
Merke
Patient und Angehörige sollten bereits vor der Operation mit der Prothese vertraut gemacht werden und sie anfassen können.
Material
Um die Augenprothese herausnehmen bzw. wieder einsetzen zu können ( ▶ Abb. 40.8), werden folgende Materialien auf einem Pflegetablett gerichtet:
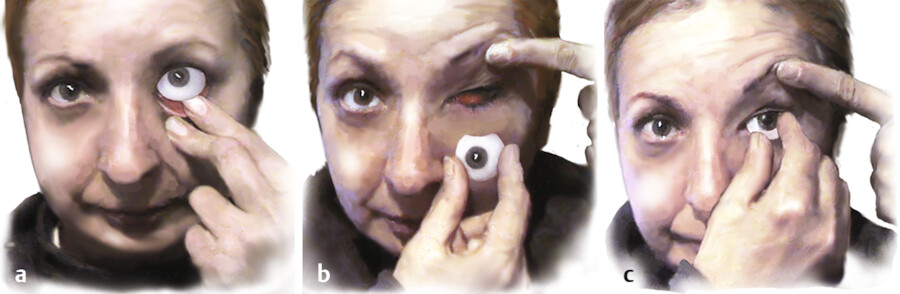
Umgang mit einer Augenprothese.
Abb. 40.8 a Zum Herausnehmen mit dem Zeigefinger das Unterlid unter den Prothesenrand drücken und die Prothese lockern, b zum Einsetzen der Prothese Oberlid anheben und c unter das angehobene Oberlid schieben.
(Grafik: V. Constantinescu, Thieme)
-
Nierenschale aus Zellstoff bzw. Prothesenbehälter
-
Schutzhandschuhe
-
weiche, saubere Unterlage (z. B. ein Handtuch)
-
Zellstofftupfer bzw. Kompressen
-
physiologische Kochsalzlösung
-
Behälter mit lauwarmem Wasser
-
10-ml-Spritze mit Aufziehkanüle
-
ärztlich angeordnete Augenmedikamente
-
aufstellbarer Tischspiegel, evtl. Glasstäbchen
Durchführung
Zunächst wird der Patient über den Zweck und Ablauf der pflegerischen Maßnahme informiert. Besucher werden gebeten, das Zimmer zu verlassen, der Patient vor den Blicken der Mitpatienten geschützt. Die Pflegende breitet zunächst die weiche Unterlage vor dem Patienten aus, damit die Glasprothese nicht zerspringen kann, wenn sie aus der Hand gleiten sollte. Dann wird der Spiegel aufgestellt. Anschließend erfolgt die gründliche ▶ Händedesinfektion.
Augenprothese herausnehmen Zum Herausnehmen der Augenprothese drückt der Patient mit dem Zeigefinger oder einem Glasstäbchen das Unterlid unter den Prothesenrand. Dadurch wird die Augenprothese gelockert und kann entweder in die bereitgehaltene Hand fallen oder zwischen Zeigefinger und Mittelfinger gehalten werden. Der Blick nach oben erleichtert den Vorgang für die Pflegende. Die herausgenommene Prothese wird mit lauwarmem Wasser gereinigt und im Aufbewahrungsbehälter oder auf einer Kompresse platziert.
Praxistipp
Verkrustungen an der Augenprothese lösen sich, wenn sie ca. 10 Min. in physiologische Kochsalzlösung gelegt wird.
Die Augenhöhle wird inspiziert. Bei Sekretbildung oder Verkrustungen wird sie, je nach Anordnung des Arztes, z. B. mit physiologischer Kochsalzlösung gespült. Fühlt sich die Oberfläche der Augenprothese rau an, besteht die Möglichkeit, dass die Prothese die Augenhöhle reizt, sie sollte deshalb ausgetauscht werden.
Augenprothese einsetzen Um das Einsetzen der Augenprothese zu erleichtern, wird sie kurz mit physiologischer Kochsalzlösung befeuchtet und dann mit einer Hand an der breitesten Stelle zwischen Daumen und Zeigefinger gefasst. Die Prothese wird dabei so ausgerichtet, dass ihre Ausbuchtung zur Nase zeigt und der breite Teil zur Schläfe. Die andere Hand zieht das Oberlid ab. Während der Patient nach unten sieht, wird die Prothese vorsichtig unter das Oberlid geschoben. Anschließend blickt er bei leichter Abhebung des Unterlides nach oben, sodass die Augenprothese auch in den unteren Bindehautsack gleiten kann.
Praxistipp
Das Herausnehmen und Wiedereinsetzen der Augenprothese muss mehrmals geübt werden. Bestehen beim Patienten Unsicherheiten in der Handhabung, sollten möglichst auch Angehörige oder Betreuungspersonen angeleitet werden, die nach der Entlassung die Pflege der Augenprothese übernehmen könnten.
40.4 Pflege von Patienten mit Augenoperationen
40.4.1 Medizinischer Überblick
40.4.1.1 Definition
Augenoperationen sind chirurgische Eingriffe im Bereich der Augen und ihrer Anhangsgebilde. Sie werden in Lokal- oder Allgemeinanästhesie durchgeführt. Beispiele sind:
-
Wundversorgung nach Verletzungen im Lidbereich
-
Anhebung eines über die Pupille herabhängenden Oberlids (Ptosisoperation)
-
Schieloperation (operative Verstärkung oder Abschwächung der Wirkung der Augenmuskeln)
-
Eingriffe am Augapfel, meist unter dem Mikroskop mit mikrochirurgischem Instrumentarium und Speziallasern
40.4.2 Medizinischer Überblick Kataraktoperation
Fallbeispiel
„Ach, liebe Ella, es ist so richtig gemütlich bei dir und ich würde gern noch bleiben, aber es dämmert schon und ich möchte vor Einbruch der Dunkelheit zu Hause sein.“ Mit sichtlichem Bedauern steht Frau Wiesmöller von ihrem Stuhl auf. „Aber warum denn? Du hast dir doch gerade ein neues Auto mit allen Schikanen zu deinem 60. Geburtstag gekauft, damit müsstest du problemlos auch nachts fahren können“, gibt ihre Freundin etwas enttäuscht zu bedenken „ Ja sicher, aber nachts bin ich so furchtbar leicht geblendet – und denk nur, letzte Woche hätte ich dadurch fast einen Fahrradfahrer übersehen!“ „Aber dann solltest du dringend mal zu einem Augenarzt. Irina, weißt du, mit der ich immer Nordic-Walking mache, ist gerade am Auge operiert worden und kann wieder ganz prima sehen!“
40.4.2.1 Definition
Die Katarakt (grauer Star oder Cataracta) ist eine Trübung der Augenlinse. Sie kann angeboren oder erworben sein und in jedem Lebensalter auftreten.
40.4.2.2 Ursachen
Die Ursachen unterscheiden sich nach Art der Katarakt.
Angeborene Katarakt Die seltenen Neugeborenenkatarakte werden oft vererbt oder durch eine intrauterine Infektion der Mutter (z. B. mit Röteln) hervorgerufen.
Erworbene Katarakt Zahlenmäßig mit Abstand am häufigsten tritt die Katarakt bei älteren Menschen als sog. senile Katarakt auf. Weitere Ursachen der Linsentrübung können sein:
-
Stoffwechselerkrankungen, z. B. ▶ Diabetes mellitus
-
Hautkrankheiten, z. B. ▶ Neurodermitis
-
Einnahme bestimmter Medikamente, z. B. Kortikosteroide
-
Unfälle, z. B. Kontusionskatarakt
40.4.2.3 Symptome
Die vollständig durchgetrübte Augenlinse führt zum Eindruck einer weißen Pupille (Leukokorie). In Industrienationen wird dies heute nur noch sehr selten beobachtet, häufiger sind nur Teile des Linsenkerns oder der Rinde getrübt. Zentrale Trübungen führen zu einer Sehherabsetzung und einer erhöhten Blendempfindlichkeit, besonders nachts während des Autofahrens und bei Regen. Das Farbensehen und die Kontrastwahrnehmung sind ebenfalls reduziert. Manchmal sieht der Patient doppelt.
40.4.2.4 Therapie
Die Behandlung einer Katarakt geschieht ausschließlich operativ. Die Operation erfolgt meist dann, wenn der Patient durch die Herabsetzung der Sehschärfe und die zunehmende Blendung bei den ▶ Aktivitäten des täglichen Lebens deutlich eingeschränkt ist.
Phakoemulsifikation Die zurzeit am häufigsten gewählte Operationsmethode ist eine Phakoemulsifikation mit Kunstlinsenimplantation: Nach dem Anlegen eines Skleratunnels oder einem Hornhautschnitt wird unter einem speziellen Mikroskop die vordere Linsenkapsel zirkulär eröffnet und entfernt (Kapsulotomie). Danach wird die Linse mit Ultraschall zerkleinert (Phakoemulsifikation) und die Linsenfragmente werden abgesaugt. In den verbliebenen Kapselsack wird eine Kunstlinse implantiert ( ▶ Abb. 40.9).
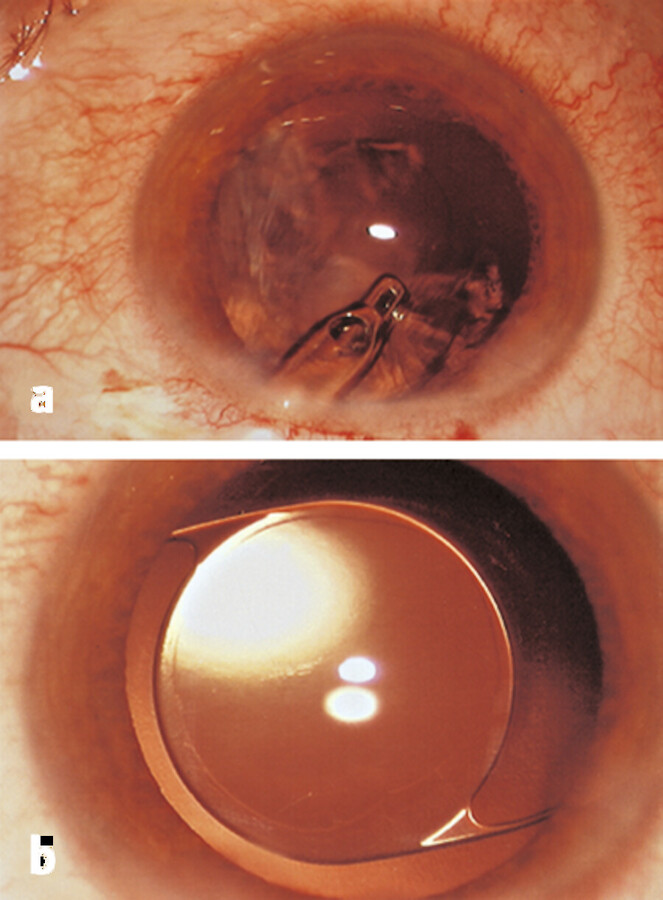
Kataraktoperation.
Abb. 40.9 a Bei der Phakoemulsifikation wird der Linsenkern zerkleinert. b Sind alle Linsenreste entfernt, wird die Kunstlinse hinter die Iris implantiert.
Merke
Ein Patient ist pseudophak, wenn die natürliche Linse durch eine Kunstlinse ersetzt worden ist, und aphak, wenn operativ nur die natürliche Linse entfernt wurde.
40.4.2.5 Komplikationen
Bei den heutigen Operationsverfahren treten sehr selten Komplikationen auf. Verschiedene Komplikationen sind z.B.:
Wundfistel Sie wird, je nach Situation, mit einer Verbandskontaktlinse, einem geschlossenen Verband mit doppelter Kompresse oder einer Wundrevision behandelt.
Postoperative Augeninnendruckerhöhung Sie kann von Schmerzen begleitet sein und erfordert entweder eine medikamentöse Augeninnendrucksenkung oder eine chirurgische Druckablassung.
Endophthalmitis Klagt ein Patient nach einer Kataraktoperation über Schmerzen oder eine Sehverschlechterung, muss umgehend ein Augenarzt informiert werden. Es kann sich eine Entzündung des gesamten Augeninneren entwickeln, die schlimmstenfalls zum Verlust des Auges führt.
40.4.3 Pflege- und Behandlungsplan
Augenärzte, die sich auf Augenoperationen spezialisiert haben, sind Mikrochirurgen. Unter dem Mikroskop ersetzen sie die getrübte Linse mit feinsten Instrumenten durch eine künstliche (s. ▶ Abb. 40.9). Der Patient kann seine Umgebung anschließend wieder scharf erkennen.
Im Rahmen einer Augenoperation haben Pflegende die Aufgabe der Operationsvorbereitung und postoperativen Versorgung.
40.4.3.1 Operationsvorbereitung
Bereits im Aufnahmegespräch erfolgt die Klärung der poststationären Nachsorge, denn nach jeder Kataraktoperation werden über den stationären Aufenthalt hinaus Augentropfen mehrmals täglich verordnet. Da die Patienten entweder ambulant operiert oder sehr schnell entlassen werden, muss sichergestellt sein, dass sie die augenärztlichen Kontrollen wahrnehmen können. Ist der Patient dazu selbst nicht in der Lage, müssen Angehörige oder Pflegedienste eingeschaltet werden.
Organisatorische Maßnahmen
Der Patient muss am Operationstag nüchtern sein. Neben dem Einweisungsschein und einer Kopie des letzten ▶ EKGs muss er eine Bescheinigung des Hausarztes mitbringen, die seine Operationsfähigkeit bestätigt.
Gerinnungsparameter Falls in Parabulbäranästhesie (das Lokalanästhetikum wird neben den Augapfel gespritzt) operiert wird, müssen in Absprache mit dem Hausarzt bereits 10 Tage vor dem geplanten Operationstermin Thrombozytenaggregationshemmer (z. B. Aspirin) abgesetzt werden. Eine Marcumartherapie (Phenprocoumon) wird nur weitergeführt, wenn die Kataraktoperation in Vollnarkose oder in Tropfanästhesie stattfinden soll. Im Falle einer Parabulbäranästhesie ist die Blutungsgefahr zu hoch, deshalb wird der Patient rechtzeitig auf Heparin umgestellt. Die Gerinnungsparameter müssen sich in einem Bereich befinden, der eine gefahrlose Operation zulässt. So sollte der ▶ Quickwert z. B. 50 % sein.
Pflegerische Maßnahmen
Die allgemeinen Maßnahmen zur Operationsvorbereitung können im Kapitel ▶ „Präoperative Phase“ nachgelesen werden. Neben Ringen, Ketten und Zahnprothesen entfernt der Patient auch Kontaktlinsen und vorhandene Augenprothesen. Besitzt der Patient Hörgeräte, sollte das, welches sich auf der zu operierenden Seite befindet, herausgenommen werden.
Prämedikation Vor der Verabreichung der Prämedikation erhält der Patient die Möglichkeit, Blase und Darm zu entleeren. Er wird darüber informiert, dass er nach der Einnahme der Prämedikation nicht mehr aufstehen sollte. Prämedikation und möglicherweise Herz- und Kreislaufmedikamente werden nach Anordnung auf dem Narkoseprotokoll verabreicht.
Pupillenerweiternde Augentropfen Anschließend werden ärztlich angeordnete pupillenerweiternde Augentropfen am zu operierenden Auge appliziert. Die Wiederholung erfolgt 1/4-stdl. bis zum Abruf in den Operationssaal.
Merke
Eine weite Pupille erleichtert die Kataraktoperation erheblich.
Weitere Maßnahmen Erhält das nicht zu operierende Auge eine lokale Augentherapie, wird diese am Operationstag nicht unterbrochen, sondern nach dem Behandlungsplan fortgesetzt. Weitere pflegerische Maßnahmen sind:
Erfolgt der Abruf in den Operationsbereich, vergewissert sich die verantwortliche Pflegende noch einmal, dass das richtige Auge weitgetropft wurde und alle Unterlagen einschließlich der Patientenakte und der OP-Einwilligung korrekt gerichtet sind.
40.4.3.2 Postoperative Pflege
Die allgemeinen postoperativen pflegerischen Maßnahmen können im Kapitel ▶ „Postoperative Phase“ nachgelesen werden.
Pflegerische Überwachung
Nach der Übernahme des Patienten aus dem OP kontrolliert die Pflegende in regelmäßigen Abständen folgende Parameter:
-
Bewusstsein
-
Vitalzeichen einschließlich Puls und Blutdruck
-
Blutzucker bei Diabetikern
-
Verband am operierten Auge
Positionierung/Lagerung Der Patient wird entsprechend seinen Wünschen bequem bzw. nach der Vorgabe des Operateurs positioniert. Nach glaskörperchirurgischen Eingriffen ordnet der Operateur in manchen Fällen eine Bauchlage an. Das Patientenzimmer wird etwas abgedunkelt, um den Patienten nicht dem hellen Licht auszusetzen. Die Klingel muss gut erreichbar sein, der Operierte sollte nicht durch Mitpatienten oder deren Besucher gestört werden.
Nahrungsaufnahme und Mobilisation Etwaige Infusionstherapie, Flüssigkeits- und Nahrungsaufnahme und Mobilisation richten sich nach dem Narkoseprotokoll.
Nachbehandlung Der kataraktoperierte Patient erhält für mehrere Tage eine Antibiotikum-Kortikosteroid-Kombination verabreicht. Tagsüber werden Augentropfen und zur Nacht Augensalbe instilliert. Der Patient wird informiert, dass er nach Augenoperationen keinesfalls die Augen reiben darf (das gilt auch für augenärztliche Untersuchungen mit Lokalanästhetikum).
40.5 Pflege von Patienten mit Tonsillitis
Anatomie und Physiologie im Fokus
(nach Schwegler u. Lucius 2016)
Hals-Nasen-Ohrenbereich im Überblick
Hals
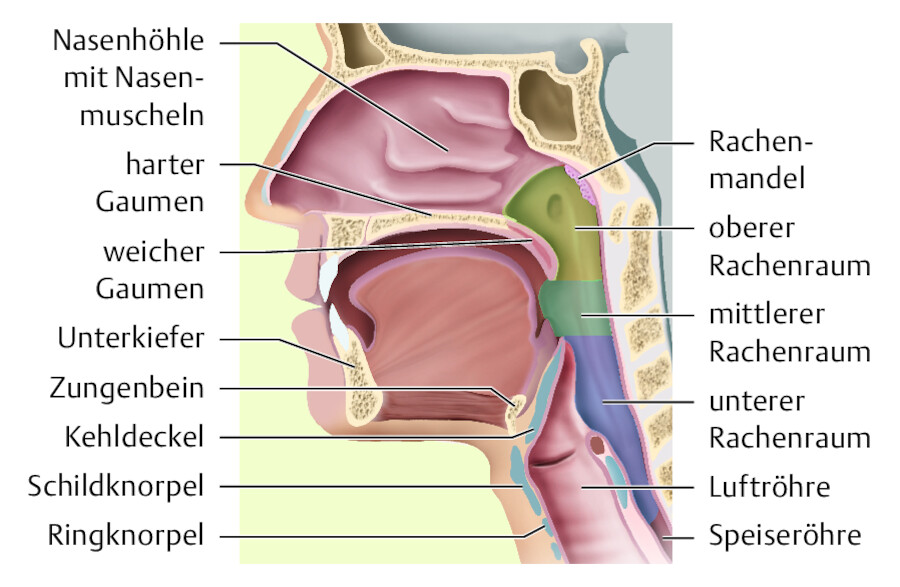
Der Rachen besteht aus dem oberen Rachenraum mit der Rachenmandel, dem mittleren Rachenraum hinter der Mundhöhle mit Zäpfchen, weichem Gaumen und Gaumenmandel mit dem an den Kehlkopfdeckel grenzenden Zungengrund sowie dem unteren Rachenraum ( ▶ Abb. 40.10). Der Kehlkopf bildet einen Verschlussmechanismus zwischen Luftröhre und unterem Rachenraum und verhindert während des Schluckaktes, dass Nahrung in die unteren Luftwege gelangt. Damit die Luftwege auch bei starken Druckschwankungen im Halsraum stets geöffnet bleiben, benötigt der Kehlkopf ein Skelett – die Kehlkopfknorpel ( ▶ Abb. 40.11).
Der Rachenraum schließt sich an die Nasenhöhle an.
Abb. 40.10
Nase
Die Nase besteht aus 2 durch die Nasenscheidewand (Nasenseptum) getrennte Nasenhöhlen. Seitlich vergrößern Nasenmuscheln die Schleimhautoberfläche, die zur Reinigung der Atemluft aus Flimmerepithel besteht. Auch die lufthaltigen Nasennebenhöhlen sind mit Schleimhaut ausgekleidet und stehen mit den Nasenhöhlen in Verbindung. Gerüche werden am Dach der Nasenhöhle wahrgenommen. Dort sind an die 10 Millionen Nervenzellen im Epithel, die über einen dicken Zellausläufer direkten Kontakt mit der Schleimschicht aufnehmen. Die Riechschleimhaut leitet die Information direkt durch die Schädelbasis zum ersten Hirnnerven weiter.
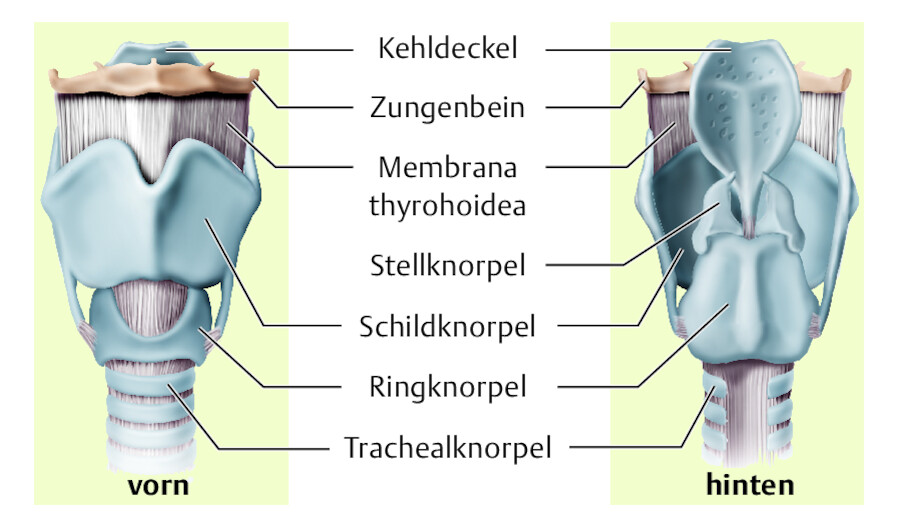
Die Kehlkopfknorpel bestehen aus Schildknorpel, Kehldeckelknorpel, Ringknorpel und 2 Stellknorpeln.
Abb. 40.11
Ohr
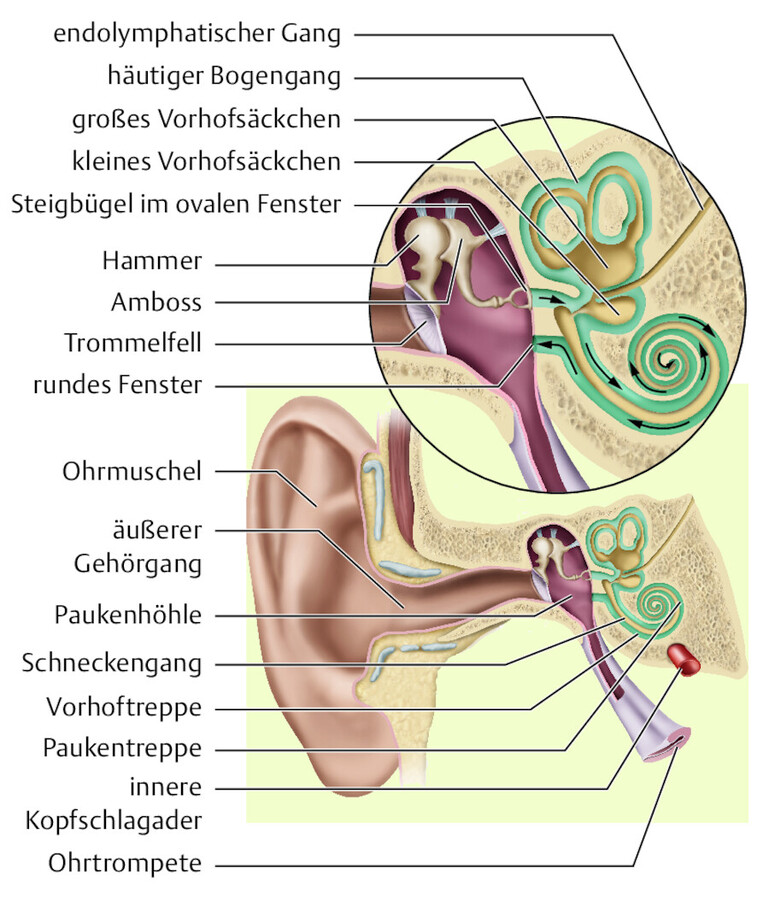
Der äußere Gehörgang verläuft schräg von hinten oben nach vorne unten und ist außerdem noch in sich gekrümmt. Seine innere Begrenzung, das Trommelfell, ist nur ca. 0,7 mm dick. Jenseits des Trommelfells liegt die Paukenhöhle (Mittelohr). Sie besitzt über die Ohrtrompete Anschluss an den Rachenraum. Die drei winzigen Gehörknöchelchen Hammer (Malleus), Amboss (Incus) und Steigbügel (Stapes) verbinden das Trommelfell gelenkig mit dem ovalen Fenster, dem Abschluss der Paukenhöhle zum Innenohr ( ▶ Abb. 40.12). Die Ohrmuschel verstärkt den einfallenden Schall. Zum Hören wird die Schallenergie auf einen kleinen Bereich am Steigbügel konzentriert und gelangt von dort ins Innenohr.
Ohr.
Abb. 40.12 Ohrmuschel, äußerer Gehörgang und Trommelfell bilden ein akustisches Verstärkungssystem. Die Schallenergie wird auf den Steigbügel konzentriert und gelangt von dort ins Innenohr.
40.5.1 Medizinischer Überblick akute Tonsillitis
40.5.1.1 Definition
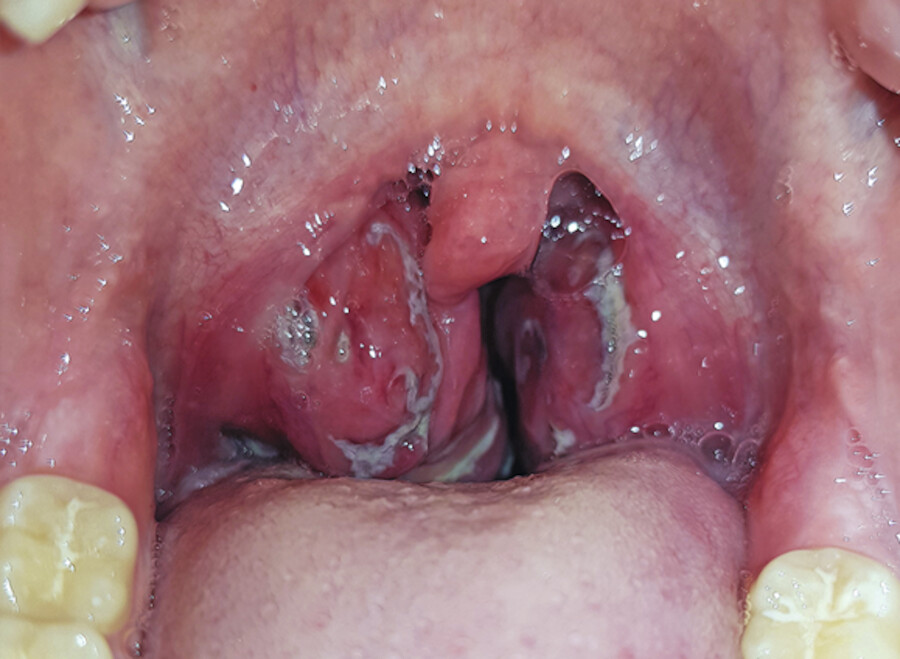
Die akute Tonsillitis ist eine Entzündung der Gaumenmandeln ( ▶ Abb. 40.13).
Akute Tonsillitis.
Abb. 40.13 Mit Eiterstippchen besetzte entzündete Gaumenmandeln.
(Foto: K. Oborny, Thieme)
Häufigkeit Die Tonsillitis kann Menschen jeden Lebensalters betreffen, tritt aber am häufigsten bei Kindern und Jugendlichen auf. Pro Jahr erkranken > 50 000 Menschen an einer akuten Tonsillitis.
40.5.1.2 Ursachen
Sie wird am häufigsten durch Streptokokken verursacht. Seltenere bakterielle Erreger der akuten Tonsillitis sind Pneumokokken, Staphylokokken oder Haemophilus influenzae. Die Mononukleose ist eine durch Viren (EBV-Viren) ausgelöste Tonsillitis.
40.5.1.3 Symptome
Die Anzeichen einer akuten Tonsillitis sind:
-
akute Halsschmerzen, besonders beim Schlucken
-
in die Ohren ausstrahlende Schmerzen
-
kloßige Sprache
-
vermehrter Speichelfluss
-
allgemeines Krankheitsgefühl
-
evtl. Fieber
40.5.1.4 Diagnostik
Bei der Untersuchung der Mundhöhle sieht der Arzt kleine weißliche Stippchen auf der Schleimhaut der Gaumenmandeln. Die Halslymphknoten sind druckschmerzhaft geschwollen. Zusätzlich sollten die Bestimmung des Differenzialblutbildes und eine Abstrichuntersuchung zur Bestimmung des Erregers erfolgen.
40.5.1.5 Komplikationen
Als Folgeerkrankung einer Streptokokkeninfektion der Tonsillen können auftreten:
-
Endo-, Myo- oder Perikarditis (Entzündung von Herzinnenhaut, Herzmuskel oder Herzbeutel)
-
rheumatisches Fieber
40.5.1.6 Therapie
Die akute Tonsillitis wird für mindestens 4 Tage mit einem Antibiotikum (Penicillin oral 3 × 1 Mio. I.E.) behandelt, um Folgeerkrankungen zu vermeiden. Zusätzlich kann gegen die Schluckbeschwerden Diclofenac gegeben werden.
40.5.2 Medizinischer Überblick chronische Tonsillitis
40.5.2.1 Definition
Als chronische Tonsillitis wird die ständig wiederkehrende bakterielle Entzündung der Gaumenmandeln bezeichnet.
40.5.2.2 Ursachen und Symptome
Die Erkrankung wird durch Streptokokken hervorgerufen. Anzeichen einer chronischen Tonsillitis sind:
-
immer wiederkehrende Halsschmerzen und Mandelentzündungen
-
häufige Infekte
-
allgemeines Krankheitsgefühl
40.5.2.3 Diagnostik
Bei der Untersuchung der Mundhöhle werden häufig kleine, vernarbte und schwer luxierbare oder hyperplastisch vergrößerte Tonsillen sichtbar. Der Antistreptolysin-Titer ist häufig erhöht.
40.5.2.4 Komplikationen
Die chronische Tonsillitis wird als Herd (Fokus) für unterschiedliche Erkrankungen gesehen, z. B.:
-
rheumatisches Fieber
-
Glomerulonephritis
-
entzündliche Herz- und Gefäßerkrankungen
-
Augenkrankheiten
-
Urtikaria
40.5.2.5 Therapie
Um einen evtl. Entzündungsherd im Körper zu beseitigen, sollte bei Verdacht auf chronische Tonsillitis eine Tonsillektomie (Mandelentfernung s. auch Tonsillektomie, ▶ Abb. 40.14) durchgeführt werden. Sie ist heute immer noch einer der am häufigsten durchgeführten chirurgischen Eingriffe.
Tonsillektomie.
Abb. 40.14 Die Gaumenmandeln werden aus ihrem Bett zwischen den Gaumenbögen scharf herausgeschält.

Durchführung In Vollnarkose oder örtlicher Betäubung werden die Gaumenmandeln mit einer Fasszange gefasst und mit einer Schere sowie einem stumpfen Instrument (Raspatorium) aus ihrer Umgebung herausgelöst. Zum Abtragen des unteren, an die Zunge angrenzenden Tonsillenpoles wird eine Schlinge verwendet. Anschließend erfolgt eine sorgfältige Blutstillung mit einer bipolaren Elektropinzette. Spritzende Blutungen sollten unterbunden oder umstochen werden.
Am Ende des Eingriffs zeigen sich zwischen vorderem und hinterem Gaumenbogen im Durchmesser ca. 2 cm große Wundflächen, die sich in den folgenden Tagen mit einem weißlichen Wundschorf (Fibrinbelag) bedecken. Dieser Wundbelag stößt sich zwischen dem 4. und 6. Tag ab, allmählich setzt die narbige Abheilung ein.
Komplikationen Da nach der Tonsillektomie die Wundflächen offen bleiben und nicht vernäht werden, kann es leicht zu postoperativen Nachblutungen kommen.
40.5.3 Pflege- und Behandlungsplan
Eine Gaumenmandelentfernung erfolgt in Deutschland immer stationär.
Da der Patient häufig erst am Operationstag zur stationären Aufnahme erscheint, stellen die Pflegenden nur die postoperative Versorgung sicher.
40.5.3.1 Postoperative Versorgung
Die Pflegende achtet in den ersten Stunden nach der Operation besonders auf Anzeichen einer Nachblutung. Ganz besonders wichtig ist diese Aufgabe bei einem noch nicht vollständig aus der Narkose erwachten Patienten. In dieser Situation kann es zur Aspiration von Blut und Blutkoageln kommen und damit zur ▶ akuten Atemnot. Der Patient wird deshalb mit erhöhtem Oberkörper gelagert.
Nachblutungsgefahr Der operierte Patient wird aufgefordert, die sich im Mund sammelnde Flüssigkeit in eine bereitgestellte Nierenschale zu spucken, um eine Blutung frühzeitig erkennen zu können. Verschluckt ein Patient über längere Zeit unbemerkt Blut, so wird ihm bald übel und er erbricht schwarz gefärbtes Blut. Bei jedem Zeichen einer Nachblutung ist der Arzt zu verständigen, der dann eine Blutstillung vornehmen muss.
Bei stärkeren Blutungen kann es notwendig werden, in einer erneuten Narkose das blutende Gefäß zu unterbinden oder zu umstechen.
Praxistipp
Häufig genügt es, eine kühlende Eiskrawatte in den Nacken zu legen und den Patienten mit Eiswasser den Mund ausspülen zu lassen.
Merke
Nach 24 Std. sinkt die Gefahr der Nachblutung. Vom 4.– 6. Tag steigt die Wahrscheinlichkeit von Nachblutungen wieder, wenn sich die Wundbeläge ablösen.
Nach der Tonsillektomie ist ein Aufenthalt von ca. 5 Tagen im Krankenhaus empfohlen. Als weitere Verhaltensmaßregeln sollte der Patient nicht zu heiß duschen und starke körperliche Anstrengung vermeiden.
Wundbehandlung Der Wundschmerz steht neben der Nachblutung in der postoperativen Phase im Vordergrund. In aller Regel ist der Wundschmerz bei Erwachsenen deutlich stärker als bei Kindern. Er bleibt über 10 Tage konstant hoch und verstärkt sich am Ende, wenn sich die Wundbeläge abstoßen. Gegen die Wundschmerzen kann nach ärztlicher Anordnung z. B. Diclofenac als Zäpfchen regelmäßig verabreicht werden.
Merke
Eine ständige Kühlung des Halsbereiches mit Kühlelementen oder einer ▶ Eiskrawatte trägt zur Schmerzlinderung bei und reduziert die Schmerzmittelgabe.
Ernährung Die Nahrungsaufnahme ist ebenfalls schmerzhaft. Deswegen sollten die Schmerzmittel 30 Min. vor der Mahlzeit verabreicht werden. Scharfe Gewürze, heiße Speisen und säurehaltige Säfte sollten gemieden werden, da sie erfahrungsgemäß Schmerzen auslösen können. Nach dem Krankenhausaufenthalt wird dem Patienten insgesamt für 14 Tage körperliche Ruhe empfohlen, da auch nach dem 7. Tag noch Nachblutungen auftreten können. Dies ist allerdings eher selten.
40.6 Pflege von Patienten mit Larynxkarzinom
40.6.1 Medizinischer Überblick
40.6.1.1 Definition
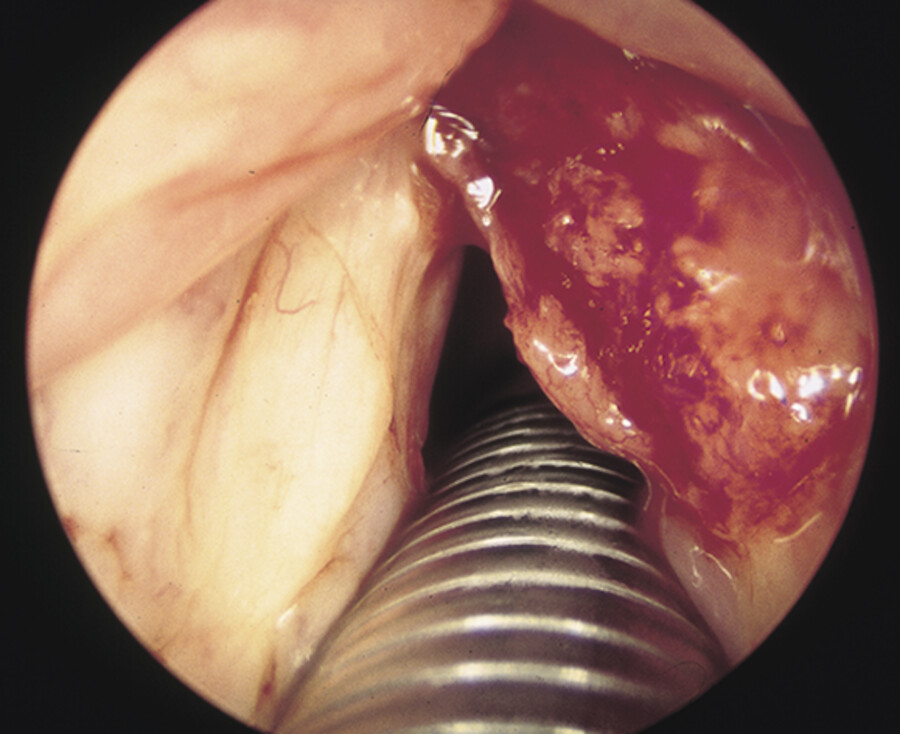
Ein Larynxkarzinom ist eine bösartige Geschwulst im Kehlkopf ( ▶ Abb. 40.15). Histologisch betrachtet sind ca. 95 % der Kehlkopftumoren Plattenepithelkarzinome.
Ansicht eines Larynxkarzinoms.
Abb. 40.15 Der Tumor hat die rechte Stimmlippe befallen.
Häufigkeit Bei etwa 40 – 50 % aller bösartigen Tumoren in der HNO-Heilkunde handelt es sich um ein Larynxkarzinom. Männer sind ungefähr 9-mal häufiger betroffen als Frauen. Der Altersgipfel liegt zwischen dem 4. und 7. Lebensjahrzehnt.
Lokalisation Rund 2/3 der Larynxkarzinome haben ihren Ursprung in der Stimmritze (Glottiskarzinome), ein weiteres Drittel bildet sich im oberhalb der Stimmritze liegenden Teil des Larynx (supraglottische Larynxkarzinome). Nur selten finden sich Larynxkarzinome unterhalb der Stimmritze (subglottische Karzinome).
Risikofaktoren Als Risikofaktoren sind hauptsächlich ein hoher Zigaretten- und Alkoholkonsum bekannt.
40.6.1.2 Symptome
Die Symptome bei Larynxkarzinomen hängen vom Sitz der Tumoren ab. Patienten mit glottischen Larynxkarzinomen entwickeln anfangs Heiserkeit. Wenn der Tumor die Glottis verlegt, entsteht eine Atemnot mit inspiratorischem Stridor. Patienten mit supraglottischen Larynxkarzinomen haben meist Schluckbeschwerden und eine kloßige Sprache. Erst später tritt eine Heiserkeit auf. Auch Ohrenschmerzen oder blutiger Auswurf können Symptome eines Larynxkarzinoms sein.
40.6.1.3 Diagnostik
Zur Diagnosesicherung werden bei Verdacht auf ein Larynxkarzinom folgende Untersuchungen durchgeführt.
Indirekte Laryngoskopie Bei der instrumentellen Inspektion des Kehlkopfes wird neben der genauen Bestimmung der Größenausdehnung und der Lokalisation der Tumoren auch die Stimmlippenbeweglichkeit geprüft, die ein wichtiger Hinweis für die Tiefeninfiltration des Tumors darstellt.
Am äußeren Hals sollten mögliche vergrößerte Lymphknoten (insbesondere beim supraglottischen Larynxkarzinom) getastet werden.
Direkte Laryngoskopie Bei einer endoskopischen Inspektion des Larynxs in Narkose (Mikrolaryngoskopie) können
-
Probebiopsien gewonnen,
-
die Ausdehnung des Tumors bestimmt und
-
das therapeutische Vorgehen festgelegt werden.
Bisweilen können kleinere Tumoren dabei sofort reseziert werden. Zusätzlich werden die oberen Atem- und Speisewege zum Ausschluss eines Zweitkarzinoms untersucht (durch die sog. Panendoskopie).
CT, MRT und Sonografie Sie werden durchgeführt, um
-
detailliertere Informationen über die Ausdehnung der Tumoren zu erhalten und
-
mögliche Tumoreinbrüche in Nachbarorgane oder Lymphknotenmetastasen zu erkennen.
40.6.1.4 Therapie
Die Therapie der Wahl ist in aller Regel die operative Entfernung des Tumors. Ist der Patient aufgrund schwerwiegender kardiovaskulärer oder pulmonaler Begleiterkrankungen nicht operationsfähig, kommt eine alleinige Strahlentherapie (primäre Strahlentherapie) als Alternative in Frage. Bei ausgedehnten Tumoren mit Metastasierung der Halslymphknoten wird meist nach dem operativen Eingriff eine postoperative Strahlentherapie angeschlossen.
Ziel einer jeglichen therapeutischen Maßnahme ist die Erhaltung der Kehlkopffunktion (Ton- bzw. Sprachbildung und intakte Schluckfunktion). Je nach Lokalisation und Ausmaß des Tumors wird eine Chordektomie, eine Kehlkopfteilresektion oder eine Laryngektomie durchgeführt.
Chordektomie Ein Tumor, der auf die Stimmlippen beschränkt ist, kann über eine Stimmlippenentfernung (Chordektomie) operativ entfernt werden. Die Patienten haben meist nur eine bleibende Heiserkeit als Nebenwirkung des Eingriffs. Der Eingriff kann sowohl von außen (transzervikal) als auch von innen (endolaryngeal mit dem Laser) erfolgen.
Kehlkopfteilresektionen Bei Tumoren, die Teile des Kehlkopfes erfasst haben, wird eine Kehlkopfteilresektion durchgeführt. Damit kann eine eingeschränkte Stimmbildung erhalten bleiben. Als Nebenwirkung des Eingriffs treten dauerhafte hartnäckige Schluckprobleme auf. Auch diese Operation kann transzervikal oder endolaryngeal mit dem Laser durchgeführt werden, wobei die Lasermethode seit ca. 15 Jahren favorisiert wird und seltener Schluckprobleme hervorruft.
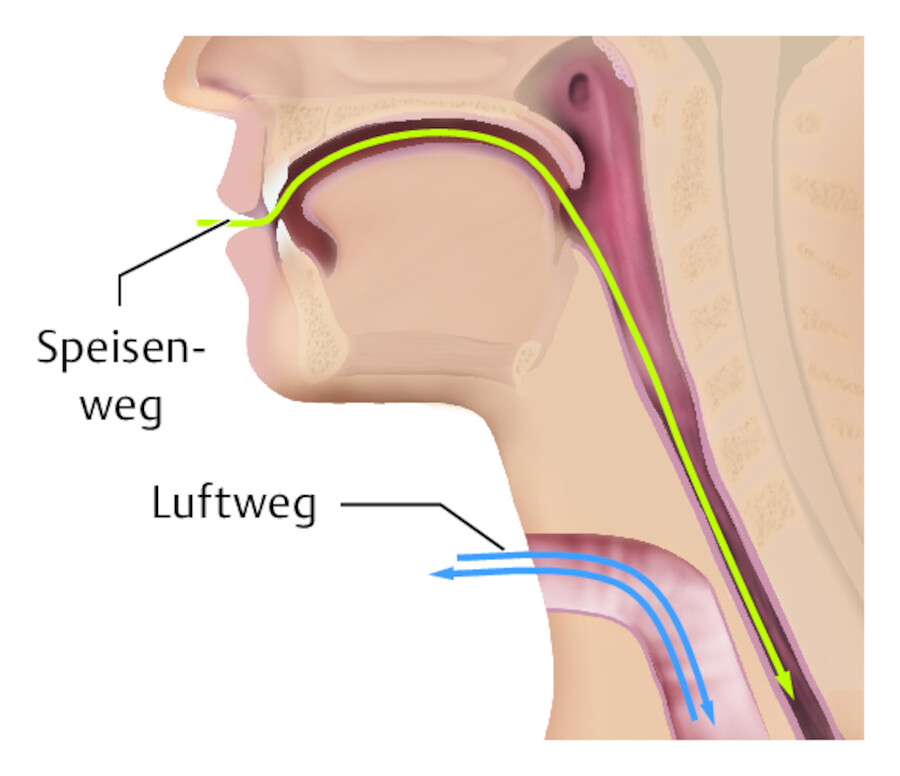
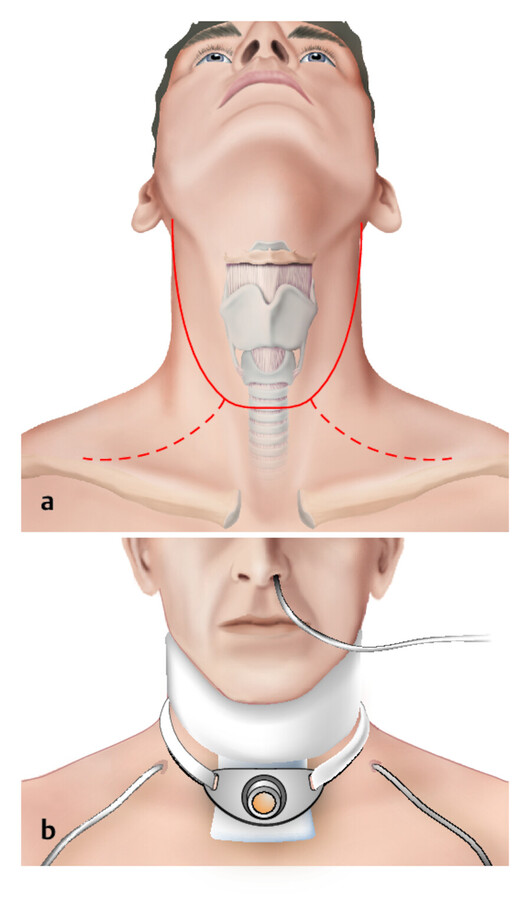
Laryngektomie Bei sehr ausgedehnten Kehlkopftumoren muss die Totalentfernung des Kehlkopfes (Laryngektomie) durchgeführt werden. Hierbei werden Luft- und Speiseweg getrennt und der abgesetzte Stumpf der Luftröhre als Tracheostoma in die Halshaut eingenäht ( ▶ Abb. 40.16). Der Verlust der sprachlichen Kommunikation ist für den Patienten die schwerwiegendste Folge des Eingriffs.
Laryngektomie.
Abb. 40.16 Nach dem Eingriff sind Atemweg und Schluckweg getrennt.
Bei ausgedehnten Tumoren finden sich häufig Halslymphknotenmetastasen. Wird der Kehlkopftumor chirurgisch entfernt, so schließt sich i. d. R. eine Ausräumung der Halslymphknoten (Neck dissection) in gleicher Sitzung, bei laserchirurgischer Entfernung in aller Regel ▶ zweizeitig nach einer Woche an.
40.6.2 Pflege- und Behandlungsplan
Eine Kehlkopfoperation hat einen tief greifenden Einfluss auf das gesamte Leben des Patienten. Wichtige Lebensaktivitäten, z. B. die Atmung, Ernährung und Kommunikation, sind nach der Operation zumindest zeitweise stark eingeschränkt.
Pflegeschwerpunkte sind die postoperative Versorgung und Gewährleistung der Kommunikation.
40.6.2.1 Postoperative Versorgung
Bei Kehlkopfeingriffen ist eine engmaschige Überwachung der Atemfunktion in den ersten Std. nach dem Eingriff notwendig. Auch bei kleinen Eingriffen kann es zu Schwellungen der Schleimhaut im Kehlkopfbereich und damit zu Atemnot kommen. Bei ausgedehnten Eingriffen bleibt der Patient 24 Std. intubiert. Er wird auf einer Intensivstation überwacht oder vorübergehend ▶ tracheotomiert.
In den ersten Stunden nach der Operation wird der Sauerstoffgehalt des Blutes kontinuierlich mit einem ▶ Pulsoxymeter gemessen. Bei einsetzender Atemnot oder sinkendem Sauerstoffgehalt des Blutes ist umgehend der Arzt zu informieren. Neben der Überwachung der Atemfunktion werden in folgenden Bereichen pflegerische Maßnahmen durchgeführt.
Wundpflege
Außer der Operationswunde (Schürzenlappen) wird beim laryngektomierten Patienten ein permanentes Tracheostoma angelegt ( ▶ Abb. 40.17). Die Wunddrainagen (Redondrainagen) verbleiben in aller Regel 2 – 4 Tage. Das Tracheostoma liegt offen und stellt somit eine potenzielle Infektionsquelle für die umliegende Haut dar. Für die Wundpflege ist zu beachten:
Permanentes Tracheostoma.
Abb. 40.17 Bei der Operation mittels Schürzenlappen (a) wird beim laryngektomierten Patienten ein permanentes Tracheostoma angelegt (b).
-
Der Wundverband muss stets sauber sein.
-
Die Wunddrainagen müssen regelmäßig kontrolliert werden.
-
Die ▶ Tracheostomapflege wird steril durchgeführt.
Atmung unterstützen
Das Atmen wird durch das Anlegen eines Tracheostomas zunächst erheblich gestört. Der natürliche Atemweg ist unterbrochen und die physiologische Funktion der Nase ist nicht mehr möglich. Die Luft wird ungefiltert über das Stoma eingeatmet. Die Trachea kann daher schnell austrocknen und sich entzünden (Tracheitis). Meist bestehen Probleme beim Abhusten von Trachealsekret, denn der Druckaufbau zum Abhusten ist durch den fehlenden Kehlkopf nicht mehr möglich. So kann sich durch eine unzureichende Bronchialtoilette Sekret ansammeln, bakteriell infizieren und zu einer Pneumonie führen. Die speziellen Maßnahmen bei Patienten mit Tracheostoma sind im Kapitel ▶ „Pflegemaßnahmen bei tracheotomierten Patienten“ zu finden.
Ernährung sicherstellen
Zur Unterstützung des Wundheilungsprozesses im Bereich der Pharynxnaht wird der Patient ca. 10 Tage über eine Magensonde ernährt, die intraoperativ gelegt wurde. Die Patienten erhalten einen Kostaufbau mit Sondennahrung, die über eine Ernährungspumpe entsprechend dosiert gegeben wird.
Der Sitz der Sonde am Naseneingang muss täglich kontrolliert und verändert werden, da Druckstellen entstehen können. Die Sonde wird so fixiert, dass sie nicht herausrutschen kann. Ein erneutes Einlegen im frischen Operationsgebiet birgt die Gefahr, die Pharynxnähte einzureißen. Bevor die Ernährungssonde entfernt werden kann, wird mit einer Röntgenkontrastuntersuchung die Dichtigkeit der Pharynxnähte geprüft. Nach dem Ziehen der Sonde erfolgt der orale Kostaufbau.
Bei kehlkopfteilresizierten Patienten ist die Gefahr der Aspiration groß. Deswegen wird ein vorsichtiger Kostaufbau mit Schlucktraining durch Logopäden durchgeführt.
40.6.2.2 Gewährleisten der Kommunikation
Die Betreuung von Patienten nach einer Kehlkopfoperation stellt eine besondere Herausforderung für Pflegende dar. Probleme der Patienten können nicht einfach besprochen werden, sondern müssen durch gute Beobachtung und nonverbale Kommunikation gelöst werden.
Stimmrehabilitation
In den ersten Tagen nach einer Laryngektomie erfolgt die Kommunikation schriftlich bzw. in Zeichensprache. Im Rahmen der eigentlichen Stimmrehabilitation stehen verschiedene Möglichkeiten zur Verfügung.
Elektroakustische Sprechhilfe Die einfachste Möglichkeit ist die Elektroakustische Sprechhilfe (Elektrolarynx, z. B. Servox). Durch den Apparat, den sich der Patient an die Halshaut hält, werden Schallschwingungen über die Haut in den Mundraum übertragen. Durch Sprechbewegungen des Mundes kann damit eine leise Ersatzstimme erzeugt werden.
Ösophagusersatzstimme Ein besseres Ergebnis ist durch das Erlernen der Ösophagusersatzstimme zu erwarten. Da beim Kehlkopflosen die für die Tonerzeugung benötigte Atemluft durch das Tracheostoma ungenutzt entweicht, muss der Patient lernen, Luft in den Magen zu schlucken und diese anschließend zum Sprechen willkürlich in den Rachen zu pressen.
Dies ist im Grunde genommen nichts anderes als ein Rülpsen, wobei die Tonerzeugung durch die Schwingungen der Schleimhautfalten im Bereich des Ösophaguseingangs erfolgt. Mit viel Training wird der Rülpston einem Kehlkopfton immer ähnlicher. Die Ösophagusersatzstimme hat zwar nicht die Kraft, Tondauer und Klangfarbe der Kehlkopfstimme, ermöglicht aber eine gut verständliche Sprache.
Shuntprothesen Die beste Möglichkeit, eine Ersatzstimme zu bilden, wird durch Shuntprothesen (Sprechprothesen, z. B. Provox) erreicht. Hierzu wird intraoperativ eine tracheo-ösophageale Fistel gebildet. In die Öffnung wird dann ein Shuntventil aus Silikon eingesetzt. Durch das Ventil kann die über das Tracheostoma in die Lungen eingeatmete Luft anschließend beim Ausatmen und gleichzeitigem Zuhalten des Tracheostomas in den Ösophagus gelangen.
Hier wird die Luft, ähnlich wie bei der Ösophagusersatzstimme, zur Stimmbildung benutzt. Da das gesamte Atemvolumen nun zur Stimmbildung zur Verfügung steht, können lange Sätze ohne Unterbrechung gesprochen werden.
Die Stimmrehabilitation wird durch Logopäden unterstützt.
Merke
Das Einbringen von Shuntprothesen stellt heute die anzustrebende Art und Weise der Stimmrehabilitation dar.
40.7 Pflege von Patienten mit Nasennebenhöhlenerkrankungen
40.7.1 Medizinischer Überblick chronische Sinusitis
40.7.1.1 Definition
Bei der Sinusitis ist die Schleimhaut einer oder mehrerer Nasennebenhöhlen entzündet. Eine chronische Sinusitis liegt dann vor, wenn über einen Zeitraum von mindestens 8 Wochen Symptome bestehen oder 4 Episoden einer akuten Sinusitis im Jahr auftreten und Veränderungen im CT auch nach medikamentöser Vorbehandlung nachweisbar sind.
40.7.1.2 Ursachen
Durch Engstellen in den Ausführungsgängen der Nasennebenhöhlen oder durch eine starke Septumdeviation kommt es zur Behinderung des Sekretabflusses. Dadurch können sich Bakterien, Viren oder Pilze ansiedeln. Die chronische Sinusitis geht mit einer hyperplastischen (verdickten) Schleimhaut einher.
40.7.1.3 Symptome
Die Patienten haben Schmerzen und ein Druckgefühl im Bereich der Nasennebenhöhle. Begleitsymptome sind das Gefühl der behinderten Nasenatmung und ein chronischer Schleimfluss im Rachen, besonders in den Morgenstunden. Mitunter kann auch das Geruchsvermögen eingeschränkt sein.
40.7.1.4 Diagnostik
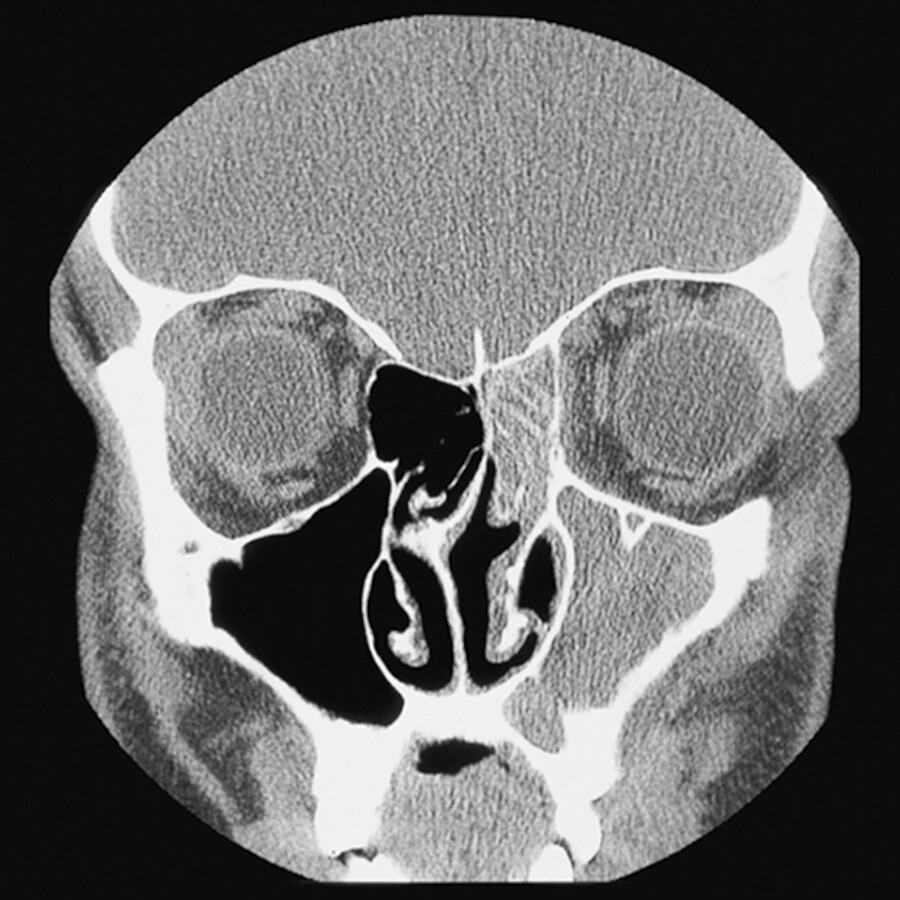
Zur genaueren Untersuchung der Nasennebenhöhlen wird in der Nasenhaupthöhle insbesondere der mittlere Nasengang unterhalb der mittleren Muschel endoskopiert. Mit der Nasenendoskopie können z. B. Nasenpolypen beobachtet werden. Anschließend erfolgt eine CT der Nasennebenhöhle. Hierbei zeigt sich eine verdickte Schleimhaut, die bisweilen auch einige oder alle Nasennebenhöhlen vollständig verlegen kann ( ▶ Abb. 40.18).
Chronische Sinusitis.
Abb. 40.18 Bei einer chronischen Sinusitis sind im CT-Bild Schleimhautschwellungen zu sehen.
40.7.1.5 Therapie
Zunächst wird konservativ behandelt. Der Patient erhält kortikoidhaltige Nasensprays (z.B. Nasonex, Pulmicort) in Kombination mit einem Sekretolytikum (z. B. ACC 600, Sinupret) verabreicht. Bei einer zusätzlich vorhandenen akuten Entzündung wird auch eine kurzzeitige Therapie mit einem Antibiotikum durchgeführt.
Sollte auch nach mehreren Wochen der konservativen Therapie keine Besserung eingetreten sein, wird eine endoskopische Nasennebenhöhlenoperation durchgeführt, um die Ausführungsgänge der Nasennebenhöhlen zu erweitern. Zusätzlich sollte eine Septumdeviation intraoperativ korrigiert werden.
40.7.2 Medizinischer Überblick Nasenpolypen
40.7.2.1 Definition
Nasenpolypen (Polyposis nasi) sind polypöse Schleimhautwucherungen, die durch die Ostien der Nasennebenhöhlen in die Nase vorwachsen.
40.7.2.2 Ursachen und Symptome
Die Ursachen sind bisher nicht geklärt. Folgende Anzeichen treten auf:
-
Druckgefühl über den Nasennebenhöhlen
-
Geruchsstörungen oder das völlige Fehlen des Geruchssinns
-
verstopfte Nase
-
veränderter Stimmklang
40.7.2.3 Diagnostik
Bei der HNO-ärztlichen Untersuchung zeigen sich glasige Polypen, die meist aus dem mittleren Nasengang kommen und die Nasenhaupthöhle ganz verlegen können. In der CT zeigt sich eine Verschattung der Nasennebenhöhle.
40.7.2.4 Therapie
Polypen werden operativ über eine endonasale Nasennebenhöhlenoperation entfernt und mit einem kortikoidhaltigen Nasenspray nachbehandelt. Bei kleinen Polypen reicht in manchen Fällen die alleinige Verabreichung eines kortikoidhaltigen Nasensprays aus.
40.7.3 Pflege- und Behandlungsplan
Die Patienten befinden sich nur in stationärer Behandlung, wenn ihre Erkrankungen der Nasennebenhöhlen operativ versorgt werden müssen. Operationen der Nasennebenhöhlen werden heute minimal-invasiv endoskopisch oder mikroskopisch durch die Nase (endonasaler Zugang) durchgeführt, ohne äußerliche Narben im Gesicht zu hinterlassen. Nur noch selten werden Zugangswege von außen gewählt. Die Sicherheit bei der endoskopischen Nasennebenhöhlenoperation kann durch den Einsatz von CT-gesteuerten Navigationsgeräten erhöht werden.
Im Rahmen der Nasennebenhöhlenoperation führen die Pflegenden die präoperative Betreuung und postoperative Versorgung durch.
40.7.3.1 Präoperative Betreuung
Vor der Operation erhält der Patient die Möglichkeit zu duschen. Um das Risiko einer Nachblutung zu reduzieren, sollte er dann in den ersten 5 postoperativen Tagen nicht duschen und auch keine Haare waschen. Wird ein Zugangsweg von außen gewählt, muss bei Männern evtl. der Bart rasiert werden.
40.7.3.2 Postoperative Versorgung
Nach der Operation ist die Operationshöhle mit einer entsprechenden Nasentamponade vor frischen Nachblutungen geschützt. Dennoch kann es zu Nachblutungen kommen. Daher ist ein verstärktes Bluten durch die Tamponade oder im Rachen (Inspektion des Rachens durch die Pflegende) dem Operateur zu melden.
Erstmaßnahmen bei Blutungen Der Patient wird in eine halb sitzende Position gebracht. Ihm wird eine Eiskrawatte in den Nacken gelegt, außerdem muss der Blutdruck kontrolliert werden. Eine hypertensive Phase muss evtl. medikamentös behandelt werden.
Überwachung bei Komplikationen Die postoperative Kontrolle sollte auch Sehstörungen und Störungen der Augenbeweglichkeit sowie Schwellungen oder Einblutungen im Bereich der Augenlider oder des Auges beinhalten. Durch Eingriffe in den Nasennebenhöhlen können leicht Verletzungen des Auges oder des Augenhöhleninhalts vorkommen. Sowohl Augapfel als auch Sehnerv können geschädigt werden. Verletzungen der Augenhöhle können an einem beginnenden Bluterguss im Bereich des Auges erkannt werden. In all diesen Fällen sollte der Operateur verständigt und ein augenärztliches Konsil durchgeführt werden.
Merke
Beginnende Kopfschmerzen und Nackensteifigkeit können ein erstes Warnsymptom einer intraoperativen Verletzung der Schädelbasis und einer ▶ beginnenden Meningitis sein. Auch diese Warnsymptome müssen umgehend gemeldet werden.
Überwachung der Mundschleimhaut Da die Nasentamponade meist für 2 Tage belassen wird und der Patient in dieser Zeit nur durch den Mund atmen kann, besteht die Gefahr, dass der Mund stark austrocknet und es zu Halsentzündungen kommt. Daher sind eine gute Flüssigkeitszufuhr und Inhalationen wichtig. Mit einem Kaltluftvernebler wird die Raumluft angefeuchtet. Der Patient erhält direkt nach der Operation Glyzerinstäbchen mit Zitronengeschmack zum Lutschen. Sobald er wieder trinken darf, muss auf eine ausreichende Flüssigkeitszufuhr geachtet werden.
Entfernen der Nasentamponade Am 2. postoperativen Tag wird die Nasentamponade entfernt. Danach kann es kurzfristig nochmals zu stärkerem Nasenbluten kommen, daher sollten dem Patienten prophylaktisch eine Eiskrawatte in den Nacken gelegt und eine Nierenschale vorgehalten werden. Der Patient wird angehalten, sich auch nach der Entfernung der Nasentamponade in den nächsten 3 Tagen nicht zu schnäuzen.
Nasenpflege Da die Nasenatmung in der Phase der postoperativen Wundheilung durch eine reaktive Schleim- und Sekretbildung verlegt ist, wird mindestens 1-mal täglich die Nasenhaupthöhle durch den Arzt abgesaugt. Für die weitere Pflege erhält der Patient rückfettende Nasensalben, die auch abschwellende Wirkstoffe enthalten. Diese sollten in den ersten 8 Tagen nach der Entfernung der Tamponade 3-mal täglich angewandt werden.
40.8 Pflege von Patienten mit Erkrankungen des Ohres
Ohrenerkrankungen sind angeborene oder erworbene Anomalien, Entzündungen, degenerative oder dystrophische Veränderungen, z. B.
-
des äußeren Ohres (z. B. Mikrotie, abstehende Ohren),
-
des Mittelohres (z. B. Paukenerguss, Otitis media) oder
-
des Innenohres (z. B. Hörsturz, Altersschwerhörigkeit).
Stellvertretend für die Vielzahl von Ohrenerkrankungen werden der Paukenerguss und die Innenohrschwerhörigkeit näher vorgestellt.
40.8.1 Medizinischer Überblick Paukenerguss
40.8.1.1 Definition
Bei einem Paukenerguss sammelt sich Flüssigkeit in der Paukenhöhle an.
40.8.1.2 Ursachen
Die Ursachen liegen in anhaltenden Tubenfunktionsstörungen und einem ständigen Unterdruck in der Paukenhöhle. Häufig leiden Kinder im Vorschulalter mit vergrößerten Adenoiden (Rachenmandeln, im Volksmund Polypen genannt) und Patienten mit Gaumenspalten an Paukenergüssen.
40.8.1.3 Symptome
Durch die Dämpfung der Schallübertragung und Herabsetzung der Schwingungsfähigkeit des Trommelfells ist eine Hörminderung zu beobachten.
40.8.1.4 Diagnostik
Mit folgenden Untersuchungsmethoden wird die Diagnose gesichert:
-
Otoskopie (Ohrspiegelung)
-
Tympanogramm (zur Ermittlung der Schwingungsfähigkeit des Trommelfells)
40.8.1.5 Therapie
Die konservative Therapie erfolgt mit Nasenspray (z. B. Otriven), Schleimlöser (z. B. ACC) und dem Valsalva-Versuch (Ausatmung bei zugehaltener Nase und geschlossenem Mund). Ist die konservative Behandlung nicht erfolgreich, wird eine operative Trommelfellpunktion (Parazentese) durchgeführt, bei der evtl. ein Paukenröhrchen zur Drainage eingelegt und ggf. eine Entfernung der Rachenmandel durchgeführt wird.
40.8.2 Medizinischer Überblick Innenohrschwerhörigkeit
40.8.2.1 Definition und Ursachen
Unter Schwerhörigkeit versteht man ein herabgesetztes Hörvermögen durch einen Funktionsverlust der Sinneszellen. Diese Schwerhörigkeit kann symmetrisch, beidseitig und langsam fortschreitend auftreten, dann handelt es sich meist um eine Altersschwerhörigkeit. Nach einem Hörsturz tritt ein Funktionsverlust des Hörorganes plötzlich und einseitig auf.
40.8.2.2 Symptome
Altersschwerhörige Patienten haben zunehmend Schwierigkeiten, im Gespräch mit mehreren Personen das Gesprochene richtig zu verstehen. Bei einem Hörsturz kommen unterschiedlich ausgeprägte Funktionsverluste von nur leichten Hörminderungen bis hin zur vollständigen Ertaubung vor.
40.8.2.3 Diagnostik
Sie geschieht durch Hörprüfungen, z. B. die Tonaudiometrie. Dabei markiert der Patient den Zeitpunkt, zu dem er einen angegebenen Ton hört. Auch objektive, teils computergestützte Hörprüfungen werden angewandt.
40.8.2.4 Therapie
Bisher steht zur Behandlung der Altersschwerhörigkeit nur die Versorgung mit Hörgeräten zur Verfügung. Der plötzliche Hörverlust wird durch mehrere Tage dauernde Verabreichung von Infusionen mit Kortison behandelt.
40.8.3 Pflege- und Behandlungsplan
Menschen mit Erkrankungen des Ohres können Geräusche nicht differenziert wahrnehmen. Im Krankenhaus sind schwerhörige oder am Ohr erkrankte Menschen oftmals noch von Geräuschen umgeben, die sie nicht kennen und demzufolge auch nicht einordnen können. Das kann zu Verunsicherungen und Ängsten führen.
Bei Patienten mit Erkrankungen des Ohres führt die Pflegende die Ohrenpflege, die prä- und postoperative Maßnahmen bei Ohroperationen und die Beratung bei Schwerhörigkeit durch.
40.8.3.1 Ohrenpflege
Grundsätzlich reinigt der Gehörgang sich selbst. Nach Ohroperationen wird die Pflege durch den Operateur vorgenommen, um die Wundheilung im Gehörgang zu beurteilen. Die Pflegende verabreicht dem Patienten auf Anordnung des Arztes Ohrentropfen.
Verabreichen von Ohrentropfen Vor der Anwendung werden die Tropfen in der Hand erwärmt. Der Patient wird gebeten, seinen Kopf zur Seite zu drehen. Die Pflegende dehnt den Gehörgang, indem sie die Ohrmuschel leicht nach oben hinten zieht. Die angeordnete Tropfenanzahl kann dann in das Ohr getropft werden. Nach der Applikation sollte der Patient noch ca. 5 – 10 Min. auf der Seite liegen bleiben.
Bei manchen Ohrenerkrankungen (z. B. Otitis media) ist es erforderlich, zusätzlich Nasentropfen zu verabreichen, um ein Abschwellen des Nasenrachens und des Eingangs der Ohrtrompete zu erreichen. Hierzu werden die Nasentropfen in Rückenlage mit überstrecktem Kopf verabreicht.
40.8.3.2 Präoperative Maßnahmen
Am Vorabend der Operation erhält der Patient die Möglichkeit, seine Haare zu waschen. Um eine Wundinfektion zu vermeiden, darf er mindestens 1 Woche nach der Operation keine Haare waschen. Bei einem retroaurikulären (hinter der Ohrmuschel) Zugang wird am Vorabend gut 2 Finger breit um das Ohr herum rasiert. Für ausgedehntere Eingriffe muss eine entsprechend große Fläche hinter dem Ohr rasiert werden.
40.8.3.3 Postoperative Maßnahmen
Bei allen Patienten werden postoperativ neben den Vitalzeichen auch Anzeichen einer Komplikation überwacht (Wunddehiszenz, Wundinfektion, Schwindel, Gesichtslähmung). Es ist darauf zu achten, dass der Verband gut sitzt, da bei schlechtem Sitz (z. B. bei umgeknickten Ohrläppchen) Schmerzen entstehen können. Bei Eingriffen an der Ohrmuschel können Hämatome unter dem Verband entstehen, weswegen der Verband ständig fest sitzen muss.
Um das operative Ergebnis bei einer Tympanoplastik (Gehörknöchelchenplastik) oder einer Stapesplastik (Steigbügelplastik) nicht zu beeinträchtigen, haben die Patienten 3 Tage ein Schneuzverbot einzuhalten, um einen plötzlichen Überdruck im Mittelohr zu vermeiden. Die Belüftung des Mittelohres sollte durch die Gabe von Nasentropfen verbessert werden.
Merke
Nach einer Stapesplastik-Operation können Patienten in der ersten postoperativen Phase unter Schwindel und Übelkeit leiden. Sie sollten daher 12 Std. Bettruhe einhalten und erst dann mobilisiert werden.
Bei den meisten Ohroperationen liegt im Gehörgang eine Tamponade. Über dem Ohr wird ein lockerer Verband (z. B. Ohrklappe) angelegt, der anfangs täglich gewechselt werden sollte. Am 7. Tag werden die Fäden gezogen. Die Tamponade verbleibt weitere 7 – 14 Tage und wird vom Operateur dann endgültig entfernt. Während der gesamten Zeit sollte die Gehörgangstamponade mit Ohrentropfen feucht gehalten werden, da sie sonst austrocknet und sich schwerer entfernen lässt.
40.8.3.4 Beratung bei Schwerhörigkeit
Der Umgang mit schwerhörigen oder gehörlosen Menschen erfordert besondere Kenntnisse und großes Einfühlungsvermögen. Die eigentliche Betreuung, Versorgung und Rehabilitation geschieht durch HNO-Ärzte, Logopäden und Sprachtherapeuten. Viele schwerhörige oder gehörlose Menschen lesen von den Lippen ab, andere verständigen sich in der Gebärdensprache. Allen gemeinsam ist, dass sie in der Gemeinschaft der Hörenden und Sprechenden verloren sind. Im Umgang mit schwerhörigen und gehörlosen Patienten sind daher gewisse Regeln zu beachten:
-
sich Zeit nehmen – z. B. bei der Aufnahme und bei OP-Vorbereitungen
-
anschauen – beim Sprechen immer wieder dem Patienten das Gesicht zuwenden
-
deutlich sprechen – nicht unbedingt laut, aber in kurzen Sätzen und langsam, damit der Patient von den Lippen ablesen und die Mimik einbeziehen kann
-
Körperkontakt anbieten – Schwerhörige und Gehörlose suchen Körperkontakt zum Gegenüber; er gibt ihnen ein sicheres Gefühl
-
das Gespräch suchen – und nicht die Kommunikation scheuen, weil sie schwierig oder zeitaufwändig erscheint
-
zeichnen oder schreiben – als Alternative bei schwierigen Sachverhalten
Hörgeräte
Definition
Ein Hörgerät ist eine akustische Hörhilfe für Schwerhörige, die im Prinzip wie ein Schallverstärker funktioniert.
Bei Schwerhörigkeit können dem Patienten Hörgeräte angepasst werden, die ihn dann wieder besser mitreden und soziale Kontakte knüpfen lassen können. Durch den Fortschritt der Technik und Elektronik können immer bessere und immer kleinere Hörgeräte gefertigt werden ( ▶ Abb. 40.19).
Hörgerät.
Abb. 40.19 Das Hinter-dem-Ohr-Gerät (Hdo-Gerät) kann Hörminderungen aller Grade ausgleichen.
(Foto: K. Oborny, Thieme)
40.9 Pflege von Patienten mit Erkrankungen der Haut
Anatomie und Physiologie im Fokus
(nach Schwegler u. Lucius 2016)
Die Haut im Überblick
Die Oberfläche unseres Körpers beträgt ungefähr 1,5 – 2 m². Bei einer Dicke der oberen Hautschichten von 2 – 3 mm und einer sehr variablen Dicke der Subkutis (Fettgewebe) errechnet sich ein Gesamtgewicht der Haut von 3 – 10 kg. Die Haut ist im Gegensatz zu den inneren Organen sehr widerstandsfähig und dient als eine Art „Schutzschild“ gegen mechanische und chemische Schädigungen.
Aufbau
Als Grenzfläche zwischen dem Körperinneren und der „Außenwelt“ besteht die Haut (Cutis) aus einem oberflächlichen Epithel (Oberhaut, Epidermis), das mit der daruntergelegenen Bindegewebsschicht (Lederhaut, Dermis oder Corium) verwachsen ist. Die Hautanhangsgebilde Drüsen, Haare und Nägel entstehen aus der Oberhaut, während die Lederhaut mit ihren parallel zur Oberfläche laufenden Kollagenfasern für die mechanische Festigkeit der Haut sorgt. Die Oberhaut besitzt ein mehrschichtiges verhornendes Deckepithel. Die Fettschicht des Unterhautgewebes schützt vor Auskühlung und speichert Energie ( ▶ Abb. 40.20).
Funktion
Die Haut erfüllt verschiedene Funktionen und Aufgaben. Dazu zählen:
-
Schutz: vor mechanischen, chemischen, elektrischen Einwirkungen, Hitze- und Kälteschäden, dem Eindringen von Bakterien
-
Speicher: für Wasser, Fett und andere Bestandteile des Stoffwechsels
-
Wärmeausgleich und Flüssigkeitshaushalt: maßgeblich am Wasserhaushalt beteiligt durch Haargefäßnetz und Schweißdrüsen
-
Sensibilität: Nervenenden und Rezeptoren registrieren Schmerz, Temperatur, Berührung und Druck.
-
Immunorgan: Erkennung von Fremdsubstanzen (z. B. Bakterien, Viren, Allergene) und Aktivierung des Immunsystems
-
Vitamin D Haushalt: Vitamin-D-Synthese
-
Erscheinungsbild und Aussehen: Emotionen spiegeln sich in der Haut wider („Spiegel der Seele“)
Querschnitt durch die Haut mit den verschiedenen Hautschichten.
Abb. 40.20

40.9.1 Medizinischer Überblick Ekzemerkrankungen
40.9.1.1 Definition
Unter „Ekzem“ versteht man eine Gruppe nicht-infektiöser, entzündlicher Hauterkrankungen, die durch verschiedene Auslöser hervorgerufen werden können. Klinisch werden Ekzeme je nach Stadium durch Rötung, Bläschen, Nässen, Krusten, Schuppung und Lichenifikation charakterisiert, sodass akute, subakute und chronische Ekzeme unterschieden werden können. Häufig wird der Begriff „Dermatitis“ synonym verwendet. Wichtige Ekzemerkrankungen sind:
-
Kontaktekzem (allergisch oder nicht-allergisch bedingt),
-
atopisches Ekzem (Synonym: atopische Dermatitis, Neurodermitis)
-
seborrhoisches Ekzem (chronisches Ekzem besonders am behaarten Kopf, naso-labial, vordere und hintere Schweißrinne).
Etwa 15 – 21 % aller Patienten mit Hauterkrankungen leiden unter Ekzemerkrankungen.
Für die Beschreibung von Hauterkrankungen sind Grundkenntnisse in unterschiedlichen Hautveränderungen (Effloreszenzen) ( ▶ Tab. 40.1 ) unabdingbar. Die Wirksamkeit der dermatologischen Therapie wird von verschiedenen Faktoren bestimmt:
-
Liberation (Freisetzung) des Wirkstoffes aus Externa
-
Adsorption des Wirkstoffes abhängig von der oberen Hautschicht
-
Absorption des Wirkstoffes aus Externa
-
Penetration als Vermögen des Wirkstoffes, in die Haut einzudringen
-
Permeation als Eigenschaft des Wirkstoffes, die Haut zu durchdringen
-
Resorption als Eigenschaft des Wirkstoffes, nach Durchdringung der Haut in das Blut-, und Lymphsystem des Körpers einzudringen, was mit systemischen Wirkungen verbunden sein kann.
|
Primäreffloreszenzen (unmittelbar durch die Erkrankung verursacht) |
Sekundäreffloreszenzen (entstehen im Anschluss an eine primäre Effloreszenz) |
|
|
Arzneimittel im Fokus
Externa
Dies sind Zubereitungen für die topische (örtlich, lokal) Therapie. Die prinzipielle Zusammensetzung von Grundlagen für die Therapie zeigt ▶ Abb. 40.21.
Grundsätzliche Zusammensetzung von Externa für die dermatologische Therapie.
Abb. 40.21

Wässrige Lösungen
Sie wirken als feuchte Umschläge oder Verbände durch Verdunstungskälte kühlend und haben damit abschwellende, antientzündliche und juckreizlindernde Eigenschaften. Durch Zusatz von Antiseptika sind sie z. B. bei Hautinfektionen geeignet; zugesetzte Alkohole erhöhen den Kühleffekt durch Verdunstungskälte.
Fette
Vaseline oder Paraffin bilden einen Film auf der Hautoberfläche, der einen Schutz vor hydrophilen (wasserlöslichen) Stoffen bildet. Sie lassen sich mit Wasser nicht abwaschen, wirken hautaufweichend und fördern die Penetration von Arzneimitteln. Sie wirken der Feuchtigkeits- und Wärmeabgabe entgegen.
Öle
Sie werden insbesondere als Badezusätze verwendet, die der Rückfettung der ausgetrockneten Haut dienen.
Puder
Dies sind pertikuläre Feststoffe, die durch ihre große Oberfläche Verdunstung fördern und durch Verdunstungskälte kühlend und antientzündlich wie auch austrocknend wirken. In Abhängigkeit vom Feststoff können sie Sekret aufnehmen.
Schüttelmixturen
Diese Suspensionen aus Feststoff und Flüssigkeit müssen vor Gebrauch geschüttelt werden, da sich ihre Bestandteile beim Stehen trennen. Nach dem Auftragen mit einem Pinsel verdunstet die Flüssigkeit durch die große Oberfläche des Feststoffs. Dies entzieht der Haut Wärme und Feuchtigkeit; übrig bleibt eine fest haftende Puderschicht.
Pasten
Sie bestehen aus Fett und pulverförmigen Bestandteilen und wirken abdeckend und hautschützend. Je höher der Anteil der Pulverbestandteile ist, desto härter ist die Paste. Eine harte Zinkpaste eignet sich z. B. zur Abdeckung von Ulkusrändern, um den Kontakt der Haut mit Ulkustherapeutika zu verhindern. Weiche Pasten wirken stärker antientzündlich und fettend, der Wärmestau ist geringer.
Salben
Diese bestehen aus unterschiedlichen Fetten. Sie erweichen Keratosen, haben okklusive (verschließende) Effekte, die zu Sekret- und Wärmestau führen können, und sind i. d. R. schlecht abwaschbar.
Cremes
Dies sind hydrophile (Öl-in-Wasser-) oder lipophile (Wasser-in-Öl-)Emulsion, die sich durch den Fettgehalt unterscheiden. Umgangssprachlich werden Cremes vom Wasser-in-Öl-Typ gelegentlich auch als Salbe bezeichnet. Wirkstoffe können in die Wasser- oder Fettphase eingearbeitet werden.
40.9.2 Medizinischer Überblick akute Kontaktdermatitis
40.9.2.1 Definition
Die akute Kontaktdermatitis ist eine akute, entzündliche Reaktion der Haut. Man unterscheidet nach dem auslösenden Mechanismus zwischen der akuten toxischen und der akuten allergischen Kontaktdermatitis.
40.9.2.2 Ursachen
Die akute toxische Kontaktdermatitis entsteht nach äußerlichem Kontakt mit einer obligat toxischen (die Haut schädigenden) Noxe. Die akute allergische Kontaktdermatitis basiert auf einer Immunreaktion (Typ-IV-Allergie); prinzipiell muss dabei eine Sensibilisierung für ein Kontaktallergen vorausgegangen sein.
40.9.2.3 Symptome
Klinisch sind beide Formen kaum voneinander zu unterscheiden. Es findet sich eine Entzündungsreaktion der Haut mit Erythem (Rötung), Schwellung, Bläschen (Blasen) und nässenden, gelegentlich auch erosiven Veränderungen. Beim toxischen Ekzem ist die Entzündung streng auf den Ort beschränkt, an dem die Noxe auf die Haut eingewirkt hat. Die Hautveränderung ist i. d. R. scharf begrenzt. Bekannt sind solche Reaktionen insbesondere nach Kontakt mit starken chemischen Irritanzien, aber auch bei Verätzungen mit Säuren oder Laugen. Bei allergischen Kontaktekzemen werden auch Streureaktionen in der Umgebung des Allergenkontakts beobachtet.
40.9.2.4 Diagnostik
Der Nachweis eines allergischen Geschehens kann durch einen Epikutantest (Hauttest) erfolgen. Ein allergisches Kontaktekzem tritt frühestens Stunden nach dem Allergenkontakt auf, i. d. R. erst nach ein bis zwei Tagen. Das Maximum der Reaktion ist meist etwa 72 Stunden nach Exposition mit dem Kontaktallergen erreicht.
40.9.2.5 Therapie
Bei der Behandlung der akuten toxischen Kontaktdermatitis steht die Entfernung der auslösenden Substanz durch Abwaschen oder Baden zunächst im Vordergrund. Bei beiden Formen können gegen die Entzündung Glukokortikosteroide zur Anwendung kommen, im akuten Stadium werden topisch kühlende Umschläge mit Antiseptika verabreicht. Ein allergisches Kontaktekzem benötigt längere Zeit, um komplett abzuheilen. Eine exakte Diagnostik zum Nachweis des auslösenden Allergens ist notwendig, damit der Patient eine erneute Allergenexposition vermeiden kann.
40.9.3 Medizinischer Überblick chronisches Kontaktekzem
40.9.3.1 Definition
Das chronische Kontaktekzem ist eine Entzündungsreaktion der Haut. Man unterscheidet:
-
kumulativ-subtoxisches Kontaktekzem: nicht-allergisches Ekzem, das durch subtoxische (allein nicht hautschädigende) Einwirkungen auf die Haut entsteht ( ▶ Abb. 40.22).
Chronisches Kontaktekzem.
Abb. 40.22 a Handekzem mit Rötung, Schuppung und Rhagaden, b Windeldermatitis, hier über die Grenzen des Windelbereichs hinausgehend.

-
allergisches Kontaktekzem: basiert auf einer zellulären Immunreaktion (Typ-IV-Allergie) und setzt eine frühere Sensibilisierung voraus.
Häufigkeit des allergischen Kontaktekzems Geschätzt sind 15 – 20 % der Bevölkerung für zumindest ein Kontaktallergen sensibilisiert, und 5 – 10 % leiden zumindest einmal pro Jahr unter einem allergischen Kontaktekzem.
40.9.3.2 Ursachen
Kumulativ-subtoxisches Kontaktekzem Häufiges Händewaschen und Desinfizieren führt besonders im Winter bei empfindlicher, trockener Haut, insbesondere bei Atopie, zu einem Handekzem. Unter dieses Krankheitsbild fallen auch Leckekzeme an den Lippen, Pflasterreizungen sowie die Windeldermatitis.
Allergisches Kontaktekzem Nach erfolgter Sensibilisierung führt die erneute Exposition gegenüber einem Allergen zur Entzündungsreaktion. Die Sensibilisierung setzt ein gewisses Irritationspotenzial der Substanz voraus. Daneben erleichtert eine Schädigung der Hautbarriere das Eindringen der Substanz in die Haut.
Merke
Das wichtigste Kontaktallergen stellt Nickel dar. Sensibilisierungen für Duft- und Konservierungsstoffe und Salbengrundlagen, aber auch für Medikamente, Gummiinhaltsstoffe, Textilfarben und Pflanzen sind nicht selten.
40.9.3.3 Symptome
Kumulativ-subtoxisches Kontaktekzem Klinisch ist die Haut trocken, gerötet, schuppig und rissig und häufig besteht Juckreiz. Der Verlauf ist chronisch, wenn die Ursache der Erkrankung nicht beseitigt werden kann. Durch die Schädigung der Hautbarriere treten sekundär häufig Allergien auf. Auch für eine „Latexallergie – „Soforttyp-Allergie gegen Naturlatex“ ist diese Form des Handekzems ein bedeutender Risikofaktor.
Allergisches Kontaktekzem Als Hautreaktion entstehen i. d. R. 24 – 48 Stunden nach dem Allergenkontakt zunächst Rötung, Ödem, Bläschen und Juckreiz. Auch nach Entfernung des Allergens nimmt die Hautreaktion zu und erreicht nach etwa 3 Tagen ihren Höhepunkt. Bei chronischer Allergenexposition stehen Juckreiz, trockene Schuppung und weniger die Rötung der Haut im Vordergrund.
40.9.3.4 Diagnostik
Kumulativ-subtoxisches Kontaktekzem Dies kann rein klinisch häufig nicht sicher gegen ein allergisches Kontaktekzem abgegrenzt werden. Hier ist der Epikutantest zum Ausschluss einer Sensibilisierung sehr wichtig.
Allergisches Kontaktekzem Das Kontaktallergen kann durch einen Epikutantest identifiziert werden. Dabei werden definierte Substanzen mittels spezieller Testpflaster auf der Rückenhaut für 24 oder 48 Std. appliziert. Die Ablesung erfolgt nach (24 Std.), 48 Std. und 72 Std. Im positiven Fall bildet sich im Testfeld eine entzündliche Hautreaktion.
40.9.3.5 Therapie
Kumulativ-subtoxisches Kontaktekzem Kurzfristig können zum Abklingen der Entzündungsreaktion topische Glukokortikosteroide angewendet werden. Wichtig ist eine intensive Hautpflege und bei Ekzemen an den Händen die Verwendung von Hautschutzpräparaten. Pflegepräparate mit Harnstoff erhöhen die Wasserbindungsfähigkeit der Hornschicht (nicht bei Hautverletzungen, im Gesichts- oder Windelbereich anwenden!).
Allergisches Kontaktekzem Die langfristige Therapie besteht in der Meidung des Kontaktallergens. Kurzfristig können topische Glukokortikosteroide und bei akuten Formen antiseptische, kühlende Umschläge die Entzündung der Haut lindern. Bei ausgedehnten Formen sind systemische Glukokortikosteroide angezeigt.
Merke
Irritative Handekzeme treten oft in Berufen mit Feuchtigkeitsbelastung der Haut (häufiges Händewaschen, -desinfizieren, Handschuhtragen) auf. Intensive Hautschutz- und Hautpflegemaßnahmen können das Auftreten von Ekzemen verhindern. Eine gestörte Hautbarriere stellt einen wichtigen Risikofaktor für die Entwicklung von Allergien dar.
40.9.4 Medizinischer Überblick atopisches Ekzem
40.9.4.1 Definition
Das atopische Ekzem (Synonyme: atopische Dermatitis, endogenes Ekzem, Neurodermitis) ist eine chronische oder chronisch-rezidivierende, nicht kontagiöse, erbmäßig verankerte Hauterkrankung mit starkem Juckreiz, deren klinisches Bild und Lokalisation altersabhängig variiert. Aktuell wird in der deutschen Leitlinie wieder der Begriff „Neurodermitis“, der dem Sprachgebrauch von Patienten entspricht, favorisiert.
Häufigkeit Sie beträgt bei Kindern in Deutschland derzeit ca. 13% und bei Erwachsenen 1 – 3 %.
40.9.4.2 Ursachen
Voraussetzung ist eine genetische Veranlagung, wobei kein einzelnes Gen verantwortlich gemacht werden kann. Provokationsfaktoren sind Aeroallergene (insb. Hausstaubmilbenallergene), Nahrungsmittelallergene, Staphylococcus aureus, klimatische Einflüsse, Hormone und Stress. Eine wesentliche Ursache stellt auch eine genetisch bedingte Störung der Hautbarriere da.
40.9.4.3 Symptome
Die Erkrankung manifestiert sich bei etwa 50 % der Betroffenen in den ersten 6 Lebensmonaten und bei bis zu 85 % aller Betroffenen vor dem 5. Lebensjahr. Das Säuglingsekzem ist gekennzeichnet durch Erythem, Papeln, Vesikel, Erosion, Krusten und Schuppenbildung, bevorzugt als Milchschorf am behaarten Kopf und im Gesicht und sonst vorwiegend an den Streckseiten der Extremitäten. Im Kindesalter kommt es eher zu entzündlichem Befall von Gesicht, Hals, Nacken, Gelenkbeugen, Brustbereich, Hand- und Fußrücken.
Im Erwachsenenalter sind typischerweise die Gelenkbeugen betroffen. Das klinisch Bild reicht von einer ausgeprägten Entzündung der gesamten Haut (Erythrodermie), bis zum chronischen Ekzem, bei dem die Lichenifikation (Verdickung der Haut mit Vergröberung der Hautstruktur, ▶ Abb. 40.23) im Vordergrund steht; daneben können auch Knoten am Stamm und an den Extremitäten mit sehr ausgeprägtem Juckreiz charakteristisch sein. Zur Bestimmung des Schweregrades werden Haut-Scores verwendet (SCORAD – Scoring Atopic Dermatitis Index), EASI (Eczema Area and Severity Index).
Durch hautbelastende Tätigkeiten wie z.B. Feuchtarbeit oder Händedesinfektion kommt es gehäuft zu Handekzemen. Empfohlen wird, dass Patienten mit Neurodermitis bei der Berufswahl auf die Meidung hautirritierender Expositionen achten.
Lichenifikation.
Abb. 40.23 Verdickte und vergröberte Hautstruktur mit Rötung bei Neurodermitis.

40.9.4.4 Diagnostik
Als Zeichen der atopischen Hautdisposition bzw. Minimalvarianten der Neurodermitis gelten eine Verminderung der seitlichen Augenbrauen (Hertoghe-Zeichen), eine doppelte Lidfalte, Ohrrhagaden, eingerissene Mundwinkel, Pityriasis alba (hypopigmentierte Flecken bei latenter Hautentzündung), verstärkte Handlinienbildung sowie eine Verhornungsstörung der Haarfollikel, die sog. Reibeisen-Haut. Infektionen der Haut stellen häufige Komplikationen dar; neben bakteriellen Infektionen muss auch auf virale Infektionen (Eczema herpeticatum (Herpesviren), Dellwarzen (Mollusca contagiosa) und Pilzerkrankungen geachtet werden. Da viele Patienten unter Soforttyp-Allergien leiden, wird in Abhängigkeit von der Anamnese ein Pricktest und/oder die Bestimmung von spezifischen IgE-Antikörpern empfohlen.
40.9.4.5 Therapie
Als Basisbehandlung gilt bei jedem Schweregrad die Meidung oder Reduktion von Triggerfaktoren (Meidung intensiver austrocknender Waschprozeduren, Verwendung geeigneter Kleidung – Schwitzen und der Kontakt mit Wolle fördert Juckreiz) neben der topischen Basistherapie.
Die antientzündliche Behandlung richtet sich nach dem Schweregrad. Prinzipiell können zur Entzündungshemmung Glukokortikosteroide und topische Immunmodulatoren eingesetzt werden. UV-Therapie und systemische Immunmodulatoren sind bei ausgeprägten Ekzemen indiziert. Juckreiz wird durch adäquate Behandlung des Ekzems reduziert, Antihistaminika können in Kombination mit der topischen Therapie gegen Juckreiz eingesetzt werden. Bei Hautinfektionen kann man die Keimbesiedlung durch Antiseptika reduzieren.
Die Verwendung der unterschiedlichen therapeutischen Zubereitungen hängt vom Hautzustand ab. Im akuten Stadium werden bei akuter Entzündung feuchte Umschläge und fettarme Externa (Öl-in-Wasser-Emulsion) angewandt, bei chronischer Entzündung fettreichere Externa (Wasser-in-Öl-Emulsion, Salben). Zur Rückfettung der Haut können Ölbäder hilfreich sein.
Fallbeispiel
Zur stationären Aufnahme kommt eine 18-jährige Patientin, die in der Kindheit unter Milchschorf litt, später unter juckenden Ekzemen hauptsächlich im Bereich der Ellenbeugen und Kniekehlen. Jetzt kam es im Rahmen von Prüfungsstress zu einer Verschlechterung der Hauterkrankung. Die gesamte Haut ist gerötet, trocken und schuppig, es finden sich multiple Exkoriationen. Die Patientin leidet unter ausgeprägten Schlafstörungen aufgrund des Juckreizes. Zuletzt hat sie topische Glukokortikosteroide zur Behandlung verwendet.
40.9.5 Pflege- und Behandlungsplan
40.9.5.1 Zur topischen Therapie anleiten
Patienten wird das Wissen vermittelt, dass im akuten Stadium die Entzündungshemmung mit topischen Glukokortikosteroiden oder topischen Calcineurin-Inhibitoren im Vordergrund steht; bei sehr starker Entzündung der Haut kann auch eine Kurzzeittherapie mit oralen Glukokortikosteroiden zur Unterbrechung des akuten Schubes sinnvoll sein. Der Patientin muss die Angst vor Glukokortikosteroiden (Steroidphobie) genommen werden. Für Problemareale wie dem Gesicht, können wegen der Gefahr der Hautatrophie Calcineurin-Inhibitoren (2-mal täglich) als First-Line-Therapie empfohlen werden. Bei Infektion der Haut sind Umschläge hilfreich. Dazu werden Kompressen in Antiseptika-Lösungen getaucht, ausgewrungen und auf betroffene Areale aufgelegt und wiederholt befeuchtet. Im späteren Stadium sind zunächst fettarme, kühlende Cremes hilfreich, Salben nur bei im Vordergrund stehender trockener Haut und Schuppung. Mehrfaches Eincremen pro Tag ist i. d. R. günstiger als einmalige Therapie mit zu fettreichen Lokaltherapeutika.
40.9.5.2 Gesundheitsberatung
In Gesprächen lassen sich Stress auslösende Situationen abklären; ggf. muss darauf hingewirkt werden, dass Patienten professionelle psychologische Betreuung akzeptieren. Informationen über auslösende Faktoren wie Schwitzen (Juckreizerzeugung durch Schwitzen und ungeeignete Kleidung – z.B. Wolle) müssen vermittelt werden. Hinweise auf Typ-I-Allergien (Nahrungsmittel, Aeroallergene) sind im Gespräch abzuklären.
40.9.6 Medizinischer Überblick Psoriasis
40.9.6.1 Definition
Die Psoriasis (Schuppenflechte) ist eine entzündliche Hauterkrankung. Unter klinischen Gesichtspunkten werden die pustulöse und die Plaque-Typ-Psoriasis (Psoriasis vulgaris) unterschieden. Eine Beteiligung der Gelenke (Psoriasis-Arthritis) ist möglich. Neben der genetischen Prädisposition spielen epigenetische Faktoren und Umwelteinflüsse eine Rolle.
Häufigkeit Die Psoriasis ist eine häufige Erkrankung mit einer Morbidität von 1 – 2 %.
40.9.6.2 Ursachen
Die Psoriasis ist eine genetisch fixierte (erbliche) Erkrankung. Eine Aktivierung des angeborenen Immunsystems führt zur Aktivierung spezifischer T-Zellen, die in die Haut einwandern und entzündungsfördernde Botenstoffe freisetzen. Entzündungsfaktoren stimulieren auch die Proliferation von Keratinozyten, die Epidermis erneuert sich in <10 Tagen (normal sind 25 – 29 Tage); daher die starke Schuppung.
Provokationsfaktoren sind bakterielle Infektionen (insbesondere Tonsillitis mit β-hämolysierenden Streptokokken der Gruppe A), Medikamente wie Betablocker und Lithium, Alkohol, Stress, aber auch eine Schädigung der Epidermis z. B. durch Kratzen oder Sonnenbrand. Übergewicht fördert eine Entzündung und stellt ebenso wie das Rauchen einen Triggerfaktor für Schuppenflechte dar.
40.9.6.3 Symptome
Klinisch bestehen bei der Psoriasis vulgaris erythematosquamöse Plaques (rötliche, schuppige, flach erhabene Hautveränderungen) besonders an den Streckseiten der Gelenke. Auch Kopfhaut, Rumpf und Gehörgänge sind häufig betroffen. Die Herde jucken häufig. Besondere Manifestationsorte sind die Finger- und Fußnägel ( ▶ Abb. 40.24). Auch intertriginöse Bereiche (Achseln, Genitalbereich, Bauchnabel, Analfalte) können betroffen sein. Bei den pustulösen Formen kann es zur generalisierten Aussaat von kleinen sterilen Pusteln kommen, bei anderen Formen sind überwiegend die Handinnenflächen und Fußsohlen betroffen.
Zur Berechnung des Ausmaßes der Hauterscheinungen wird häufig der PASI (Psoriasis Area and Severity Index) bestimmt. Psoriasis wird heute als systemische Erkrankung aufgefasst, möglich ist eine Gelenkbeteiligung; Komorbiditäten sind zu beachten. Gehäuft sind Patienten von entzündlichen Darmerkrankungen, Fettstoffwechselstörungen, Diabetesneigung und arterieller Hypertonie betroffen. Es besteht ein erhöhtes Risiko für kardiovaskuläre Folgeerkrankungen wie Herzinfarkt und Schlaganfall.
Psoriasis vulgaris.
Abb. 40.24
(Foto: K. Oborny, Thieme)
40.9.6.4 Diagnostik und Therapie
Die Diagnose lässt sich i. d. R. aufgrund des klinischen Befundes stellen.
Zur Behandlung können zunächst keratolytische Externa mit „abschuppender“ Wirkung zur Anwendung kommen. Verwendet werden Harnstoff, Milchsäure und häufig Salizylsäure in Vaseline (Cave: Bei großflächiger Anwendung Systemwirkung durch Resorption von Salizylsäure, insbesondere Vergiftungen bei Kindern möglich).
Auch Emulgatoren in Externa (z.B. Unguentum emulsificans aquosum) lösen Schuppen, verwendet werden auch Externa mit Dimeticone.
-
Topische Glukokortikosteroide wirken antientzündlich, haben aber keinen Dauereffekt.
-
Vitamin-D-ähnliche Substanzen (z. B. Calcipotriol) wirken anti-proliferativ und topisch immunsuppressiv.
-
Topische Vitamin-A-Säure-ähnliche Substanzen wirken ebenfalls anti-proliferativ.
-
Cignolin zeigt eine gute Wirkung bei längerfristiger Therapie, wird aber nur noch selten angewendet. Die Substanz riecht unangenehm und verfärbt Kleidung und selbst Badewanne und Dusche.
-
UV-Therapie, insbesondere UVB und PUVA (Photochemotherapie)
-
Fumarsäureester beeinflussen die T-Zell-Aktivierung.
-
Retinoide (Vitamin-A Abkömmlinge) wirken anti-proliferativ.
-
MTX (Methotrexat) und Ciclosporin als Zytostatika bei schweren Formen und Gelenkbeteiligung
-
Biologicals sind spezielle Antikörper und Proteine, die sich gegen Entzündungszellen oder spezielle Zytokine richten.
Fallbeispiel
Zur stationären Aufnahme kommt ein 26-jähriger Patient mit seit Jahren bestehender Psoriasis. In der Familie leiden der Vater und ein Bruder ebenfalls an der Erkrankung. Es finden sich auf der gesamten Haut bis zu 20 cm große erythematosquamöse Plaques mit weißlicher, fest haftender Schuppung, auch im Bereich der behaarten Kopfhaut. Perianal ist die Haut gerötet und mazeriert, hier finden sich schmerzhafte Rhagaden. Der Patient klagt über deutlichen Juckreiz. Früher wurden mehrfach Behandlungen mit Dithranol (Cignolin) durchgeführt. Im vergangenen Jahr wurde die Hauterkrankung mit selektiver UVB-Bestrahlung erfolgreich behandelt. Zuletzt hat er verschiedene Salben, auch topische Glukokortikosteroide verwendet, die ausgeprägte Schuppenbildung ist er mit einer Bürste angegangen.
40.9.7 Pflege- und Behandlungsplan
Nach Ablösen der Schuppung mittels Salizylvaseline (Salizylsäure in Vaselinum album oder Dimeticone) wird eine UV-Behandlung begonnen. Topisch wird Calcipotriol und ein Glukokortikosteroid über 14 Tage verwendet. Die Kopfhaut wird mit Salizylsäure in einer abwaschbaren Salbengrundlage oder alternativ mit Ung. emuls. aquosum oder ebenfalls Dimeticone entschuppt; weiter wird zunächst mit einem Kombinationspräparat (Calcipotriol plus Betamethason) therapiert.
40.9.7.1 Zur angepassten Hautpflege anleiten
Nach Baden oder Duschen soll die Haut mit einem weichen Handtuch vorsichtig abgetrocknet werden, um eine zusätzliche Reizung zu vermeiden. Anschließend trägt man ein geeignetes Hautpflegepräparat auf, z. B. harnstoffhaltige Externa. Zu fettige Salben können ungünstig wirken; wichtig ist die Auswahl eines individuell verträglichen und als angenehm empfundenen Präparates.
Schuppen können durch Keratolytika (Salizylsäurehaltige Externa, Ung. emuls. aquosum oder Dimeticone) abgelöst werden. Die mechanische Schuppenablösung mit Bürste, Bimsstein usw. ist strikt zu unterlassen. Auch Schuppung im Bereich der Kopfhaut wird mit keratinolytischen Externa abgelöst und mit speziellen Shampoos ausgewaschen.
Die Behandlung der Haut mit Externa erfolgt prinzipiell nach der UV-Therapie. Durch Lichteinstrahlung können Inhaltsstoffe der Salbe zerstört werden, zudem wird das Eindringen der Strahlen in die Haut durch Salbenbestandteile verhindert und die Behandlung ist damit weniger wirksam.
Haut auf Haut und Feuchtigkeit in intertriginösen Bereichen verstärkt Schuppenflechte. Daher wird der Patient zum Einlegen von Kompressen angeleitet. Die Haut in der Umgebung des Afters wird nach dem Stuhlgang intensiv gereinigt, Zinkpaste kann zum Hautschutz aufgetragen werden. Sitzbäder mit Gerbstoffen wirken entzündungshemmend.
40.9.7.2 Gesundheitsberatung
Informieren Sie den Patienten über juckreizverstärkende Faktoren (Stress, Alkohol und mechanische Hautreizung) und den Kontakt mit hautreizenden Substanzen. Lindernd können spezielle Externa wirken (z. B. mit Menthol, Polidocanol oder Harnstoff). Auch Entspannungstechniken können hilfreich sein. Informationen über das Auslösen von Schuppenflechte durch Reizung (Köbner-Phänomen) sind unerlässlich. Sowohl mechanische Reizung, z. B. durch Kratzen, aber auch Sonnenbrand, Verbrennungen usw. können Psoriasisschübe/-herde auslösen.
Da die Erkrankung als Systemerkrankung aufgefasst wird und Komorbiditäten eine große Rolle spielen, wird bei übergewichtigen Patienten die Gewichtsabnahme propagiert. Gegebenenfalls wird eine Rauchentwöhnung angeraten. Beachtet werden muss das erhöhte Risiko für kardiovaskuläre Erkrankungen, auch psychische Probleme sind zu thematisieren.
40.9.8 Medizinischer Überblick primäre Pyodermien
40.9.8.1 Definition
Primäre Pyodermien sind bakterielle Infektionen (meist Staphylokokken und Streptokokken). Sekundäre Hautinfektionen, die eine Komplikation von z. B. Verletzungen, Verbrennungen, Ekzemen und Geschwüren darstellen, sind abzugrenzen.
40.9.9 Medizinischer Überblick Impetigo contagiosa
40.9.9.1 Definition
Die Impetigo contagiosa ist eine hoch ansteckende, oberflächliche Hautinfektion, die besonders bei Kindern auftritt.
40.9.9.2 Ursachen
Die kleinblasige Form der Erkrankung wird meist durch hämolysierende Streptokokken, die großblasige eher durch Staphylococcus aureus verursacht. Die Infektion wird durch Kratzen und Reiben auf andere Körperstellen übertragen. Epidemisches Auftreten in Kindergärten und Schulklassen ist möglich.
40.9.9.3 Symptome
Kennzeichnend sind zunächst Flecken, auf denen Bläschen mit klarem, gelblichem Inhalt entstehen. Die Bläschendecke ist dünn und kann relativ schnell platzen. Durch Eintrocknen der austretenden Gewebsflüssigkeit entstehen typische honiggelbe Krusten ( ▶ Abb. 40.25). Bei der großblasigen Form entstehen aus schlaffen Blasen eher gerötete, erosive, feucht wirkende Läsionen.
Infektion mit Impetigo contagiosa beim Kind mit Rötungen und Krusten.
Abb. 40.25

40.9.9.4 Komplikationen
Hier können eitrige Augenentzündungen, Otitis media und bei Auslösung durch Streptokokken auch Nierenentzündungen (Poststreptokokken-Nephritis) oder immunbedingte Gefäßentzündungen (Purpura Schoenlein-Henoch) auftreten.
40.9.9.5 Diagnostik
Die Diagnose wird aufgrund der typischen Hautveränderungen gestellt. Die Bakterienidentifikation erfolgt durch bakteriologischen Abstrich.
40.9.9.6 Therapie
Sie geschieht systemisch mit Antibiotika. Lokal kommen antiseptische Umschläge zum Einsatz, ausgeprägte Verkrustungen können durch Salben aufgeweicht werden.
Merke
Die Impetigo contagiosa ist eine relativ häufige bakterielle Infektionserkrankung bei Kindern, die hoch ansteckend ist. Sie erfordert striktes Tragen von Handschuhen und Händedesinfektion!
40.9.10 Medizinischer Überblick Erysipel (Wundrose)
40.9.10.1 Definition
Das Erysipel ist eine meist durch β-hämolysierende Streptokokken ausgelöste akute, flächenhafte Infektion der Haut.
40.9.10.2 Ursachen
Bakterien treten durch kleine Hautverletzungen, aber auch durch Mazerationen im Bereich der Zehenzwischenräume bei Fußpilz in die Haut ein.
40.9.10.3 Symptome
Typischerweise kommt es einseitig z. B. am Bein oder im Gesicht, zu einer rasch auftretenden, scharf begrenzten, flammenden Rötung ( ▶ Abb. 40.26). Die Haut ist überwärmt und druckschmerzhaft, insbesondere an den Extremitäten tritt ein deutliches Ödem auf. Das betroffene Hautareal kann sich rasch vergrößern, Bläschen, größere Blasen und auch Nekrosen können auftreten. Der Patient fühlt sich abgeschlagen und krank, er hat Schüttelfrost und Fieber.
Erysipel.
Abb. 40.26 Ein Hautpilz im Zwischenzehenraum diente als Eintrittspforte für die Bakterien.
(Foto: Thieme Verlagsgruppe)
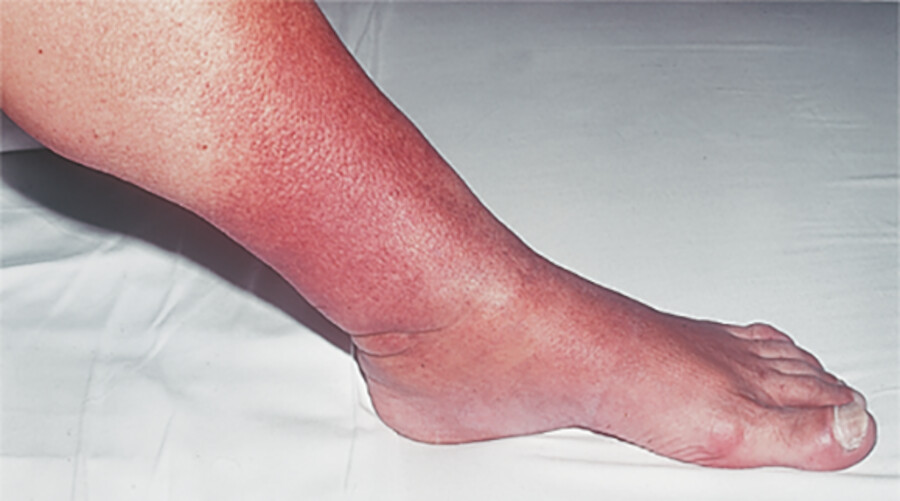
40.9.10.4 Komplikationen
Hier muss bei chronisch-rezidivierendem Verlauf mit einem Lymphödem gerechnet werden. Als Streptokokkenfolgeerkrankungen sind insbesondere Nierenentzündungen (Poststreptokokken-Nephritis) sowie Entzündungen am Herzen (Endokarditis und Perikarditis) zu nennen.
40.9.10.5 Diagnostik und Therapie
Die Diagnose wird klinisch gestellt, Leukozyten und Entzündungsparameter wie CRP und Blutsenkungsgeschwindigkeit sind erhöht. Eine Abstrichdiagnostik ist nicht hilfreich, da die sich in der Haut ausbreitenden Bakterien nicht erfasst werden.
Eine hoch dosierte intravenöse Antibiotikabehandlung (z. B. Penicillin, Cephalosporin, ggf. auch Makrolide oder Clindamycin) ist unerlässlich. Topisch werden zusätzlich antiseptische Umschläge angewandt. Weitere Maßnahmen sind Bettruhe und Ruhigstellung des betroffenen Körperabschnitts, bei einem Erysipel im Gesicht Sprechverbot und flüssige Kost. Eintrittspforten müssen konsequent saniert werden. Bei anhaltendem Ödem kommen nach Abheilung der akuten Phase Lymphdrainage und Kompressionsverbände zur Anwendung.
40.9.11 Pflege- und Behandlungsplan
Pflegende haben folgende Aufgaben:
-
Anleitung des Patienten zur Durchführung antiseptischer Umschläge
-
regelmäßige Kontrolle der Ausbreitung der Hautentzündung, ggf. Markierung des Randes
-
Bettruhe und ggf. Hochlagerung der betroffenen Körperpartie
-
Kontrolle von Temperatur und Kreislaufparametern
-
nach Abklingen der Infektion ggf. Anlegen von Kompressionsverbänden
-
Behandlung der Eintrittspforte, z. B. Versorgung der Zehenzwischenräume mit einem Antimykotikum
-
gegebenenfalls Thromboseprophylaxe
Merke
Infolge kleiner Verletzungen können Bakterien in die Haut eindringen und eine akute Entzündung der Haut auslösen. Auf die Sanierung der Eintrittspforte muss geachtet werden, ein Lymphödem kann Folge eines chronisch-rezidivierenden Erysipels sein.
40.10 Pflege von Patienten mit Verbrennungen
40.10.1 Medizinischer Überblick
Bei einer Verbrennung führen thermische, elektrische oder chemische Unfälle zu Verletzungen der Haut. Eine Schädigung der Haut geschieht bei einer Temperatur von mehr als 52 °C.
Häufigkeit Brandverletzungen zählen neben Autounfällen zu den häufigsten Unfallgeschehen weltweit. Die Dunkelziffer, meist mit Bagatellverletzungen, ist relativ hoch.
40.10.1.1 Ursachen
Ursachen für die Verletzungen sind Flammenverbrennungen, Verbrühungen, Explosionen, Kontaktverbrennungen (Herdplatte), elektrische, chemische und aktinische (Radioaktivität, Strahlung) Verbrennungen ( ▶ Abb. 40.27).
Verbrennungen Grad 2a–2b am Unterarm.
Abb. 40.27
(Abb. von: BGU-Tübingen)
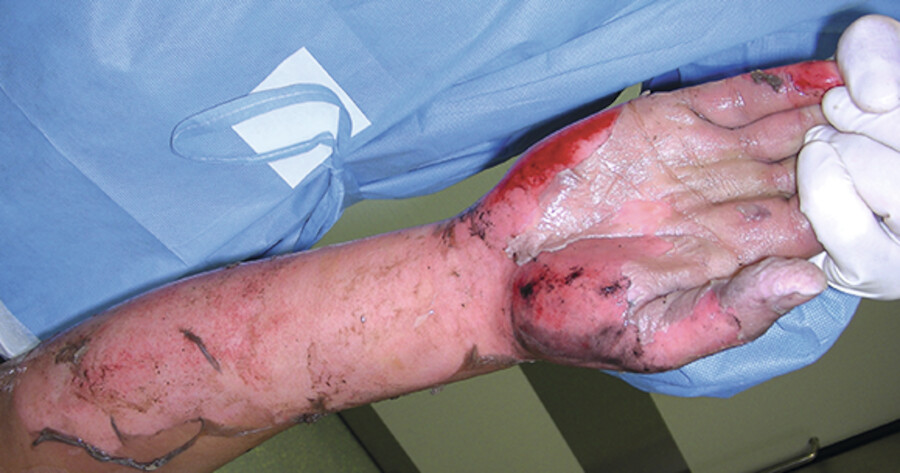
40.10.1.2 Symptome
Als Symptome werden die Verletzung der Haut in unterschiedlicher Tiefe ( ▶ Tab. 40.2 ), der Verbrennungsschock und im weiteren Verlauf die Verbrennungskrankheit gefasst.
|
Verbrennungsgrad |
Symptomatik |
Lokalisation |
Besonderheit |
|
1. Grades |
Rötung, Sonnenbrand, Schwellung durch reaktives Ödem |
Obere Epidermis |
schmerzhaft |
|
2 a. Grades |
Rötung, Blasenbildung, feuchter Wundgrund |
Epidermis, teils Corium |
sehr schmerzhaft |
|
2 b. Grades |
Blasen zerrissen, weißlicher Wundgrund |
Epidermis, teils Corium |
weniger schmerzhaft, Haare und Nägel bleiben fest |
|
3. Grades |
Nekrose, weißgrauer Wundgrund, lederartig |
Epidermis und Corium zerstört |
schmerzfrei, Haare und Nägel fallen aus |
Verbrennungstiefe
Bisher gibt es kein zuverlässiges Verfahren, um die Verbrennungstiefe ( ▶ Abb. 40.28) zu messen. Deshalb erfolgt die Einschätzung durch das geschulte Auge. Symptome und Merkmale sind in ▶ Tab. 40.2 aufgeführt.
Unterschiedliche Verbrennungstiefen in der schematischen Darstellung.
Abb. 40.28
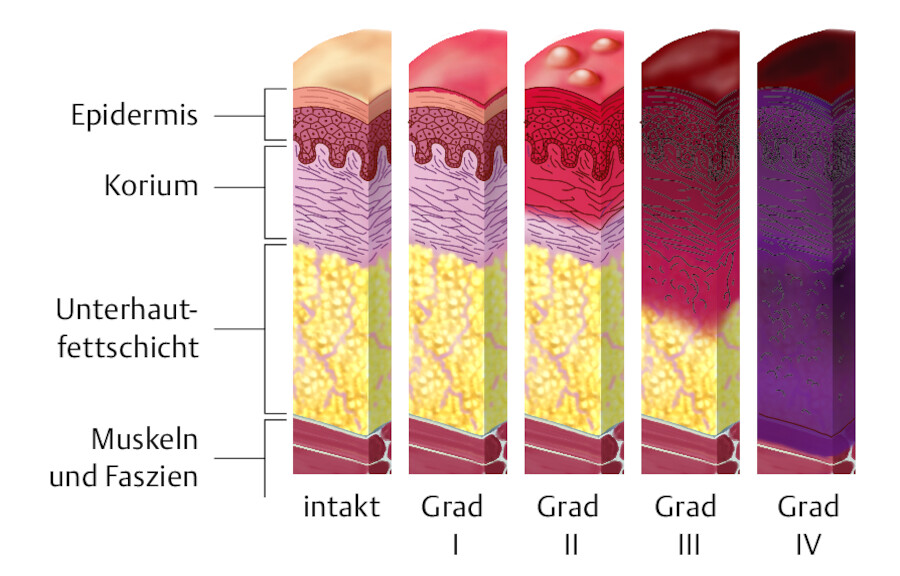
Merke
Drittgradige Verbrennungen sind schmerzfrei, denn die in der Epidermis und Dermis liegenden Nervenfasern wurden zerstört!
Verbrennungsausmaß und -schwere
Das Ausmaß einer Verbrennung wird mit der Neuner-Regel nach Wallace berechnet. Ein betroffener Arm nimmt z. B. 9 % ein, der Rücken 18 %. Ein Bein vorne und hinten je 9 %, gesamt also 18 % ( ▶ Abb. 40.29). Eine einfache Regel für den Laien am Unfallort ist die 1-%-Regel. Die Handfläche des Verletzten (nicht die eigene!) entspricht einem Prozent der Körperoberfläche.
Neunerregel nach Wallace.
Abb. 40.29 a Ganz exakt trifft sie nur auf Erwachsene zu, b Kinder haben einen größeren Kopf und kürzere Beine. Für das Genitale wird 1 % berechnet.
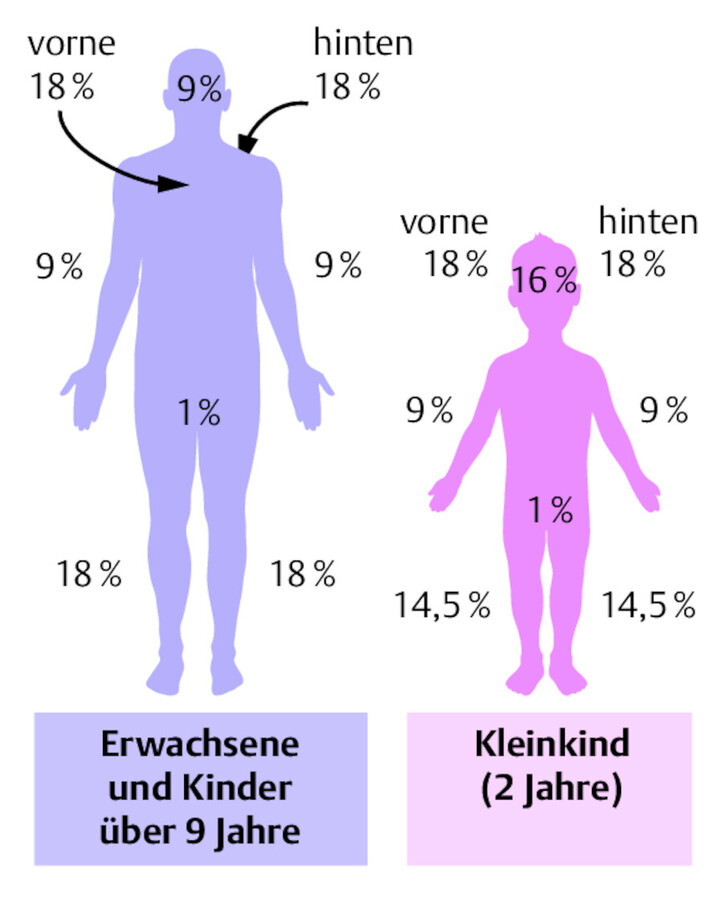
Die Verbrennungsschwere wird nach dem Verbrennungsindex (ABSI-Score nach Tobiasen) berechnet. Dabei werden verschiedenen Parametern (z. B. Alter, verbrannte Körperoberfläche, Verbrennungstiefe) Punktwerte zugeordnet. Die Summe der Punkte lässt Aussagen über die Prognose zu; je höher die Summe, desto höher das Sterblichkeitsrisiko.
Verbrennungskrankheit
Bei ausgedehnten Verbrennungen kommt es durch das thermische Trauma zur Verbrennungskrankheit. Dies ist ein eigengesetzliches schweres Krankheitsbild, welches im weiteren Verlauf Schäden an allen Organen oder Organsystemen auslöst. Der genaue Entstehungsmechanismus ist bis heute nicht bekannt. Die Schwere der Verbrennungskrankheit ergibt sich aus Verbrennungsausmaß, -bezirk und -tiefe, dem Lebensalter und den evtl. Begleitverletzungen bzw. -erkrankungen. Gekennzeichnet ist die Verbrennungskrankheit durch einen typischen Verlauf in 3 Phasen.
1. Verbrennungsschock Über die Verbrennungswunde verliert der Körper am 1.– 3. Tag Flüssigkeit (Exsudat). Zusätzlich verdunstet mehr Wasser über die verbrannte Haut (Evaporation). Daneben treten Wasser, Elektrolyte und Plasmaeiweiß aus dem Blutgefäßsystem in das umgebende Gewebe über. Das so entstehende Verbrennungsödem befällt nicht nur die Verletzungsareale, sondern den gesamten Körper und alle Organe. Die Folge ist ein hoher Flüssigkeitsverlust, der unbehandelt zu einem Volumenmangelschock führt.
2. Resorptionsphase Nach frühestens 24 Std. stoppt der massive Flüssigkeitsverlust und das Ödem wird – medikamentös durch Diuretika unterstützt – rückresorbiert. Die Flüssigkeitszufuhr gegenüber dem ersten Tag wird deutlich reduziert. Es erfolgt eine Flüssigkeitsbilanzierung, bei der die Evaporation und das Exsudat mit berechnet werden müssen. Das fehlende Eiweiß und die Elektrolyte, die über die Wunde weiter verlorengehen, müssen ersetzt werden. Diese Phase dauert vom 2. bis zum 8. Tag.
3. Verbrennungskrankheit Diese dauert ca. vom 8. Tag bis zur Wundheilung. Wache Patienten fühlen sich kraftlos, antriebsarm, appetitlos und haben ein ausgeprägtes Krankheitsgefühl. Klinisch erkennt man eine Tachykardie, gesteigerte Ventilation, vermehrten Sauerstoffverbrauch, Fieber und Gewichtsabnahme. Ursache ist ein gesteigerter Stoffwechsel, der bei allen Brandverletzten eintritt. Der Körper versucht mit diesem Hypermetabolismus den Wärmeverlust auszugleichen. Eine andere Ursache ist die erhöhte Katecholaminausschüttung, die bei ausgeprägten Verbrennungsverletzungen nachgewiesen wurde.
Merke
Eine Verbrennungswunde wird unweigerlich mit Keimen besiedelt und Infektionen treten auf. Da die Immunabwehr bei Brandverletzten gesenkt ist, können diese Infektionen bis zur Sepsis führen. Dies ist immer noch eine der häufigsten Todesursachen in der Verbrennungsbehandlung.
Inhalationstrauma
Das Einatmen von heißen Gasen und die Schädigung des Respirationstraktes werden als Inhalationstrauma bezeichnet. Neben der toxischen Zerstörung der Alveolen durch Rauchgas (z. B. Kohlenmonoxyd) treten thermische Schäden der Trachealschleimhaut mit Rötungen, Ödemen, Hypersekretionen, Ischämien und Nekrosen auf. Der Verdacht auf ein Inhalationstrauma liegt immer vor bei:
-
Verbrennungsunfall in geschlossenen Räumen
-
Gesichtsverbrennungen
-
Ruß im Nasen-Rachen-Raum (versengte Nasenhaare)
-
Heiserkeit
Schon bei dem Verdacht auf ein Inhalationstrauma ist die frühzeitige Intubation das Mittel der Wahl. Neben der Gefahr eines toxischen Lungenödems besteht zusätzlich die Gefahr, dass sich wie an der Verbrennungswunde ein Ödem bildet und somit eine spätere Intubation nur unter Schwierigkeiten möglich ist. Die Prognose eines Schwerstbrandverletzten mit Inhalationstrauma verschlechtert sich gravierend.
Merke
Ein Brandverletzter ist primär ansprechbar. Bewusstlosigkeit spricht immer für eine Rauchgasvergiftung oder eine Begleitverletzung (z. B. Schädel-Hirn-Trauma)!
40.10.1.3 Therapie
Sie gliedert sich in Erstversorgung am Unfallort, stationäre Aufnahme und Verbrennungsbehandlung.
Erstversorgung
Erste-Hilfe-Maßnahmen durch den Laien Dazu gehören:
-
brennende Kleidung mit Decken, Kleidungsstücken oder durch Wälzen auf dem Boden löschen
-
Verletzten aus dem Gefahrenbereich ziehen
-
Feuerwehr, Rettungsdienst alarmieren
-
schwelende Kleidung mit Wasser löschen
-
Kleidung entfernen
-
auf der Haut klebende Kleidung belassen
-
sofortiges Kühlen mit lauwarmem Wasser zur Schmerztherapie – nicht bei großflächiger Verbrennung oder bewusstlosen Patienten. Gefahr der Unterkühlung!
-
zum Transport Wunden steril abdecken
Erstversorgung durch den Notarzt Diese umfasst:
-
Legen großlumiger venöser Zugänge
-
Gabe von Elektrolytlösung oder Ringerlaktat
-
Analgosedierung
-
frühzeitige Intubation
-
steriles Abdecken von Wunden
Die Volumentherapie richtet sich heute fast einheitlich nach der Baxter-Formel. Für Erwachsene gilt:
4 ml Ringerlaktat × % verbrannte Körperoberfläche (VKOF) × kg Körpergewicht
Davon wird die Hälfte in den ersten 8 Stunden gegeben, der Rest in den nachfolgenden 16 Stunden. Für einen 80 kg schweren Patienten mit 60 % verbrannter KOF bedeutet dies 19 200 ml Ringerlaktat (innerklinisch Jono 1/1) in den ersten 24 Stunden.
Stationäre Aufnahme
Indikationen zur stationären Aufnahme in einem Brandverletztenzentrum sind (nach den Leitlinien der Deutschen Gesellschaft für Verbrennungsmedizin 2010):
-
Patienten mit Verbrennungen an Gesicht/Hals, Händen, Füßen, Anogenital, Achselhöhlen, Bereichen über großen Gelenken oder sonstiger komplizierter Lokalisation
-
Patienten mit mehr als 15 % zweitgradiger verbrannter Körperoberfläche
-
Patienten mit mehr als 10 % drittgradiger verbrannter Körperoberfläche
-
Patienten mit mechanischen Begleitverletzungen
-
Patienten mit Inhalationstrauma
-
Patienten mit Vorerkrankungen oder Alter unter 8 bzw. über 60 Jahre
-
Patienten mit Verletzungen durch Elektrizität
Merke
In ganz Deutschland gibt es 36 Zentren mit insgesamt 171 Betten für Brandverletzte mit ca. 44 Betten nur für Kinder. Die Feuerwehr Hamburg ist die zentrale Anlaufstelle für die Vermittlung von Betten für Schwerbrandverletzte.
Stationäre Erstversorgung In den Zentren werden die Patienten in einem speziellen Aufnahmeraum erstversorgt. Dieser Raum hat eine Duschmöglichkeit für den Patienten, ist klimatisiert und hat eine Raumtemperatur von 35 – 40 °C. Hier wird unter sterilen Bedingungen gearbeitet. Zur Erstversorgung in einem Brandverletztenzentrum gehören folgende Maßnahmen:
-
Sicherung von Atmung und Kreislauf
-
Weiterführung der Analgesie und Sedierung
-
Festlegung von Verbrennungsausmaß und -tiefe
-
Berechnung des Flüssigkeitsbedarfs
-
Anlage eines Blasenkatheters
-
Abstriche aller Verbrennungsareale zum Bakteriennachweis
-
Reinigung und Desinfektion des gesamten Körpers mit Rasur und Abtragung der Verbrennungsblasen, kleine Blasen werden als Infektionsprophylaxe nur eröffnet, Wunddebridement
-
evtl. Escharotomie (Entlastungsschnitte zur Durchtrennung der Nekrose)
-
Wundverband
-
evtl. Bronchoskopie zum Ausschluss eines Inhalationstraumas
-
kontinuierliche Überwachung von Kreislaufsituation, Atmung und Urinausscheidung
-
Tetanusprophylaxe
Merke
Bei drittgradigen Verbrennungen ist die Nekrose nicht mehr dehnungsfähig. Bei zirkulären, tiefen Verbrennungen können durch das entstehende Verbrennungsödem die arterielle Blutversorgung bzw. (bei drittgradigen Verbrennungen des Thorax) die Atmung stark beeinträchtigt werden. Deshalb müssen Entlastungsschnitte (Escharotomie) durchgeführt werden. Dabei wird lediglich die Nekrose durchtrennt.
Verbrennungsbehandlung
Zur lokalen Behandlung der Verbrennungswunde, die sich nach der Verbrennungstiefe richtet, gehören Nekrosenabtragung und Wundverschluss. ▶ Tab. 40.3 gibt Aufschluss über Behandlungsmöglichkeiten und die ungefähre Dauer der Wundheilung.
|
Verbrennungsgrad |
Behandlung |
Abheilung |
|
1. Grades |
kühlende Gels oder Lotionen |
spontan, nach ca. 3 Tagen ohne Narben |
|
2 a. Grades |
Polyhexanid-basiertes Antiseptikum, Fettgaze, Hautersatzmaterial |
nach ca. 7 – 10 Tagen spontan, ohne Narben |
|
2 b. Grades |
Polyhexanid-basiertes Antiseptikum, Hautersatzmaterial, Fettgaze |
unter Narbenbildung nach ca. 2 – 3 Wochen, evtl. ist eine Hauttransplantation nötig |
|
3. Grades |
Fettgaze bis zur operativen Versorgung |
immer mit Narbenbildung, Defektverschluss nur mit Hauttransplantation möglich |
Nekrosenabtragung
Die Verbrennungsnekrose ist ein idealer Nährboden für Keime; in ihr entstehen Toxine, die auch gesunde Zellen zerstören. Aus diesem Grunde ist die Frühexzision heute das Mittel der Wahl. Ab dem dritten Behandlungstag beginnt die eigentliche operative Lokalbehandlung mit der Abtragung der Nekrosen. Dazu gibt es zwei Methoden:
-
tangentiale Abtragung: Abtragung bis auf den durchbluteten Wundgrund bei tief zweitgradigen Verbrennungen (kosmetisch günstigere Variante)
-
epifasziale Abtragung: Abtragung bis auf die Muskelfaszie bei tief drittgradigen Verbrennungen
Wundverschluss
Hierzu stehen Transplantate aus Spalt- und Zuchthaut sowie Hautersatzmittel zur Verfügung. Ein bleibender Wundverschluss ist nur mit Eigenhaut möglich.
Spalthaut Eigenhauttransplantate werden an unverletzten Hautpartien in einer Dicke von 0,2 – 0,3 mm entnommen. Diese sog. Spalthaut kann direkt als Transplantat verwendet werden. Um größere Defekte abzudecken, wird sie vor dem Auflegen „gemesht“ (= Herstellung eines rautenförmigen Spalthauttransplantats, das stark auseinander gezogen werden kann). Die Netzstruktur des Transplantates ist bleibend zu erkennen ( ▶ Abb. 40.30) und eignet sich daher aus kosmetischen Gründen nicht für Gesicht oder Hände.
Transplantiertes Meshgewebe.
Abb. 40.30 An der Verbrennungswunde am rechten Unterschenkel und Fuß wird 10 Tage nach dem Unfall nekrotisches Gewebe exzidiert und autogene Spalthaut („Mesh-Graft“) transplantiert.
(Abb. von: BGU-Tübingen)

Zuchthaut Diese ermöglicht Patienten mit ausgedehnten Verbrennungen einen bleibenden Wundverschluss und damit das Überleben. Dabei wird dem Patienten ein Hautstück von 3 cm² entnommen und in einem Labor zu Keratinozyten gezüchtet. Dies dauert etwa 3 Wochen, danach kann hiermit eine Fläche von ca.1,7m² abgedeckt werden.
Hautersatzmittel Bei einer Verbrennungsfläche von mehr als 50 % der Körperoberfläche (KOF) können die nekrotischen Areale nicht sofort mit Eigenhaut abgedeckt werden. Hier kommen zum vorübergehenden Wundverschluss andere synthetische Hautersatzmittel (Epigard, Biobrane) zur Anwendung.
40.10.2 Pflege- und Behandlungsplan
Eine erfolgreiche Behandlung von Brandverletzten ist wesentlich abhängig von der Teamarbeit. Zu einem therapeutischem Team in einem Verbrennungszentrum gehören Chirurgen, Intensivmediziner, Krankenpflegepersonal, Physiotherapeuten, Ergotherapeuten, Psychologen und nicht zu vergessen Seelsorger und Angehörige.
Zu den Aufgaben der Pflege gehören:
-
Isolation
-
Wundversorgung
-
Ernährung
-
Infektionskontrolle
-
Lagerung und Mobilisation
-
Kontrakturenprophylaxe und Narbenbehandlung
40.10.2.1 Isolation
Auf einer Brandverletztenstation liegt der Patient in einem Einzelzimmer (Box) isoliert. Diese darf nur durch eine Schleuse und nur mit sterilem Kittel, Haube, Mundschutz und sterilen Handschuhen betreten werden. Die Boxentemperatur liegt meist bei 30 – 35 °C bei einer Luftfeuchtigkeit von ca. 45 %.
40.10.2.2 Wundversorgung
Sie ist eines der Hauptaufgabengebiete der pflegerischen Versorgung. Unter OP-Bedingungen dauert der tägliche Verbandwechsel u. U. zwei Stunden und mehr. Ein Verbandwechsel gliedert sich immer in die folgenden Schritte:
-
alten Verband entfernen
-
Wunde mit antiseptischer Lösung säubern
-
Nekrosen und Krusten abtragen und Wunde beurteilen
-
Gaze- bzw. Salbenverband auftragen
Da der Verbandwechsel schmerzbedingt eine hohe Belastung darstellen kann, ist für eine ausreichende Analgosedierung zu sorgen. Schmerzlos verläuft der Verbandwechsel bei Verbrennungen 2. Grades mit der Wundauflage Suprathel, da diese mit einer abdeckenden Fettgaze auf der Wunde verbleibt und nur die äußeren Mullkompressen gewechselt werden. Nach ca. 10 – 21 Tagen löst sich das Suprathel; die Wunde darunter ist verheilt.
40.10.2.3 Ernährung
Bei dem erhöhten Energiebedarf des Brandverletzten ist immer eine Kombination aus parenteraler, enteraler und später oraler Ernährung notwendig. Die Nahrung sollte kalorien- und eiweißreich sein. Zusätzlich werden Vitamine und Spurenelemente verabreicht. Ein Mangel führt zu Wundheilungsstörungen und Schwächung der Infektabwehr.
Schmerzen, Angst und Frieren erhöhen den Kalorienverbrauch. Eine geplante Pflege mit ausreichender Analgesie, einer warmen Umgebung sowie Vermeidung unnötiger Schmerzen und Ängste sind Prioritäten in der Brandverletztenpflege.
40.10.2.4 Infektionskontrolle
Der Brandverletzte ist ausgesprochen infektanfällig. Er ist gefährdet durch die eigenen Keime aus dem Gastrointestinaltrakt, den oberen Luftwegen, der unverbrannten Haut und den behaarten Körperteilen. Ein weiteres Problem sind Klinikkeime, die v.a. über das Personal auf den Patienten übertragen werden. Die Verbrennungswunde bildet einen idealen Nährboden (Wärme, Feuchte) für das Keimwachstum. Hier gilt es, sämtliche Hygienevorschriften streng zu beachten.
40.10.2.5 Positionierung und Mobilisation
Die Positionierung am ersten Behandlungstag ist auf die Ödemausbildung ausgerichtet. Alle verletzten Extremitäten werden hochgelagert; bei Gesichtsverbrennungen wird der Patient sitzend gelagert. Im weiteren Verlauf ist die zwei- bis dreistündliche Positionsveränderung des Patienten die einfachste und verletzungsgerechte Lagerung. Liegt der Verletzte zu lange auf seinen Wundflächen, kommt es zu einer Minderperfusion, Schmerzen und direktem Kontakt mit Wundsekreten. Dies bedeutet Wundheilungsstörungen und Infektionsgefahr.
Für die Weichlagerung gibt es spezielle Betten, Wechseldruck- und Quarzsandbetten. Diese Betten werden individuell eingesetzt, z. B. bei Rückenverbrennungen und nach Transplantationen. Sie bieten neben dem Effekt der Weichlagerung auch den der Wundaustrocknung. Sobald die Genesung fortschreitet, legen Pflegepersonal und Ergotherapeutin großen Wert auf die Frühmobilisation.
40.10.2.6 Kontrakturenprophylaxe und Narbenbehandlung
Die Kontrakturprophylaxe hat in der Verbrennungsbehandlung einen hohen Stellenwert. Bei spontan heilenden tieferen Verbrennungen und allen transplantierten Arealen entstehen Narben. Diese Narben schrumpfen, sodass gesunde Hautpartien der Umgebung verzogen werden und die Bewegung eingeschränkt wird. Die Physiotherapeuten, aber auch Ergotherapeuten und Pflegende arbeiten von Anfang an gegen den Narbenzug, um eine möglichst hohe Beweglichkeit der Gelenke zu erhalten.
Narben neigen auch zur Hypertrophie (überschießende Gewebebildung). Druck verändert die Narbe, hält sie geschmeidiger und flacher. Sobald die Wunden verheilt sind, wird dem Brandverletzten eine maßangefertigte Kompressionsbandage angelegt, die möglichst 24 Stunden getragen werden sollte. Dies ist so lange nötig, bis die Narben nach ca. 1 – 2 Jahren ausgereift sind.
40.10.2.7 Psychologische Betreuung
Intakte Haut bedeutet für den Menschen nicht nur Integrität, physischen und psychischen Schutz, sondern auch ungestörte Abgrenzung von der Umwelt. Beim Schwerstbrandverletzten verstärken seelische und soziale Einflüsse die ausgeprägten Schmerzerlebnisse; er hat Angst zu sterben und entstellt zu sein. Die frühe und regelmäßige psychologische und psychotherapeutische Behandlung von Brandverletzten bildet einen wesentlichen Faktor zur Vorsorge gegen seelische und soziale Langzeitschäden.
40.11 Lern- und Leseservice
40.11.1 Literatur
40.11.1.1 Augenerkrankungen
[1992] Bowling B. Kanski’s Clinical Opthamology. A Systematic Approach. Eighth Edition. Edinburgh: Elsevier; 2016
[1993] Burk A, Burk R. Checkliste Augenheilkunde. 5. Aufl. Stuttgart: Thieme; 2014
[1994] European Glaucoma Society: Terminology and Guidelines for Glaucoma. 4. Aufl. Savona: Dogma; 2014
[1995] Oestreicher E, Burk A, Burk R. HNO, Augenheilkunde, Dermatologie und Urologie für Pflegeberufe. Stuttgart: Thieme; 2002
[1996] Schrader WF. Altersbedingte Makuladegeneration. Sozioökonomische Zeitbombe in der alternden Gesellschaft. Ophthalmologe 2006; 103: 742–748
[1997] Schwegler J, Lucius R. Der Mensch. Anatomie und Physiologie, 6. Aufl. Stuttgart: Thieme; 2016
40.11.1.2 Erkrankungen des HNO-Bereichs
[1998] Arnold W, Ganzer U. Checkliste HNO. 5. Aufl. Stuttgart: Thieme; 2011
[1999] Boeninnghaus HG. HNO für Studierende in der Medizin. 11. Aufl. Berlin: Springer; 2001
[2000] Böhme G. Sprach-, Sprech-, Stimm- und Schluckstörungen. Band 1: Klinik. 4. Aufl. München/Jena: Urban und Fischer; 2003
[2001] Paetz B, Benzinger-König B. Chirurgie für Pflegeberufe. 22. Aufl. Stuttgart: Thieme; 2013
[2002] Putz R, Pabst R, Hrsg. Sobotta. Atlas der Anatomie des Menschen – Band 1: Kopf, Hals, obere Extremität. München: Urban und Fischer; 2000
[2003] Silbernagl S, Despopoulos A. Taschenatlas der Physiologie. 6. Aufl. Stuttgart: Thieme; 2003
[2004] Simmen D, Jones D. Chirurgie der Nasennebenhöhlen. Thieme; 2005
40.11.1.3 Erkrankungen der Haut
[2005] AWMF Leitlinie: Kontaktekzem (08/2013). Online: http://www.awmf-leitlinien.de; Stand: 19.12.2016. Allergo J Int 2014; 23: 126–38
[2006] AWMF Leitlinie: Leitlinie Neurodermitis [atopisches Ekzem; atopische Dermatitis] (Letzte Überarbeitung: 03/2015). Online: http://www.awmf-leitlinien.de; Stand: 19.12.2016
[2007] AWMF Leitlinie: Staphylococcus aureus bedingte Infektionen (Letzte Überarbeitung: 04.2011). Im Internet: http://www.awmf.org/uploads/tx_szleitlinien/013–038l_S2k_Staphyococcus_aureus_2011-abgelaufen.pdf; Stand: 19.12.2016
[2008] AWMF Leitlinie: Therapie der Psoriasis vulgaris Update 2011. Im Internet: http://www.awmf-leitlinien.de; Stand: 19.12.2016
[2009] Bruck J, Müller FE, Steen M. Handbuch der Verbrennungstherapie. Landsberg am Lech: Ecomed Verlagsgesellschaft; 2002
[2010] Hengge U, Ruzicka T. Lehrbuch der Dermatologie und Venerologie. Stuttgart: Wissenschaftliche; 2006
[2011] Künzi W, Wedler V. Wegweiser Verbrennung. Manno: La Buona Stampa; 2006
[2012] Latasch L, Ruck K, Seiz W. Anästhesie – Intensivmedizin – Intensivpflege. 2. Aufl. München: Urban-Fischer; 2004
[2013] Moll I. Dermatologie. 7. Aufl. Stuttgart: Thieme; 2010
[2014] Plewig, G., Landthaler, M., Burgdorf, W., Hertl, M., Ruzicka, Th.: Braun-Falco's Dermatologie, Venerologie und Allergologie. 6. Auflage Berlin: Springer; 2012
[2015] Wappler F, Spilker G. Verbrennungsmedizin. Stuttgart: Thieme; 2009
40.11.2 Kontakt- und Internetadressen
40.11.2.1 Augenerkrankungen
[2016] Albinismus Selbsthilfegruppe e.V. NOAH. Im Internet: http://www.albinismus.de; Stand: 10.03.2017
[2017] Berufsverband der Augenärzte, Deutschlands e.V. (BVA), 40474 Düsseldorf, Tersteegenstr. 12, 40401 Düsseldorf Postfach 30 01 55, Tel.: 0211/43 037–00, E-Mail: bva@augeninfo.de, Im Internet: http://cms.augeninfo.de/ ; Stand: 19.12.2016
[2018] Deutscher Blinden- und Sehbehindertenverband e.V., Rungestr. 19, 10179 Berlin, Tel.: 030/285 387–0, E-Mail: info@dbsv.org, Tel.: 01805/666 456, Im Internet: http://www.dbsv.org; Stand: 19.12.2016
[2019] Pro Retina Deutschland, Vaalserstr. 108, 52074 Aachen, Tel.: 0241/870 018, E-Mail: info@pro-retina.de, Im Internet: http://www.pro-retina.de; Stand: 19.12.2016
40.11.2.2 Erkrankungen im HNO-Bereich
[2020] http://www.akustikus.de; Stand: 19.12.2016
[2021] http://www.dcig.de; Stand: 19.12.2016
[2022] http://www.forumbesserhoeren.de; Stand: 19.12.2016
[2023] http://www.hno.org; Stand: 19.12.2016
[2024] http://www.rehadat.de; Stand: 19.12.2016
[2025] http://www.schwerhoerigkeit.de/DSB/index2.htm; Stand: 19.12.2016
[2026] http://www.tinnitus-liga.de; Stand: 19.12.2016
40.11.2.3 Erkrankungen der Haut
[2027] http://eczema.dermis.net/content; Stand: 19.12.2016
[2028] http://www.derma.de; Stand: 19.12.2016
40.11.2.4 Verbrennungen
[2029] Bundesverband für Brandverletzte e.V., Dorfstraße 18b, 31020 Salzhemmendorf, E-Mail: brandverletze.leben@t-online.de, Im Internet: http://www.brandverletzte-leben.de; Stand: 19.12.2016
[2030] Deutsche Gesellschaft für Verbrennungsmedizin. Im Internet: http://www.verbrennungsmedizin.de; Stand: 27.01.2017
[2031] Paulinchen e.V., Initiative für brandverletzte Kinder e.V., Segeberger Chausee 35, 22850 Norderstedt, Tel.: 040 529 50 66, E-Mail: info@paulinchen.de, Im Internet: http://www.paulinchen.de; Stand: 19.12.2016
[2032] Phoenix Deutschland, Hilfe für Brandverletzte e.V., Dorfstr. 12, 19273 Amt Neuhaus-Sückau, Tel.: 038841–6 11 80 Im Internet: http://www.phoenix-deutschland.de; Stand: 19.12.2016
[2033] Zentrale Vermittlungsstelle für die Vermittlung von Krankenhausbetten für Schwerbrandverletzte, Feuerwehr Hamburg, Tel.: 040/42 851–39 98 oder 39 99, E-Mail: leitstelle@feuerwehr.hamburg.de; Stand: 07.03.2017